Nat. Chem.:脂肪胺直接对芳香烃胺化 |
您所在的位置:网站首页 › 脂肪胺和芳香胺的结构差别 › Nat. Chem.:脂肪胺直接对芳香烃胺化 |
Nat. Chem.:脂肪胺直接对芳香烃胺化
|
Nat. Chem.:脂肪胺直接对芳香烃胺化
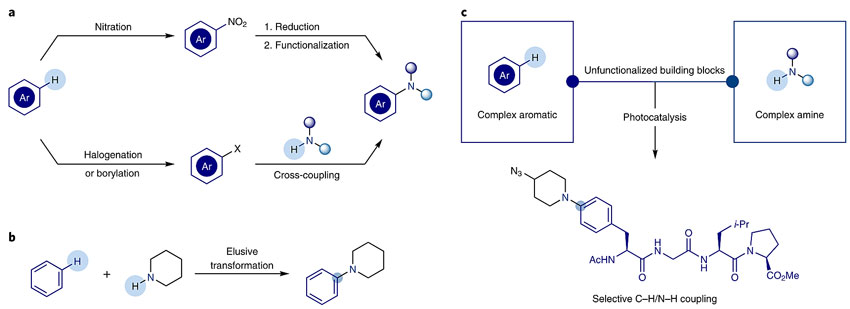
氮是地球上丰富的元素,是医药、农药和有机材料的重要组分。据统计,药物合成中大约有30%的操作涉及氮,但传统的引入氮的方式,不是需要苛刻的条件(如硝化),就是需要卤代或硼酸酯化等预官能化底物(如Buchwald–Hartwig偶联、Ullmann反应和Chan–Lam反应),且这些反应都很难实现区域选择性。以上缺点对含有多种官能团的先导化合物的后期修饰是不利的,因此,实现C-H键的直接胺化无疑是更为步骤经济性和廉价的方案,学术界也为此倾注了大量努力。比如,利用特殊的含氮基团(如酰亚胺、DABCO、唑等)形成的自由基与芳香烃偶联直接构筑C-N键。不过,这些方法实现的前提必须是产生稳定的氮自由基。相比之下,脂肪胺(如烷基胺、吡咯烷、哌啶等)作为自由基前体形成的氮自由基稳定性差,通常会发生自由基移位,形成稳定的α-N-碳自由基;另一方面,想要水解成伯胺后再还原胺化又势必会引入多步操作。
图1. 芳香烃胺化的方法。图片来源:Nat. Chem. 将羟胺作为氮自由基前体可以解决氮自由基稳定性的问题,为此,英国曼彻斯特大学的Daniele Leonori教授(点击查看介绍)设计了一种制备预官能化羟胺的方法(Angew. Chem. Int. Ed., 2017, 56, 14948)。美国北大罗莱纳大学教堂山分校的David A. Nicewicz结合光吖啶类光氧化还原催化剂,在O2的氧化条件下实现了伯烷基胺与富电子芳香烃的偶联,反应中形成伯烷基氨阳离子自由基(Angew. Chem. Int. Ed., 2017, 56, 15644)。但这两类方法同样受到底物适用范围窄的困扰。近日,Daniele Leonori教授课题组利用可见光激发的光催化剂首次实现了脂肪胺对芳香烃的区域选择性直接胺化,无需对芳香烃进行预官能化。反应对一系列官能团兼容,并可实现克量级扩大规模的制备。相关工作发表在Nature Chemistry 上。
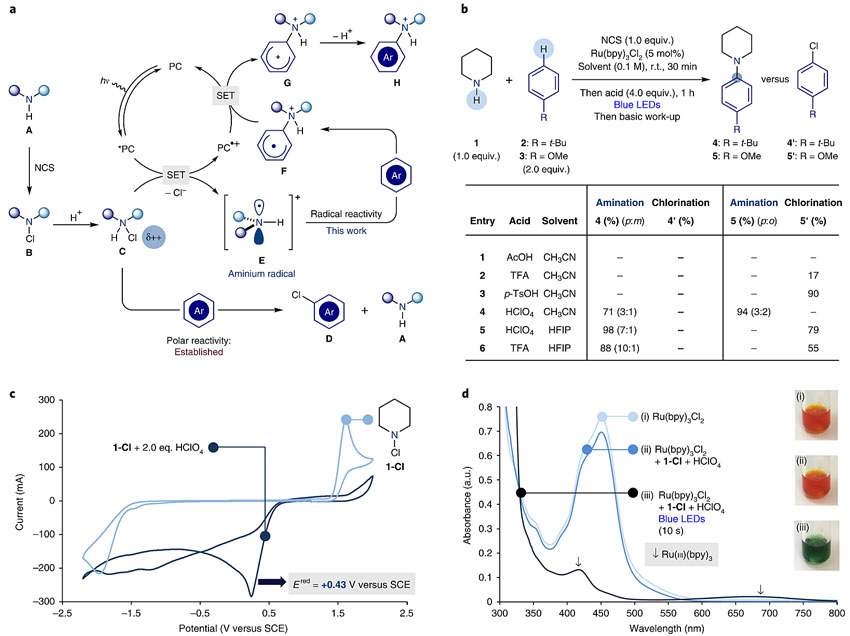
图2. Leonori教授(左四)课题组。图片来源:University of Manchester 一、条件优化 该工作首要的问题是如何高效地产生烷基氮自由基。直接产生氮自由基很难实现,他们采取了对脂肪胺双活化的方式,即先通过NCS进行N-氯代(中间体B)后进行质子化(中间体C),C可以在光催化剂的作用下通过单电子转移(SET)生成铵自由基阳离子(F)。这一过程也得到循环伏安法(CV)的证实(下图c):没有质子化时1-Cl的氧化和还原电势分别是+1.50 V(Eox)和−1.80 V(Ered),而光催化剂的氧化电势为−0.81 V,因此不能发生SET;相反,1-Cl质子化后,其Ered为+0.43 V,意味着可以被激发态的光催化剂还原。更直接的证据来自发射-淬灭实验,只有在质子化后才能观察到处于激发态的光催化剂被1-Cl淬灭的现象(下图d)。 第二个问题是如何避免副反应,因为N-氯代铵C可以对芳香烃进行氯代。研究人员发现,Bronsted酸和溶剂是关键因素(下图b)。在乙腈中,醋酸、TFA和对甲苯磺酸完全不能实现芳香烃胺化;在HFIP中,TFA则只对电中性的叔丁基苯的胺化奏效,而富电子的苯甲醚只能得到氯代副产物;在乙腈中,HClO4则可以促进两种底物均发生胺化,且在HFIP中叔丁基苯甲醚的区域选择性更高(p:m = 7:1)。
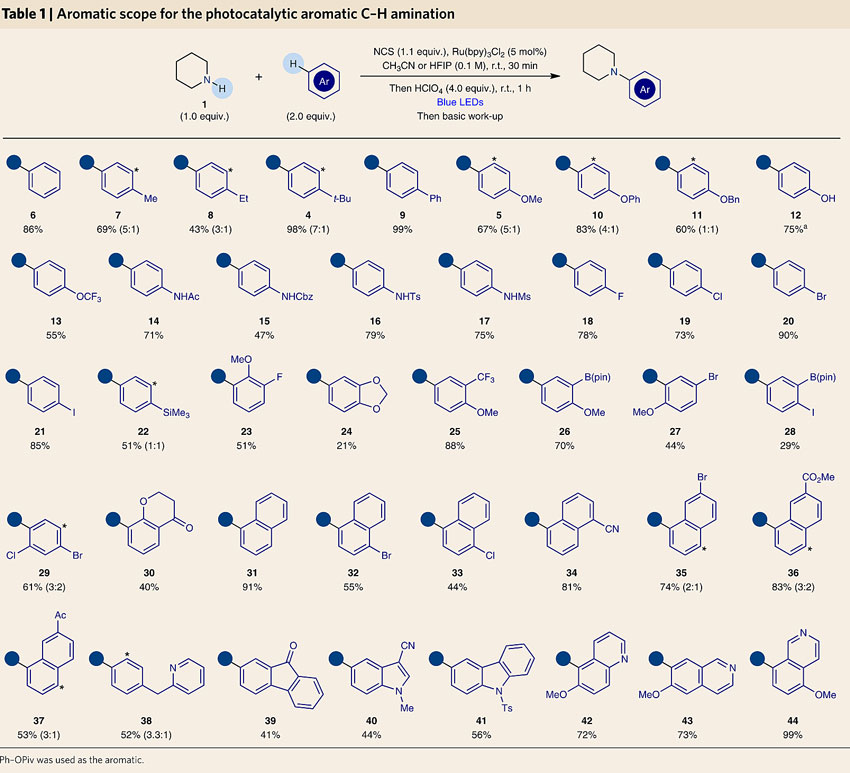
图3. 反应条件的优化。图片来源:Nat. Chem. 二、哌啶对芳香烃的直接胺化 在优化的条件下,研究人员首先用哌啶作为氮源与各种芳香烃进行反应。结果表明,胺化产物主要发生在电子密度最高的位点;单取代的苯主要发生对位胺化(4-22),特别是对卤代芳香烃而言明显优于其他C-H键官能化的方法(18-21);其他多取代的芳香烃和稠环芳烃也能得到相应的产物(22-44),官能团兼容性也较好(如氨基、硅基、醚、硼酸酯等)。值得一提的是,阿斯利康在其实验室采用这种方法实现了21的克量级规模的合成(5.6 g, 67%),而这一砌块通常需要多步才能实现。
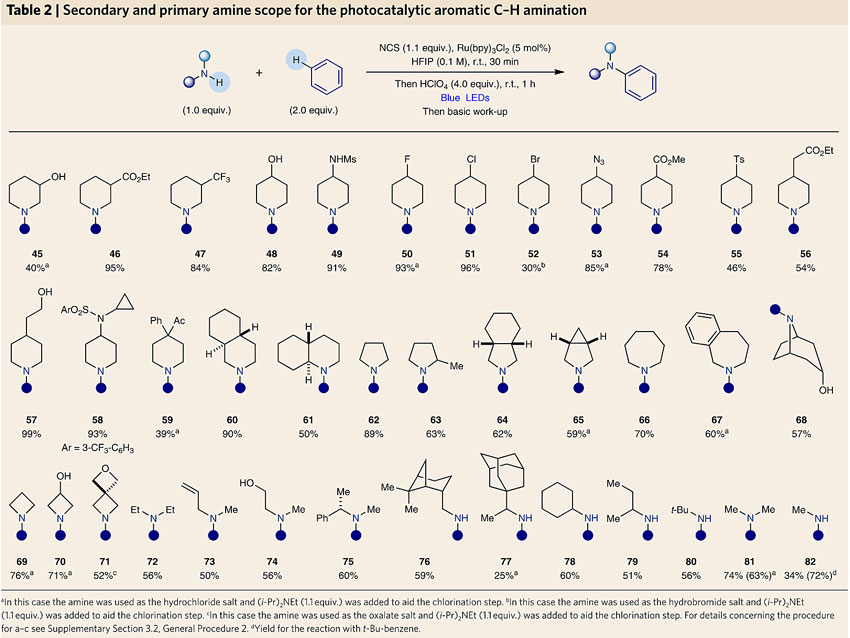
图4. 哌啶和芳香烃的胺化反应。图片来源:Nat. Chem. 三、不同脂肪胺与苯的胺化 研究人员使用38种环状或非环状脂肪胺与苯反应,这些胺即使含有羟基、卤素、酯基、叠氮基、氨基、环丙基和大位阻的环取代基都能得到相应的产物(45-82)。值得一提的是,反应在水相中进行以及使用气态的二甲胺和甲胺也不受影响(81, 82),这也是第一次实现利用气态的胺源作为底物进行C-H键官能化的例子。由此可见,这种方法远比通过硝化/还原胺化更温和,选择性更好。
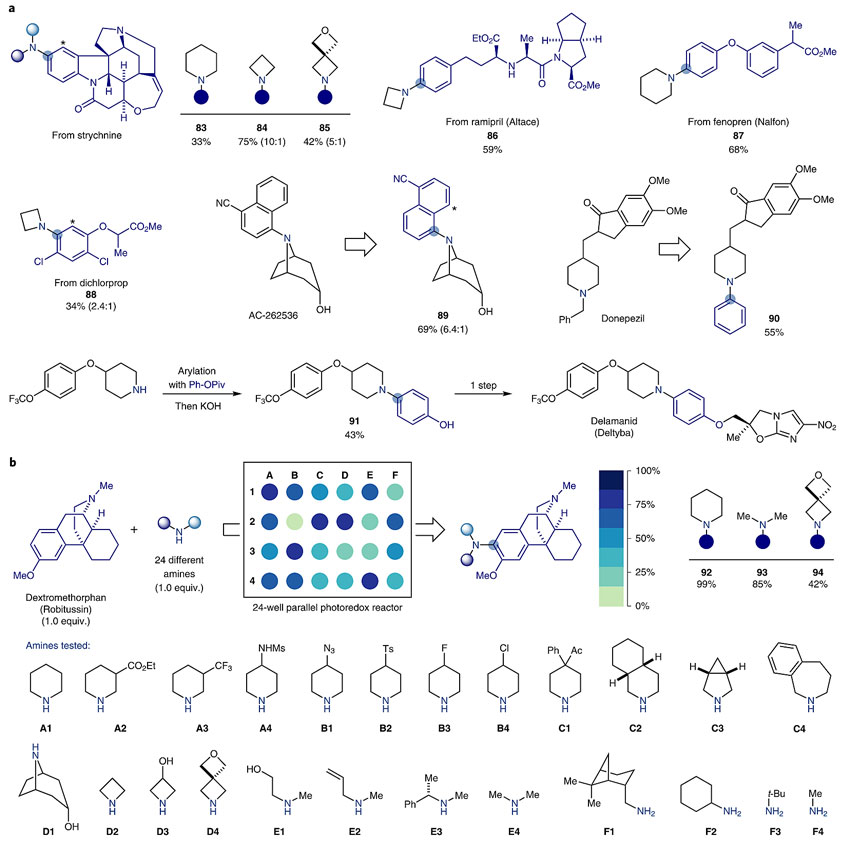
图5. 不同脂肪胺与苯的反应。图片来源:Nat. Chem. 四、在药物后期官能化和平行筛选中的应用 研究人员以马钱子碱(Strychnine)、非诺洛芬(非甾体抗炎药)、2,4-滴丙酸(除草剂)、雷米普利(降压药)作为药物前体进行测试,以上化合物均能胺化(83-88)。他们利用这种方法同样也能得到AC-262536和多奈哌齐的类似物(89, 90),还能简化delamanid(多药耐药性肺结核药)的合成工艺。另外,研究人员还利用商业化的24孔平行光反应器对Robitussin(止咳药)与24种商品化的脂肪胺进行平行反应,大多数都能以超过50%的收率得到相应的胺化产物,大大提高了药物衍生化的效率,阿斯利康正在开发自动化的方法实现其高通量合成。
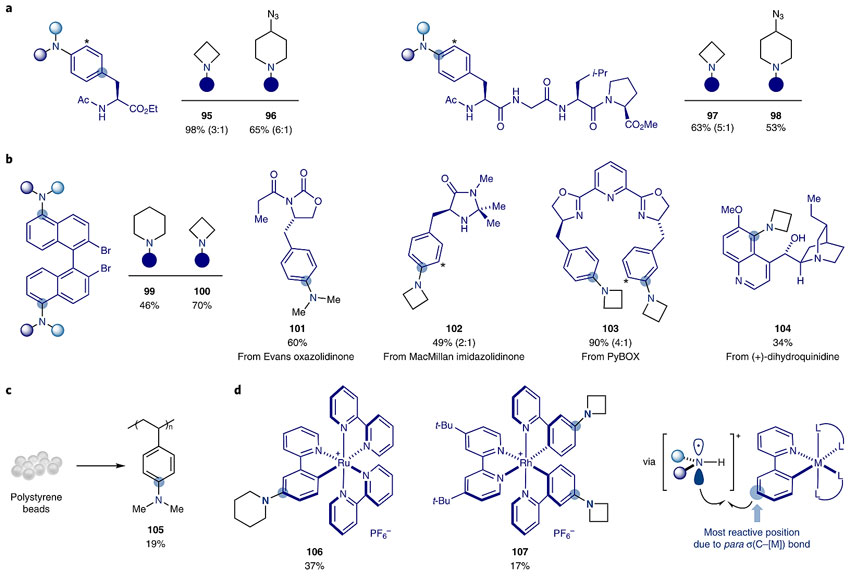
图6. 药物分子的后期衍生化。图片来源:Nat. Chem. 五、其他应用 该方法也能应用在多肽修饰上,不管是简单的色氨酸还是含色氨酸的复杂三肽都能实现其苯环的胺化(95-98);对于手性配体,如Noyori发展的BINAP、Evans手性噁唑啉酮辅基、MacMillan发展的咪唑烷酮和PyBOX以及常用的金鸡纳碱衍生物(+)-二氢奎宁也能顺利地进行修饰(101-104),因此避免了新多肽或配体的从头合成。研究人员还把该方法的应用范围延伸到材料领域,例如对聚合物的聚合后修饰(105)可产生高附加值的新聚合物,也使染料敏化太阳能电池(106)吸收光谱拓展到可见-近红外区。
图7. 芳香烃直接C-H键胺化的其他应用。图片来源:Nat. Chem. 总结 在药物发现中经常使用的策略是“基于结构的药物设计”,这项研究让笔者想到,有机化学的理论已经发展得相当完备了,合成化学应该着重于“基于科学的设计”,而不再是盲目的发现。这种基于科学的设计要求人们更加深刻地理解理论,对于减少不必要的损耗和推动有机化学的发展无疑是更有效的途径。有机合成方法学的最高境界应该是开发普适、高效和绿色的方法学,向满足人类发展需求回归,而不是简单的发文章拿基金。这项工作无疑在这个方向上做出了不错的尝试。 原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):
Practical and regioselective amination of arenes using alkyl amines Alessandro Ruffoni, Fabio Juliá, Thomas D. Svejstrup, Alastair J. McMillan, James J. Douglas, Daniele Leonori Nat. Chem., 2019, DOI: 10.1038/s41557-019-0254-5 导师介绍 Daniele Leonori https://www.x-mol.com/university/faculty/2424 (本文由峰千朵供稿) 如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载! 点击分享 收藏 取消收藏 评论: 0 |
【本文地址】
今日新闻 |
推荐新闻 |