[行业深度报告]融合蛋白:从Technique到Science的进阶之路 |
您所在的位置:网站首页 › 人血清白蛋白制剂来源主要通过基因工程技术制备获取 › [行业深度报告]融合蛋白:从Technique到Science的进阶之路 |
[行业深度报告]融合蛋白:从Technique到Science的进阶之路
|
本文转自平安医药团队公众号,版权归原作者所有,如有侵权,请及时与我们联系,谢谢。 融合蛋白:从Technique到Science的进阶之路(上篇) 平安观点重磅品种的摇篮,整体市场180亿美元。融合蛋白是指利用基因工程等技术将某种具有生物学活性的功能蛋白分子与其他天然蛋白(融合伴侣)融合而产生的新型蛋白。功能蛋白通常是内源性配体(或相应受体),如细胞因子、激素、生长因子、酶等活性物质,融合伴侣主要包括免疫球蛋白、白蛋白、转铁蛋白等。主要作用有两点:1)提高功能蛋白的稳定性、延长在体内的代谢时间;2)融合一个或多个功能片段,形成高效靶向药物。自1998年全球第一个融合蛋白药物依那西普上市以来,全球已经上市了13个Fc融合蛋白药物、2个白蛋白融合蛋白药物、1个CTP融合蛋白药物,合计约180亿美元市场规模。其中依那西普年销售额超过90亿美元,阿柏西普40亿美元、度拉鲁肽9亿美元。 融合蛋白在长效技术中优势明显。人体内存在的天然活性物数量巨大,但目前作用机制明确、应用到治疗领域的仅几十种,并且由于大部分稳定性差、半衰期短,直接作为药物使用需要频繁给药,在临床应用上受到限制。目前蛋白(多肽)药物长效化的实现策略主要包括聚乙二醇化(PEG)、蛋白融合、微球化、糖基化或脂肪酸修饰。几种长效技术各有优劣:PEG修饰应用超过20年,而PEG作为人体内异物有潜在风险;微球对技术和个性化要求高,同时对大分子药物的损耗大;糖基化、脂肪酸修饰等技术的缺点在于后期的修饰改造、纯化较为复杂。融合蛋白技术主要依靠融合伴侣的长效机制,可通过FcRn介导的循环途径和增加分子大小来延长半衰期;从基因水平将融合伴侣与效应分子连接在一起,不需要额外的化学修饰,纯化、制备过程简单,质量控制也相对容易,综合来看是非常有前景的一种长效化手段。 常用的融合伴侣包括抗体Fc、人血清白蛋白和CTP。其中 Fc融合蛋白应用最多,可利用抗体Fc段介导ADCC、CDC等各种生物学功能,并可根据4种亚型介导的细胞毒差异选择融合伴侣。明星产品依那西普、阿柏西普、康柏西普、度拉鲁肽均属于Fc融合蛋白。人血清白蛋白( HSA) 是血浆中含量最多的可溶性蛋白,无免疫原性、组织分布广,本身也是天然载体,GLP-1受体激动剂阿必鲁肽、凝血因子IX白蛋白融合蛋白两个产品上市,近10个产品在研。CTP为人绒毛膜促性腺激素β亚基羧基末端肽,是人体自身的天然长效融合伴侣,所以免疫源性非常低;构建突变体时不需要插入连接序列而直接在C端或 N端融合,设计简单灵活。目前CTP融合类产品仅默克公司的绒促卵泡素α注射剂在欧洲上市,近十款产品处于在研阶段。 展开全文重磅品种的摇篮,整体市场180亿美元。融合蛋白是指利用基因工程等技术将某种具有生物学活性的功能蛋白分子与其他天然蛋白(融合伴侣)融合而产生的新型蛋白。功能蛋白通常是内源性配体(或相应受体),如细胞因子、激素、生长因子、酶等活性物质,融合伴侣主要包括免疫球蛋白、白蛋白、转铁蛋白等。主要作用有两点:1)提高功能蛋白的稳定性、延长在体内的代谢时间;2)融合一个或多个功能片段,形成高效靶向药物。自1998年全球第一个融合蛋白药物依那西普上市以来,全球已经上市了13个Fc融合蛋白药物、2个白蛋白融合蛋白药物、1个CTP融合蛋白药物,合计约180亿美元市场规模。其中依那西普年销售额超过90亿美元,阿柏西普40亿美元、度拉鲁肽9亿美元。 融合蛋白在长效技术中优势明显。人体内存在的天然活性物数量巨大,但目前作用机制明确、应用到治疗领域的仅几十种,并且由于大部分稳定性差、半衰期短,直接作为药物使用需要频繁给药,在临床应用上受到限制。目前蛋白(多肽)药物长效化的实现策略主要包括聚乙二醇化(PEG)、蛋白融合、微球化、糖基化或脂肪酸修饰。几种长效技术各有优劣:PEG修饰应用超过20年,而PEG作为人体内异物有潜在风险;微球对技术和个性化要求高,同时对大分子药物的损耗大;糖基化、脂肪酸修饰等技术的缺点在于后期的修饰改造、纯化较为复杂。融合蛋白技术主要依靠融合伴侣的长效机制,可通过FcRn介导的循环途径和增加分子大小来延长半衰期;从基因水平将融合伴侣与效应分子连接在一起,不需要额外的化学修饰,纯化、制备过程简单,质量控制也相对容易,综合来看是非常有前景的一种长效化手段。 常用的融合伴侣包括抗体Fc、人血清白蛋白和CTP。其中 Fc融合蛋白应用最多,可利用抗体Fc段介导ADCC、CDC等各种生物学功能,并可根据4种亚型介导的细胞毒差异选择融合伴侣。明星产品依那西普、阿柏西普、康柏西普、度拉鲁肽均属于Fc融合蛋白。人血清白蛋白( HSA) 是血浆中含量最多的可溶性蛋白,无免疫原性、组织分布广,本身也是天然载体,GLP-1受体激动剂阿必鲁肽、凝血因子IX白蛋白融合蛋白两个产品上市,近10个产品在研。CTP为人绒毛膜促性腺激素β亚基羧基末端肽,是人体自身的天然长效融合伴侣,所以免疫源性非常低;构建突变体时不需要插入连接序列而直接在C端或 N端融合,设计简单灵活。目前CTP融合类产品仅默克公司的绒促卵泡素α注射剂在欧洲上市,近十款产品处于在研阶段。 风险提示 研发风险;行业政策风险。
一、 融合蛋白:重磅品种的摇篮,整体市场180亿美元 融合蛋白是指利用基因工程等技术将某种具有生物学活性的功能蛋白分子与其他天然蛋白(融合伴侣)融合而产生的新型蛋白。功能蛋白通常是内源性配体(或相应受体),如细胞因子、激素、生长因子、酶等活性物质,融合伴侣主要包括免疫球蛋白、白蛋白、转铁蛋白等。主要作用有两点:1)提高功能蛋白的稳定性、延长在体内的代谢时间;2)融合一个或多个功能片段,形成高效靶向药物。
自1998年全球第一个融合蛋白药物依那西普上市以来,全球已经上市了13个Fc融合蛋白药物、2个白蛋白融合蛋白药物、1个CTP融合蛋白药物,合计约180亿美元市场规模。以自身免疫病为应用最广泛的适应症,包括5个融合蛋白,依那西普年销售额超过90亿美元。其次是眼科药阿柏西普,单药销售额40亿美元;糖尿病药物为两个GLP-1融合蛋白,Fc融合GLP-1药物度拉鲁肽(9亿美元)和白蛋白融合GLP-1药物阿必鲁肽;以及抗贫血药、Fc融合血小板生成素拟肽罗米司亭。
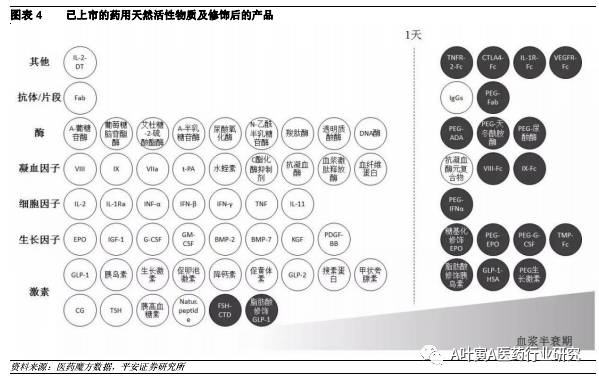
二、 融合蛋白在长效技术中优势明显 2.1天然活性物半衰期短,催生多种长效化手段 抗体融合蛋白越来越多地应用到靶向药领域,但早期融合蛋白主要是作为长效化的一种技术手段而产生,随着越来越多天然生物活性物质的药效作用被发现,融合蛋白的长效机制将在更多领域得到应用。人体内存在的天然活性物数量巨大,但目前作用机制明确、应用到治疗领域的仅几十种,并且由于大部分稳定性差、半衰期短,直接作为药物使用需要频繁给药,在临床应用上受到限制。如人体自身产生的GLP-1 血浆半衰期不足2分钟,普通重组IL-2体内半衰期仅为6.9 min,其他大部分半衰期都在1天以内,经过长效化加工后半衰期可大幅延长,给药频率可下降至每周甚至每月1次。
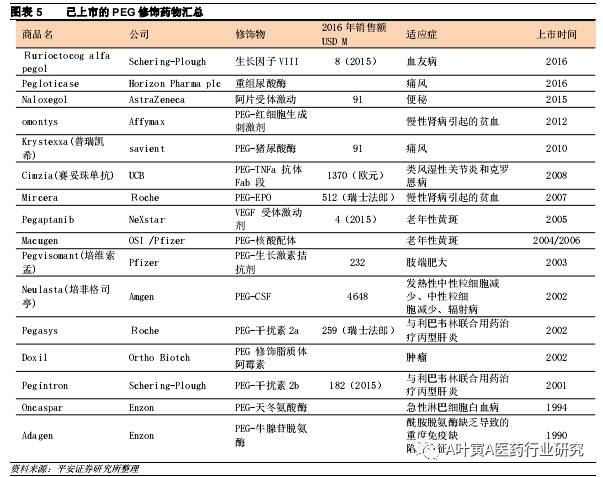
2.2 融合蛋白由于为内源性、制备相对简单,优势明显 目前蛋白(多肽)药物长效化的实现策略主要包括聚乙二醇化(PEG)、蛋白融合、微球化、糖基化或脂肪酸修饰。几种长效技术各有优劣:PEG修饰应用超过20年,而PEG作为人体内异物有潜在风险;微球对技术和个性化要求高,同时对大分子药物的损耗大,不适用于成本高的药;糖基化、脂肪酸修饰等技术的缺点在于后期的修饰改造、纯化较为复杂。融合蛋白技术主要依靠融合伴侣的长效机制,可通过FcRn介导的循环途径和增加分子大小来延长半衰期;从基因水平将融合伴侣与效应分子连接在一起,不需要额外的化学修饰,纯化、制备过程简单,质量控制也相对容易,综合来看是非常有前景的一种长效化手段。 2.2.1聚乙二醇化(PEG) 聚乙二醇是一种无活性的亲水性化合物,聚乙二醇化就是将聚乙二醇通过生物技术安装到具有活性的蛋白质分子之上,提高分子量降低血浆和肾脏清除率。聚乙二醇可形成良好的遮蔽作用,使蛋白质不易受到各种蛋白酶的攻击,降解速率明显降低;分子量达到或超出肾小球滤过作用的阈值时可以逃避肾小球滤过作用,降低肾脏清除率。同时聚乙二醇具有空间位阻,将蛋白质表面的抗原决定簇掩盖起来,降低免疫源性。其缺点在于聚乙二醇也可能遮蔽蛋白质分子的功能区域,降低其活性;此外,有研究表明PEG成分与肾小管上皮细胞空心化有关,存在潜在风险;小分子PEG有肾脏毒性,大分子PEG在体内降解机制不明。
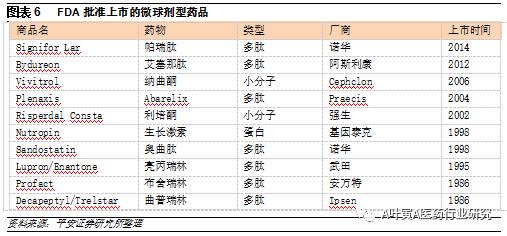
2.2.2 微球技术 微球是药物溶解或分散于高分子材料(骨架)中所形成的微小球体或类球体,随着骨架的缓慢溶解微球小体内的药物逐步释放发挥作用,溶解速率可控,用药频率可下降至每3个月注射1次。缺点在于针对不同的应用需要个性化的设计和生产,而生产过程中对药物的稳定性有影响,部分药物的损失高达25%-50%。目前FDA已批准十余个产品上市,包括多肽和蛋白类激素、小分子精神类用药。微球技术壁垒较高,国内只有丽珠集团等少数几家企业具备。
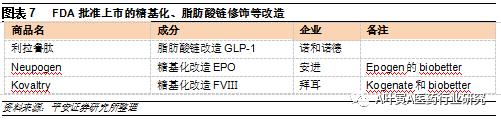
2.2.3糖基化、脂肪酸链修饰等改造 蛋白质表面的糖链、脂肪链等侧链可遮蔽蛋白水解酶位点,阻碍蛋白酶对蛋白药物的降解作用;蛋白质药物表面增加了侧链,提高蛋白质稳定性,分子量增大也可减少肾小球滤过;脂肪酸可与人血清白蛋白可逆结合,复合体在跨膜转运中受限从而延长在体内的储留时间。该类技术的缺点在于后期的修饰改造、纯化较为复杂。 以利拉鲁肽为例,其97%的氨基酸序列和人GLP-1分子相同,增加的脂肪酸侧链可以使利拉鲁肽在血夜中与白蛋白可逆性地结合,使利拉鲁肽的作用时间延长,且增强对DPP-4酶降解的抵抗,脂肪酸侧链还可以使利拉鲁肽分子在注射部位自交联成七聚体,从而延缓其自皮下吸引,使其作用时间可长达接近24小时,每天注射一次并且与进餐时间无关。
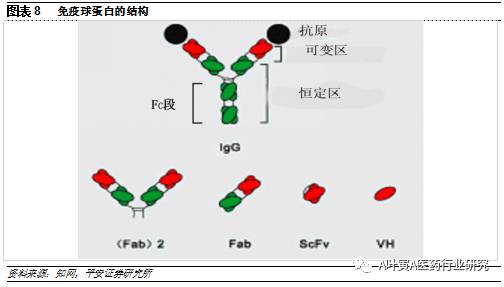
2.2.4融合蛋白 目前主要包括Fc融合、白蛋白融合以及转铁蛋白融合等,三者均可通过新生儿Fc受体(FcRn)介导的循环途径和增加分子大小来延长半衰期。其他方式还包括惰性蛋白融合如XTEN融合、HAP融合、ELP融合等,以及最新的负电蛋白融合如CTP融合等。以Fc融合为例,Fc片段与FcRn的结合是pH敏感型的形式,抗体通过胞饮作用进入细胞,在酸性pH的内涵体中,抗体与FcRn结合,FcRn介导抗体回到细胞外,在胞外中性pH条件下,与FcRn解离,这样避免了抗体通过胞饮作用进入细胞内被溶酶体降解,从而达到长效目的。 三、 常用几种融合技术 3.1 Fc融合蛋白:应用最多,可介导免疫反应 目前最常用的融合伴侣为免疫球蛋白IgG的Fc段,抗体Fc是抗体恒定区的一部分(包括铰链区-CH2-CH3,而不包括抗体恒定区的CH1部分)。与Fc段融合后通过增加分子量、FcRn介导的再循环机制增加融合分子的稳定性、延长体内半衰期,同时可利用Fc段介导ADCC、CDC等各种生物学功能,但此类融合蛋白没有抗体的可变区,其药理和药效仍主要取决于与Fc融合的功能分子。
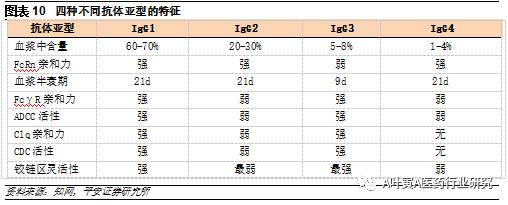
人免疫球蛋白G 有4 个亚型,不同免疫球蛋白G 亚型的生物学活性有所差异( 表3) 。对于抗肿瘤药物而言Fc段的细胞毒作用和补体激活作用可以帮助药物发挥更好的药效,而对于类风湿性关节炎,糖尿病等疾病就需要以降低。目前应用最多的是IgG1亚型抗体,近年来随着新适应症的拓展、新作用机制抗体药物的发现,细胞毒性较低的IgG2、IgG4 亚型抗体得到重视。
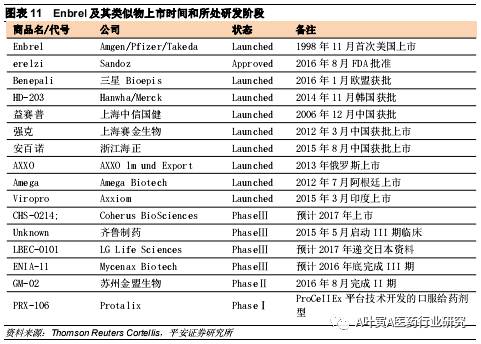
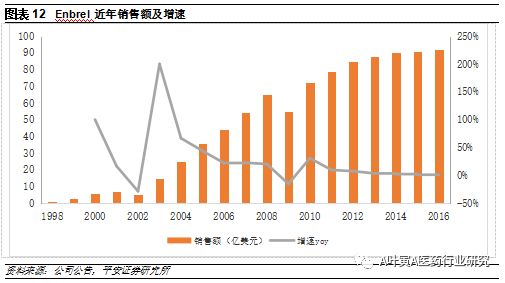
3.1.1依那西普 依那西普(原研商品名Enbrel)是第一个也是目前最畅销的融合蛋白药物, 1998年由安进研发上市,2016年销售额接近88.74亿美元。目前该药主要获批5大适应症:类风湿性关节炎(RA)、斑块型银屑病(PsO)、银屑病关节炎(PsA)、强直性脊柱炎(AS)及幼年特发性关节炎(JIA)。2016年1月,欧盟批准了首个Enbrel的生物类似药Benepali,该类似药由三星Bioepis开发,百健负责在欧盟地区的销售。Enbrel美国地区的专利则被安进成功延长到2028年,其他国家则有8个类似物上市。
该产品由安进负责美国市场销售,辉瑞负责欧洲销售,武田与辉瑞在日本共同销售,勃林格殷格翰负责中国市场销售。增速从2010年的10%逐步下降至1%,销售额稳定在92亿美元左右。
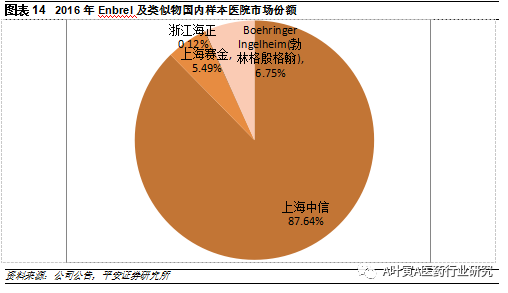
国内自2006年中信国健益赛普获批以来,目前已有三家企业的类似物上市,其他两家赛金、海正分别于2012、2015年上市,原研药2010年2月获CFDA批准。中信国健的益赛普2016年销售额达9.25亿元,先发优势明显,从样本医院数据来看,益赛普占比高达88%,原研、赛金、海正占比分为6.75%、5.49%和0.12%。
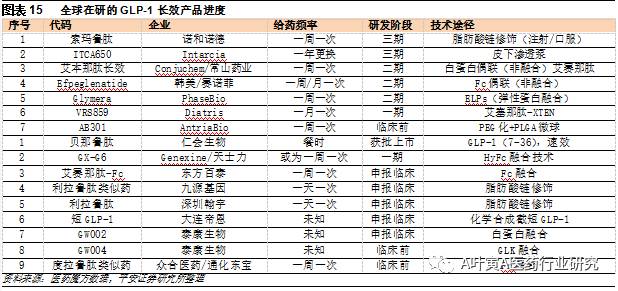
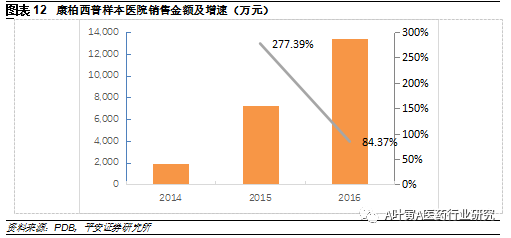
3.1.2阿柏西普&康柏西普 阿柏西普原研Eylea由Regeneron与拜耳的合作开发下成功推向市场,于2011年上市,2015年销售额达到40亿美元。Zaltrap成分与Eylea一样,用于转移性结直肠癌,由赛诺菲负责销售。康柏西普郎沐由成都康弘开发,商品名朗沐,主要用于治疗湿性年龄相关性黄斑变性。康柏西普于2013年11月CFDA获批、2014年4月国内上市,2016年销售额4.76亿元。该药是中国首个拥有自主知识产权的获得世卫组织国际通用名的生物1类新药,今年通过谈判降价17%后进入医保目录。 3.1.3度拉鲁肽 Trulicity(Dulaglutide)是胰高血糖素样肽1(GLP-1)Fc融合蛋白,每周注射一次,疗效不劣于利拉鲁肽。由礼来研发于2014年9月获得FDA批准上市,2015年、2016年销售额分别为2.49亿美元、9.26亿美元,增长迅速。GLP-1受体激动剂是目前认为最有效的降糖药,但人体天然的GLP-1半衰期短,如何长效化是目前主要的研究方向。在研产品几乎用到了所有的长效技术手段,包括融合蛋白、脂肪酸链修饰、PEG化和微球。索玛鲁肽一周一次的注射剂三期临床结束,已向7家药监机构提交上市申请。其他多个一周一次甚至一月一次的注射剂处于临床一、二期。
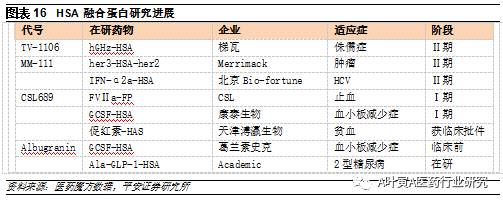
3.2 白蛋白融合:天然药物载体,多个产品在研 人血清白蛋白( HSA) 是血浆中含量最多的可溶性蛋白,有调节渗透压、营养、作为天然载体等作用,半衰期长达19 d。由于HAS无免疫原性、组织分布广,本身也是天然载体,可在酵母中大量表达降低成本,是非常理想的药物融合载体。 Ø阿必鲁肽(Tanzeum) 胰高血糖素样肽-1( GLP-1) 和HSA 的融合蛋白,GSK研发于2014 年4月FDA 批准,是全球首个HSA 融合蛋白药物。其DPP-IV 水解位点的丙氨酸被替换为谷氨酸,其半衰期长达6 ~ 8 d,一周注射一次。但在一项全球841名对照试验中,阿必鲁肽的 HbA1c下降幅度小于利拉鲁肽(GLP-1酰化后产物)。 Ø凝血因子IX白蛋白融合蛋白(Idelvion) CSL 开发的凝血因子IX白蛋白融合蛋白产品Idelvion于2016 年1 月获批上市,适用在儿童和成年有血友病B( 先天性凝血因子IX 缺乏),用药频率为1-2周每次。血友病B是一种罕见的遗传性血液疾病,患者可能会长时间或自发性出血,特别是渗入肌肉、关节或内脏等器官组织。根据美国疾病控制和预防中心(CDC)估计,该疾病约在每25000名男性新生儿中出现一例,女性患者非常罕见。在次之前用于治疗的制剂包括新鲜血浆、凝血酶原复合原复合物、高度提纯的FⅨ和重组FⅨ,FⅨ半衰期为18~24h,应每12~24小时输注1次才能维持血液FⅨ水平。
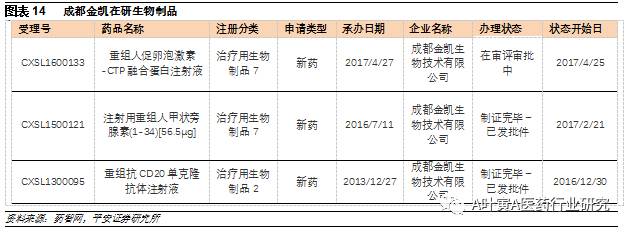
3.3 CTP融合:天然长效融合伴侣,无需连接序列 CTP为人绒毛膜促性腺激素β亚基羧基末端肽,早期发现CTP是因为人们观察到绒毛膜促性腺激素和黄体化激素两者结构相似,但半衰期却差别很大,分别为2天和20分钟,而主要原因是前者有CTP。它可以增加重组融合蛋白唾液酸含量,唾液酸能增加黏蛋白的黏度, 遮蔽蛋白上的糖链, 使其不被糖苷酶水解,保护蛋白质免受蛋白酶降解;同时可提高蛋白质糖基化程度,增加分子量,因此可以获得更长的药物体内半衰期。 CTP是人体自身的天然长效融合伴侣,所以免疫源性非常低,半CTP融合蛋白药物Elonva只有0.2%患者产生了抗药抗体,而Fc融合开发依那西普有5%患者产生了抗药抗体。在分子水平,该技术具有设计简单灵活的特性,构建突变体时不需要插入连接序列而直接在C端或 N端融合。 默克公司的绒促卵泡素α注射剂(商品名Elonva)于2010年在欧洲上市,这是目前唯一一款获批的CTP融合蛋白药物,与常用重组卵泡刺激素(rFSH)药效学一致,将早期1天1次的注射频率降低至1周1次,估计2016年销售额接近2.5亿美元。国内信立泰子公司成都金凯的重组人促卵泡激素-CTP融合蛋白于今年4月申报临床,目前处于审评审批中。全球其他在研产品中进度较快的生长激素CTP融合蛋白处于III期临床阶段,由OPKO与辉瑞合作开发。
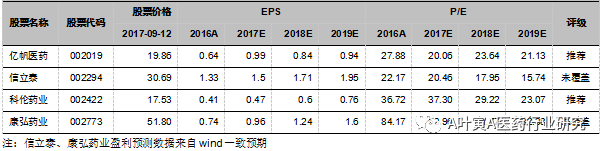
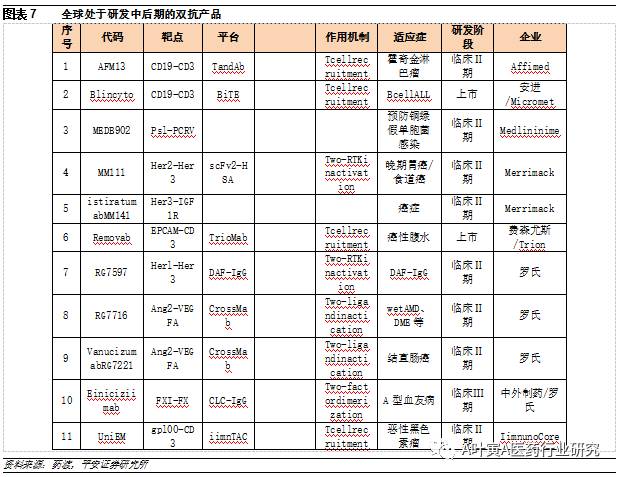
四、风险提示 研发风险;行业政策风险。 融合蛋白:从Technique到Science的进阶之路(下篇) 原创2017-09-12平安医药团队 平安观点抗体融合蛋白VS单抗:从早期的疗效无差异到更优。抗体融合蛋白和单克隆抗体的结构和作用机理相似,融合蛋白可连接多个受体结构域从而结合更多类型相似配体,理论上可达到更好的效果。随着DNA重组、蛋白表达等技术的成熟,融合蛋白将应用于更多靶向药物的开发。依那西普与英夫利昔单抗、阿达木单抗作用有细微差别,依那西普能结合更多型TNF配体、并且不裂解细胞造成额外损伤,但三者临床疗效无显著差异。雷珠单抗、康柏西普、阿柏西普均是VEGF靶点抑制剂,由于两个融合蛋白包含多个功能结构域,能与VEGF-A、VEGF-B以及PIGF结合,而雷珠单抗只与VEGF-A结合。头对头试验中阿柏西普疗效优于雷珠单抗。 双抗技术平台优化升级,国内企业快速跟进。T细胞募集型通过结合T细胞上靶点以及肿瘤细胞上的特异靶点,诱导免疫细胞杀伤肿瘤细胞;非T细胞募集型即两个靶点均位于肿瘤细胞上,阻断两条信号通路使疾病控制率更好、减少耐药产生。由于两抗体的结合方式多达50多种,出现了多个不同的双抗合成技术平台。各平台重点解决的问题包括:1)解决错配问题;2)蛋白结构的稳定性;3)后期的纯化;4)如何平衡两个抗体的表达量。目前公认比较有潜力的平台包括BiTE、CrossMAB、Triomab等,BiTE分子量小效率高、稳定性强,Crossmab解决了错配问题。目前全球超过120种双特异性抗体分子进入临床管线,预计超过10个双抗产品处于临床Ⅱ/Ⅲ期。国内双抗技术跟进较快,友芝友的Ybody、健能隆的iTAB、Epimab的FIT-Ig平台均为自主开发,博生吉应用的BiTE技术,信达主要来自与Adimab和岸迈的合作。从融资情况来看,去年9家国内布局双抗研发企业完成融资或并购,涉及金额达到21.44亿元,同比增长211.6%。 国内处于产业化初期,公司各有特色。亿帆医药(002019)的双分子平台效果强于普通Fc融合,第一个产品长效G-CSF预计明年完成三期临床申报FDA、2019年美国上市。自主研发的ITabTM双抗平台技术国际领先,在BiTE的基础上做改进,使得产品半衰期更长、副作用更小,表达系由原核改为真核细胞。国内首个双抗A-337澳洲一期临床获批。康弘药业(002773)核心产品康柏西普是我国首个拥有自主知识产权的获得世卫组织国际通用名的生物1类新药,2016年国内销售额为4.76亿元,随着纳入医保目录和适应症扩展,未来还有较大空间。信立泰(002294)是国内CTP 融合技术快速跟进者,其重组人促卵泡激素-CTP融合蛋白于今年4月申报临床,目前处于审评审批中,是默克Elonva的类似物。科伦药业(002422)的多西他赛-白蛋白结合型、重组人血小板生成素拟肽-Fc融合蛋白的临床注册已受理。 抗体融合蛋白VS单抗:从早期的疗效无差异到更优。抗体融合蛋白和单克隆抗体的结构和作用机理相似,融合蛋白可连接多个受体结构域从而结合更多类型相似配体,理论上可达到更好的效果。随着DNA重组、蛋白表达等技术的成熟,融合蛋白将应用于更多靶向药物的开发。依那西普与英夫利昔单抗、阿达木单抗作用有细微差别,依那西普能结合更多型TNF配体、并且不裂解细胞造成额外损伤,但三者临床疗效无显著差异。雷珠单抗、康柏西普、阿柏西普均是VEGF靶点抑制剂,由于两个融合蛋白包含多个功能结构域,能与VEGF-A、VEGF-B以及PIGF结合,而雷珠单抗只与VEGF-A结合。头对头试验中阿柏西普疗效优于雷珠单抗。 双抗技术平台优化升级,国内企业快速跟进。T细胞募集型通过结合T细胞上靶点以及肿瘤细胞上的特异靶点,诱导免疫细胞杀伤肿瘤细胞;非T细胞募集型即两个靶点均位于肿瘤细胞上,阻断两条信号通路使疾病控制率更好、减少耐药产生。由于两抗体的结合方式多达50多种,出现了多个不同的双抗合成技术平台。各平台重点解决的问题包括:1)解决错配问题;2)蛋白结构的稳定性;3)后期的纯化;4)如何平衡两个抗体的表达量。目前公认比较有潜力的平台包括BiTE、CrossMAB、Triomab等,BiTE分子量小效率高、稳定性强,Crossmab解决了错配问题。目前全球超过120种双特异性抗体分子进入临床管线,预计超过10个双抗产品处于临床Ⅱ/Ⅲ期。国内双抗技术跟进较快,友芝友的Ybody、健能隆的iTAB、Epimab的FIT-Ig平台均为自主开发,博生吉应用的BiTE技术,信达主要来自与Adimab和岸迈的合作。从融资情况来看,去年9家国内布局双抗研发企业完成融资或并购,涉及金额达到21.44亿元,同比增长211.6%。 国内处于产业化初期,公司各有特色。亿帆医药(002019)的双分子平台效果强于普通Fc融合,第一个产品长效G-CSF预计明年完成三期临床申报FDA、2019年美国上市。自主研发的ITabTM双抗平台技术国际领先,在BiTE的基础上做改进,使得产品半衰期更长、副作用更小,表达系由原核改为真核细胞。国内首个双抗A-337澳洲一期临床获批。康弘药业(002773)核心产品康柏西普是我国首个拥有自主知识产权的获得世卫组织国际通用名的生物1类新药,2016年国内销售额为4.76亿元,随着纳入医保目录和适应症扩展,未来还有较大空间。信立泰(002294)是国内CTP 融合技术快速跟进者,其重组人促卵泡激素-CTP融合蛋白于今年4月申报临床,目前处于审评审批中,是默克Elonva的类似物。科伦药业(002422)的多西他赛-白蛋白结合型、重组人血小板生成素拟肽-Fc融合蛋白的临床注册已受理。 风险提示研发风险;行业政策风险;个股风险。 研发风险;行业政策风险;个股风险。
四、抗体融合蛋白VS单抗:从早期的疗效无差异到更优 抗体融合蛋白和单克隆抗体的结构和作用机理相似,融合蛋白可连接多个受体结构域从而结合更多类型相似配体,理论上可达到更好的效果。随着DNA重组、蛋白表达等技术的成熟,融合蛋白将应用于更多靶向药物的开发。 4.1 依那西普与单抗作用有细微差别,临床疗效无显著差异 依那西普是TNF-α受体融合蛋白,通过特异性地与TNF-α结合,竞争性地阻断TNF-α与细胞表面的TNF受体结合,从而抑制由TNF-α介导的异常免疫反应及炎症过程。长期安全性和疗效已在临床上得到了证明。 4.1.1依那西普能结合更多型TNF配体、不裂解细胞 依那西普、英夫利昔单抗和阿达木单抗都是类风湿关节炎(RA)治疗的有效肿瘤坏死因子抑制剂(TNFis),是类风关一线生物用药,作用机制类似但仍有一些差别。从结构来看依那西普是由人肿瘤坏死因子受体2(TNFR2/p75)的胞外配体结合部位与人IgG1的Fc片段连接组成,英夫利昔单抗、阿达木单抗分别是TNFα的人鼠嵌合抗体、TNFα的全人源抗体;从结合的配体来看,依那西普可结合可溶性TNFα、膜结合型TNFα、TNFβ,其余两个单抗不能结合TNFβ,由于TNFβ同样有介导免疫反应的作用,所以阻断TNFβ通路也有缓解炎症的作用;从细胞毒性来看,体外试验显示依那西普不裂解表达膜结合型TNFα的细胞,而英夫利昔单抗可通过补体和抗体依赖性细胞毒作用导致细胞溶解,带来额外损伤;从免疫源性看,依那西普和阿达木单抗均为全人源,免疫源性弱,而英夫利昔单抗是人鼠嵌合型抗体(25%鼠源),具有一定的免疫源性,但联合甲氨碟呤用药可减少人抗嵌合体抗体的产生。
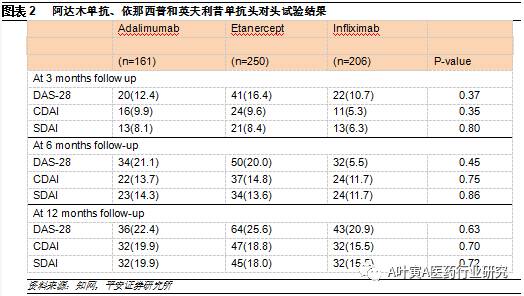
4.1.2三种TNF抑制剂临床疗效无显著差异 有效性方面,目前没有证据表明三种肿瘤坏子因子抑制剂的治疗效果有显著差异。在一项样本量617人的对照试验中,阿达木单抗、依那西普和英夫利昔单抗良好反应的比例分别为 59.6%、59.2%、51.9%(P=0.21),在统计学上无显著差异。主要观察指标包括临床的疾病活动指数(CDAI)、简化的疾病活动指数(SDAI)、疾病活动指数28(DAS28)三项,均无统计学差异。
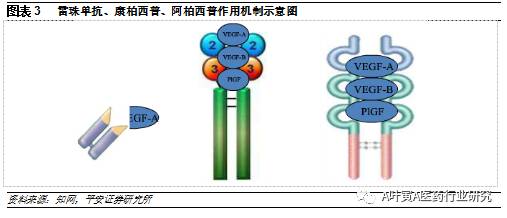
4.2 阿柏西普疗效优于雷珠单抗 雷珠单抗、康柏西普、阿柏西普是治疗湿性黄斑病变的一线生物用药,均为血管内皮生长因子(VEGF)抑制剂,阻断VEGF靶点下游信号通路,抑制新生血管生成、降低血管通透性。从结构上看,阿柏西普和康柏西普是重组VEGFR融合蛋白,阿柏西普由VEGFR1区域2、VEGFR2区域3与IgG1 Fc段融合而成,康柏西普增加了VEGFR2区域4,由VEGFR1区域2、VEGFR2区域3和4与IgG1 Fc段融合而成,两者均能与VEGF-A、VEGF-B以及PIGF结合;雷珠单抗是人源化鼠抗VEGF-A抗体Fab段,只与VEGF-A结合。有效性方面,在一项660例头对头试验中阿柏西普疗效优于雷珠单抗,尤其是对于基线视力较差的患者。在视力方面,1年后阿柏西普组提高13.3个字母,雷珠单抗组11.2个字母;在解剖学结构方面,阿柏西普组的中央区视网膜厚度降低169μm,雷珠单抗组147μm。雷珠单抗与康柏西普暂无头对头试验比较。
五、双抗技术平台优化升级,国内企业快速跟进 5.1 借助免疫系统杀伤肿瘤,CAR-T技术升级版 双特异性抗体指是含有2种特异性抗原结合位点的人工抗体,常用基因工程制备方法,属于融合蛋白。按照靶点一般分为T细胞募集型和非T细胞募集型:(1)T细胞募集型通常包含CD3、CD16等靶点,通过结合T细胞上的CD3靶点以及肿瘤细胞上的特异靶点,诱导T细胞杀伤肿瘤细胞,相当于CAR-T技术的升级版。另一个靶点位于肿瘤细胞,阻断信号通路抑制肿瘤细胞生长。(2)非T细胞募集型即两个靶点均位于肿瘤细胞上,阻断两条信号通路使疾病控制率更好、减少耐药产生。双特异性抗体还有特殊作用,如与转铁蛋白结合穿过血脑屏障,用于阿尔茨海默症等脑部疾病的治疗。
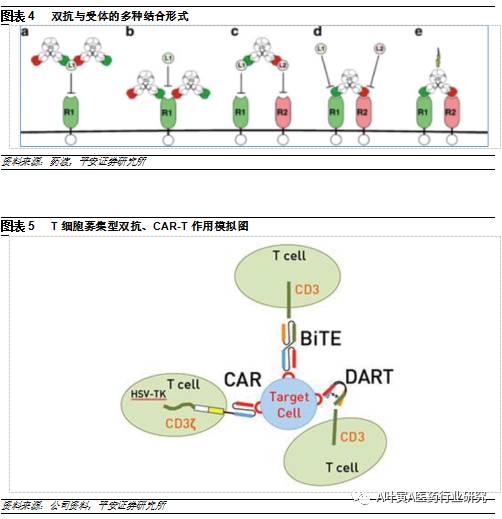
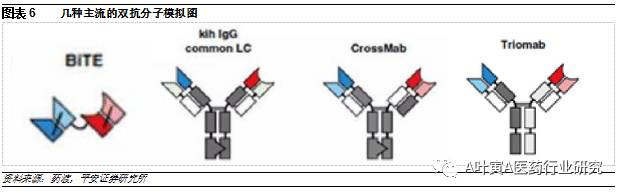
5.2 不同平台各有优劣,重点解决错配、稳定性问题 双抗的合成技术从早期直接将两单抗化学偶联到现在逐步被基因工程技术替代,由于两抗体的结合方式多达50多种,出现了多个不同的双抗合成技术平台。各平台重点解决的问题:1)解决错配问题;2)蛋白结构的稳定性;3)后期的纯化;4)如何平衡两个抗体的表达量。目前公认比较有潜力的平台包括BiTE、CrossMAB、Triomab等。
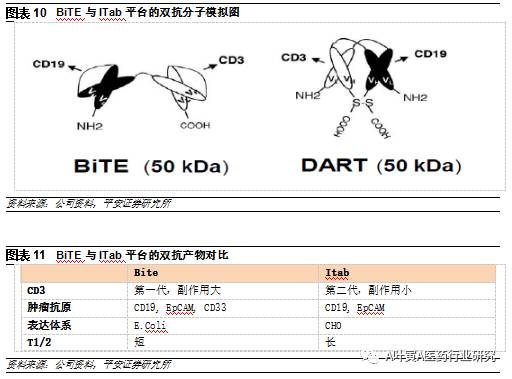
5.2.1 BiTE:效率高、稳定性强 BiTE又称双特异性T细胞衔接器,即两个抗体的可变区通过一条多肽链连接,最早由Micromet开发,后被安进收购。BiTE特点包括:1)通过CD3靶向连接激活T细胞,借助人体免疫杀伤肿瘤细胞;2)由于分子量低,容易穿透肿瘤组织、亲和力强,裂解肿瘤细胞的效率是普通单抗的100-10000倍;3)缺乏Fc段,免疫源性低;4)无需糖基化,具有较高的稳定性和均一性。 目前全球仅上市Removab(费森尤斯)和Blincyto(安进)两款双抗产品,Blincyto即采用的BiTE技术,双靶点为CD3和CD19,用于治疗B细胞急性淋巴细胞白血病。在一项有185名患者的试验中,32%的受试者大约在6.7个月的时间未出现疾病证据(完全缓解)。2014年底由FDA批准上市,2015年数据未披露,估计为7000万美元。Removab由杂交瘤细胞获得,用于治疗肿瘤恶性腹水,目前销售状况不佳。 5.2.2 Crossmab:解决错配问题,在研产品进度最快 1990s基因泰克发明的Knobs-into-holes(KiH)解决了重链正确联结的问题,罗氏的crossmab技术在KiH方案的基础上,进一步解决了轻链错误联结的问题,成为目前最有前景的双抗技术之一。基于该平台的ACE-910已进入临床三期,是目前研发进展最快的双抗产品,有望在2年内上市。ACE-910用于Ⅷ因子缺乏的血友病患者,两个靶点分别结合Ⅸ因子和Ⅹ因子,促使两者结合从而激活Ⅹ因子,从而实现Ⅷ因子的生理功能,在疗效、半衰期、安全性等方面优于重组Ⅷ因子。 5.3 全球预计超过10个双抗产品处于临床Ⅱ/Ⅲ期 目前全球超过120种双特异性抗体分子进入临床管线,据不完全统计,处于临床Ⅱ/Ⅲ期的双抗产品9个,其中3个为含有CD3靶点T细胞募集型免疫双抗。从公司来看,罗氏占到4个产品,Merrimack(被易普森收购)占2个产品。
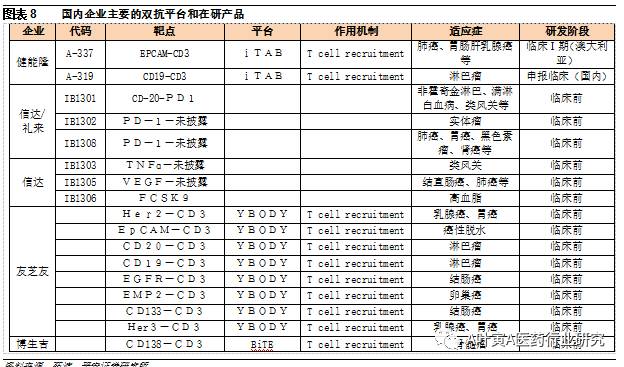
5.4 国内双抗技术快速跟进,一级市场热度高 国内双抗技术跟进较快,主要企业包括武汉友芝友、健能隆、信达生物、岸迈生物、博生吉等。友芝友的Ybody、健能隆的iTAB、Epimab的FIT-Ig平台均为自主开发,博生吉应用的BiTE技术,信达主要来自与Adimab和岸迈的合作,健能隆、友芝友和博生吉在研产品均为T细胞募集型。目前健能隆的两个产品进度最快,其中针对多种实体瘤的EPCAM-CD3双抗已获得澳大利亚批准进入Ⅰ期临床,针对淋巴瘤的CD19-CD3已向CFDA申报临床。
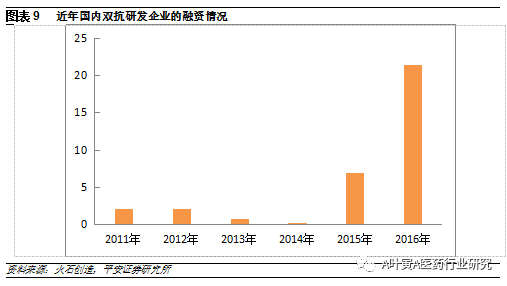
从融资情况来看,去年9家国内布局双抗研发企业完成融资或并购,涉及金额达到21.44亿元,同比增长211.6%。一级市场的火热一方面反映出资本对双抗技术前景的看好,另一方面也为双抗的发展提供资金保障。
六、 国内处于产业化初期,公司各有特色 6.1亿帆医药:双分子平台+双抗平台 亿帆医药主营业务包括原料药和化学制药两大板块。公司为全球最大的泛酸钙生产商,产能8000吨,市占率60%。制剂方面,公司传统优势产品包括头孢他啶、阿奇霉素、长春西汀等,近年通过并购丰富了妇科、血液科、皮肤科等产品线,同时通过收购健能隆切入大分子生物药领域,进一步增强了研发实力。 6.1.1 双分子平台:更高效的Fc长效融合技术 2016年7月公司以10亿人民币收购健能隆53.8%股权,健能隆拥有DiKineTM双分子和ITabTM免疫抗体两大新药研发平台。其中双分子平台的原型是Fc融合蛋白技术,相当于在Fc上加两个相同的功能蛋白片段,因为通常细胞膜上的受体激活过程中受体二聚化是一个重要步骤,所以双分子结构除了Fc融合带来的长效性外,还具有更强的生物活性,目前全球没有同类产品上市。平台在研的长效G-CSF(F-627)二期临床试验数据较好,预计明年完成三期临床申报FDA、2019年美国上市。自主首创新药普罗纳亭(F-652,白介素-22-Fc)已进入两项国际二期临床和中国一期临床,长效生长激素F-899将进入临床申报阶段,目前长春高新上市的长效生长激素应用的是PEG修饰技术。销售方面,安进的第二代长效升白药年销售额近50亿美元,据IMS预测,公司产品F-627如果第二位获批将获得20%的市场份额约10亿美元。上市后的销售三种模式都有考虑:与美国大的商业公司合作,收购一家有市场能力、资源的公司,或者完全代理模式。 6.1.2 双抗平台:BiTE技术改良版,国内研发进度最快 自主研发的ITabTM双抗平台技术国际领先,在BiTE的基础上做改进,使得产品半衰期更长、副作用更小,表达系由原核改为真核细胞。公司的首个双抗A-337澳洲一期临床获批,靶点与Catumaxomab相同,均为EPCAM-CD3,但免疫源性做了优化。针对B淋巴细胞瘤双抗F319今年7月正式申报,在国内申请临床,按照目前CFDA对创新药的审批进度有望6-12个月获批。
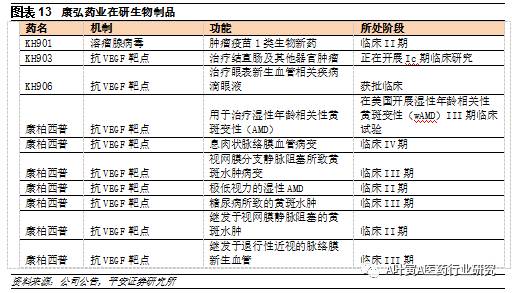
6.1.3 创始团队背景实力强 健能隆的创始团队在管理、研发、生产各领域都有很强的背景。CEO黄予良博士曾在德国生物科技中心做研究,后加入美国EGENCORPORATION,担任中国分公司总经理;2001年加入Hong Kong Pharmaceuticals(香港主板上市),并任首席科技总监,从事生物医药工艺、厂房建设运营和公司管理20余年。 首席科学官严孝强博士早期在安进从事肿瘤、自身免疫性疾病等方面的研究,参与多个大分子蛋白药物临床前研发;2002年加入和记黄埔任副总裁,主管新药研发与技术、建立肿瘤和自身免疫性疾病新药研发平台。首席医学官汤凯扬博士曾任美国法玛西亚/辉瑞临床开发总监、和记黄埔临床和注册部副总裁,具有丰富的临床方案设计和临床实验管理经验,精通FDA/EMA /CFDA临床研究法规并有与多国药监药审部门的沟通申报经验。黄予良、严孝强和汤凯扬分别持股11.06%、10.89%和4.22%,收购前后几乎不变。 公司主营业务方面,13个品种进入医保目录,是公司未来三年的业绩增长的主要动力;头孢他啶价格维护良好,特定代理业务稳步增长;泛酸钙原料药价格近期受环保和夏季检修影响大幅上涨,从上半年均价来看也高于去年均价,预计2017-2018都将处于高景气度。预计公司2017-2019年EPS分别为0.99、0.84、0.94元,维持“推荐”评级。 6.2 康弘药业:抗体融合蛋白技术国际领先 公司是国内少有的生物创新药稀缺标的,核心产品康柏西普是我国首个拥有自主知识产权的获得世卫组织国际通用名的生物1类新药,直接进入美国FDA三期临床。康柏西普于2014年在国内上市,2016年国内销售额为4.76亿元,随着纳入医保目录和适应症扩展,未来还有较大空间。目前国内黄斑变性患者约500万人,其中湿性黄斑占比约10%,每年新增30万人。治疗药物主要有雷珠单抗、阿柏西普和康柏西普,雷珠单抗2012年引进国内,阿柏西普已报CFDA、进入优先审评通道。进入医保后支付标准较原中标价降低17%,降价幅度较小。目前两种产品在国内湿性年龄相关性黄斑变性患者中渗透率约10%,市场规模约12亿元;进入医保目录后假设渗透率到达50%、考虑降价因素后国内整体空间将达到50亿元;假设公司市占率50%,则公司国内市场销售额将达到25亿元。
6.3信立泰:CTP 融合技术快速跟进 公司是国内心血管领域优秀的仿创型企业,2014年收购生物药研发型公司成都金凯,目前持股比例90%。成都金凯具备抗体药物和蛋白药物优化创新的 FC 嵌合技术平台和 CTP 嵌合技术平台。其重组人促卵泡激素-CTP融合蛋白于今年4月申报临床,目前处于审评审批中,是默克Elonva的类似物。
促卵泡激素FSH是一种由脑垂体分泌的高度糖基化蛋白,其主要生理作用是促进女性卵泡发育和男性精子成熟,广泛用于辅助生育治疗过程中。我国城市人口中不孕不育发病率约为12.5%左右,并在逐年提高;同时随着国家放开二孩政策,需要辅助生育治疗的群体数量呈不断增加的趋势。根据IMS数据,2016年 FSH相关药品在国内市场的销售总额为35亿元人民币。FSH分为尿源提纯和重组两类,尿源产品以丽珠集团为代表,重组产品以默克、长春高新为代表。国内均为短效产品,需每日注射。Elonva是全球唯一上市的一款FSH长效产品,将注射频率下降至每周1次。国内仅成都金凯一家申报其生物类似物,除此外康宁杰瑞的重组人促卵泡激素Fc融合蛋白注射液已于2016年8月获得临床批件。
6.4 科伦药业:蛋白融合+蛋白结合技术 公司是国内输液龙头企业,自2012年底全面启动创新转型战略,目前研发人员千余人。公司在研的创新药达到59个,适应症以肿瘤、肝病、麻醉镇痛等领域为主。小分子创新药42个,其中创新靶点25个,占比达到60%;生物大分子共17个创新药,其中10个为全新靶点。上半年5个创新产品获临床受理、1个获批临床,包括多西他赛-白蛋白结合型,重组人血小板生成素拟肽-Fc融合蛋白。结合型蛋白与融合型蛋白的区别在于前者运用纳米技术将不同蛋白分子结合,而后者运用基因工程技术在蛋白表达前的DNA层面进行拼接。 近年公司收入增长稳定,利润受折旧摊销、研发费用、市场拓展费用增加等因素影响,呈现负增长。大输液板块除集中度提升外,包装升级替换、治疗性输液占比的增加以及双腔(多腔)袋产品的上市预计未来输液业务将有10%左右的增速。抗生素板块,伊犁川宁一期硫红满产,二期青霉素、三期头孢受环保核查影响预计9月恢复生产。创新药板块随着国内药审加快将不断催化,同时公司采取早期授权的形式,首付款有望计入今年收入。预计公司2017-2019年EPS分别为0.47 、0.60 、0.76元,维持“推荐”评级。 六、 风险提示 研发风险;行业政策风险;个股风险
责任编辑: |
【本文地址】
今日新闻 |
推荐新闻 |












 返回搜狐,查看更多
返回搜狐,查看更多