下图是制备和研究乙炔的性质实验装置图.下列说法不正确的是A. 制备乙炔的反应原理是CaC2+2H2O Ca(OH) 2+C2H2↑ B. c的作用是除去影响后续实验的杂质C. d中的有机产物与AgNO3溶液混合能产生沉淀D. e中的现象说明乙炔能被高锰酸钾酸性溶液氧化 题目和参考答案 |
您所在的位置:网站首页 › 电石制备乙炔的实验 › 下图是制备和研究乙炔的性质实验装置图.下列说法不正确的是A. 制备乙炔的反应原理是CaC2+2H2O Ca(OH) 2+C2H2↑ B. c的作用是除去影响后续实验的杂质C. d中的有机产物与AgNO3溶液混合能产生沉淀D. e中的现象说明乙炔能被高锰酸钾酸性溶液氧化 题目和参考答案 |
下图是制备和研究乙炔的性质实验装置图.下列说法不正确的是A. 制备乙炔的反应原理是CaC2+2H2O Ca(OH) 2+C2H2↑ B. c的作用是除去影响后续实验的杂质C. d中的有机产物与AgNO3溶液混合能产生沉淀D. e中的现象说明乙炔能被高锰酸钾酸性溶液氧化 题目和参考答案
|
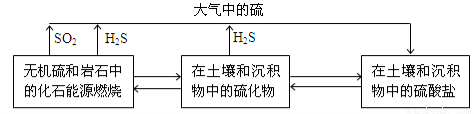
(14分)硫化物在自然界中的部分循环关系如下。
(1)H2S在空气中可以燃烧。 已知: 2H2S(g) + O2(g) S(s) + O2(g) H2S(g)与O2(g)反应产生SO2(g)和H2O(g)的热化学方程式是 。 (2)SO2是大气污染物,海水具有良好的吸收SO2的能力,其过程如下。 ① SO2溶于海水生成H2SO3,H2SO3最终会电离出SO32—,其电离方程式是 。 ② SO32—可以被海水中的溶解氧氧化为SO42—。海水的pH会 (填“升高” 、“不变”或“降低”)。 ③ 为调整海水的pH,可加入新鲜的海水,使其中的HCO3—参与反应,其反应的离子方程式是 。 ④ 在上述反应的同时需要大量鼓入空气,其原因是 。 (3)自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO4溶液,向地下深层渗透,遇到难溶的ZnS,慢慢转变为铜蓝(CuS),用化学用语表示由ZnS转变为CuS的过程: 。 (4)SO2和O2在H2SO4溶液中可以构成原电池,其负极反应式是 。
|
【本文地址】
今日新闻 |
推荐新闻 |
 2S(s) + 2H2O(g) ΔH= -442.38 kJ/mol ①
2S(s) + 2H2O(g) ΔH= -442.38 kJ/mol ①