有机化学基础 |
您所在的位置:网站首页 › 环戊二烯和环丙烯连在一起有芳香性吗 › 有机化学基础 |
有机化学基础
|
一、芳香性:
1.芳香族化合物的定义:
2.芳香性:
2.1判断的基本标准:
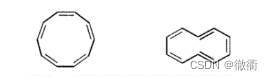
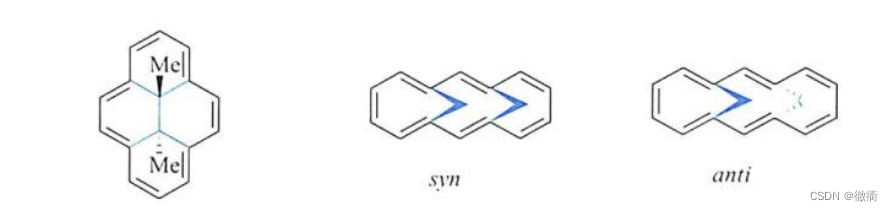
①具有环系的共轭双键。②每个碳上都有未参与杂化的p轨道且参与电子离域。③碳骨架属于平面结构。 2.2芳香性的其他条件:①Π电子离域。 2.3反芳香性的其他条件:①Π电子离域。②能量大幅度提升(环丁二烯)。 2.4 芳香性与反芳香性判断的经验规则(休克尔规则):①Π电子数目为4n+2,具备芳香性。②Π电子数目为4n,具备反芳香性。 3.轮烯: 3.1轮烯的定义:共轭(单双键交替出现)的单环多烯(环丁二烯、苯环)。 3.2轮烯的性质:化学(能量)差别大(有的芳香性(苯环)、有的反芳香性(环丁二烯的能量高于1,3-丁二烯))。 3.3 环辛四烯:非平面结构,不具有芳香性。 3.4 {10}-轮烯不具备芳香性的原因:①顺式结构和反式结构的差异:顺式结构中的H全部朝着环外的方向,反式结构中的H有的朝着环内,有的朝着环外。②顺式(左侧):非平面,船式结构。③反式(右侧):非平面,中间位置(C1和C6)的两个H存在空间位阻。
环扩大,整体相对松弛。 3.6[14]-轮烯以及[4n+2]-轮烯具备芳香性的原子:在经验规则判断的基础上,环内的H造成的空间位阻减少,环不会变形。 4.周边共轭体系化合物的芳香性: 4.1存在形式:在共轭轮烯的环中引入单键相连的原子。 4.2性质影响:引入单键相连的原子可以避免H的空间效应,化学性质趋向于碳直连后的化合物。([10]-环烯和萘)
4.3例题:前后芳香性判断:
5.离子化合物的芳香性:
5.2环戊二烯的芳香性: 5.2.1环戊二烯负离子:环戊二烯脱去顶端C上的一个H之后再补充一个电子,形成环戊二烯负离子,具有4n+2离域Π电子且符合其他休克尔规则,故具有芳香性。
5.3环庚三烯的芳香性: 5.3.1正离子&负离子:正离子Π电子数属于4n+2,符合芳香性。负离子Π电子数属于4n,符合反芳香性。 6.多环(稠环)分子的芳香性: 6.1六元环并接六元环的芳香性(线性稠环体系、角状稠环体系):由于是多个苯环并接而成,苯环的平面性、4n+2电子性、Π电子离域性使得稠密分子也具备芳香性。 6.2六元环并接其他环的分子: 6.2.1环对于芳香性的影响:环中碳原子数量大于5,会避免环内张力过大而使得整个分子非平面形。 6.3分子内没有六元环的多环体系:
6.4富瓦烯类化合物的芳香性: 6.4.1表现形式:环丙烯、环戊二烯、环庚三烯的顶端加上一个双键。
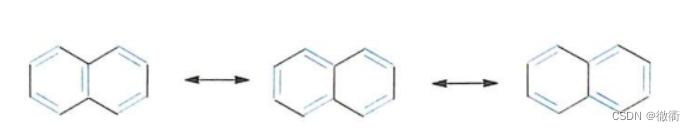
7.1离域的特性:在Y的中间位置离域。 7.2胍的性质的电子轨道解释:成为骨架的N、C原子都是sp2杂化结构,下侧的两个N上的p轨道有两个电子和碳氮双键上的两个电子共轭。胍的性质稳定,碱性强。 8.芳香族化合物分析: 8.1苯: 8.1.1苯与共轭二烯烃的性质差异:苯的单双键之间性质等同,共轭双键之间的单键有趋向于双键的性质,但终究还是以单键性质为主。 8.1.2苯的化学性质(易取代难加成):①加成之后,苯变成1,3-环己二烯,能量升高不稳定(▲H>0,▲G<0,难以发生反应)。②取代之后,仍然有完整的芳香性,能量升高变化不大,可以发生反应。 8.2萘: 8.2.1共振式之间的差异:
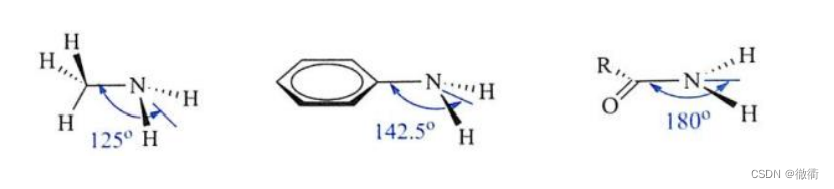
相比较而言,前者相比于后两者都能凑出一个完整的苯环结构,电子离域更强。后两者具有“琨”的结构,电子的共轭效应更差,相比于前者能量更高,更不稳定。 8.2.2萘的电子轨道:呈现“十电子十原子”的共轭体系。 8.3酚: 8.3.1与醇的对比:无论是哪一种杂化,都以稳定为第一原则。醇上的O是sp3杂化,杂化后的氧的2s还是2p轨道的能量值和发生降低。酚上的氧为了能够和苯环上的Π电子发生离域,采取sp2杂化,剩下的p轨道参与离域。 8.3.2酚的共轭式:键长平均化后,碳氧键具有双键的性质。 8.4胺: 8.4.1与氨类似:氮上的孤对电子和苯环共轭,趋向于sp2杂化结构。 8.4.2比较酰胺、脂肪胺、苯胺之间的电子结构:酰胺处于完全的sp2杂化结构,脂肪胺处于完全的sp3杂化结构,苯胺介于这两种杂化结构之间。 8.5硝基苯: 8.5.1硝基苯的电子轨道结构:硝基苯上的氮属于sp2杂化结构。与苯环完全平行。 |
【本文地址】
今日新闻 |
推荐新闻 |

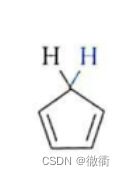 5.1奇数碳原子化合物的芳香性:由于奇数,不存在单双键交替,可以通过负离子或者正离子实现对于p轨道的补充从而实现Π电子离域。
5.1奇数碳原子化合物的芳香性:由于奇数,不存在单双键交替,可以通过负离子或者正离子实现对于p轨道的补充从而实现Π电子离域。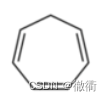 5.2.2环戊二烯正离子:在强酸的条件下失去一个电子,环内仅存在4n个离域Π电子,具备反芳香性,能量更高更不稳定。
5.2.2环戊二烯正离子:在强酸的条件下失去一个电子,环内仅存在4n个离域Π电子,具备反芳香性,能量更高更不稳定。 6.3.1 电子趋向带来的芳香性:分子内可以通过借电子而实现4n+2的电子趋向,在下示的“薁“中,七元环中含有三个共轭双键,具有六个电子。五元环中含有两个共轭双键,具有四个电子。在离域共轭体系当中,七元环将电子转移给五元环,使得五元环具有4n+2的趋势,两者合并具有芳香性。(可以理解为环戊二烯负离子和环庚三烯正离子的组合)
6.3.1 电子趋向带来的芳香性:分子内可以通过借电子而实现4n+2的电子趋向,在下示的“薁“中,七元环中含有三个共轭双键,具有六个电子。五元环中含有两个共轭双键,具有四个电子。在离域共轭体系当中,七元环将电子转移给五元环,使得五元环具有4n+2的趋势,两者合并具有芳香性。(可以理解为环戊二烯负离子和环庚三烯正离子的组合)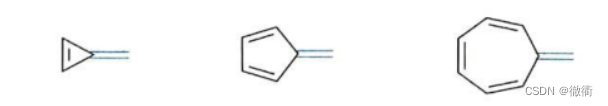
 6.4.2具备芳香性的方法:富瓦烯类化合物外的碳碳双键不参与环内的芳香性,环外双键通过链接其他烯烃的极性满足休克尔规则。如下所示,环戊二烯和环乙烯通过双键相连。环戊二烯夺取双键上的两个Π电子,变成环戊二烯负离子,满足休克尔规则。环乙烯通过失去一个p轨道上Π电子而变成环乙烯正离子,满足休克尔规则。
6.4.2具备芳香性的方法:富瓦烯类化合物外的碳碳双键不参与环内的芳香性,环外双键通过链接其他烯烃的极性满足休克尔规则。如下所示,环戊二烯和环乙烯通过双键相连。环戊二烯夺取双键上的两个Π电子,变成环戊二烯负离子,满足休克尔规则。环乙烯通过失去一个p轨道上Π电子而变成环乙烯正离子,满足休克尔规则。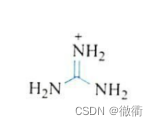 7.Y-芳香性:
7.Y-芳香性: