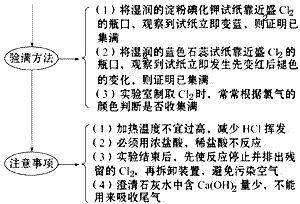
高中化学之气体的收集、净化、干燥 |
您所在的位置:网站首页 › 氯气的实验室制法尾气处理化学方程式 › 高中化学之气体的收集、净化、干燥 |
高中化学之气体的收集、净化、干燥
|
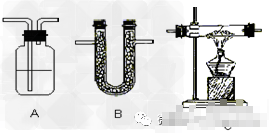
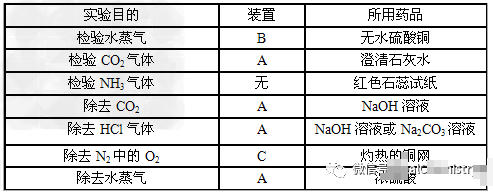
2.气体净化: 装置:
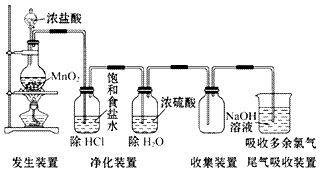
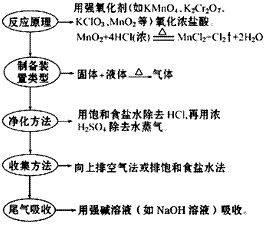
3.气体干燥: (1)干燥原则: 干燥剂只能吸收气体中含有的水分而不能与气体发生反应。 ①酸性干燥剂不能干燥碱性气体。 ②碱性干燥剂不能干燥酸性气体。 ③具有强氧化性的干燥剂不能干燥具有强还原性的气体。注意H2、CO、SO2虽具有还原性,但可用浓H2SO4干燥。 (2)常见物质干燥 氯气的实验室制法: (1)实验室用浓盐酸和二氧化锰反应制取氯气。 (2)装置图:
(3) 步骤:
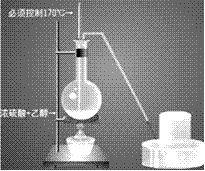
氯气的工业制法: (1)电解饱和食盐水(氯碱工业),化学方程式为: (2)电解熔融的氯化钠(可制得金属蚋),化学方程式为: (3)电解熔融的氯化镁(可制得金属镁),化学方程式为: 实验室制取甲烷(CH 4 ): (1)反应原理:CH 3 COONa+NaOH CH 4 +Na 2 CO 3 (2)发生装置:固+固 气 (3)净化方法:浓硫酸(除水蒸气) (4)收集方法:排水集气法/向下排空气法 (5)尾气处理:无 (6)检验方法:①点燃,淡蓝色火焰,燃烧产物是H 2 O和CO 2 实验室制取一氧化氮(NO): (1)反应原理:3Cu+8HNO 3 (稀)==3Cu(NO 3 ) 2 +2NO↑+4H 2 O (2)发生装置:固+液→气 (3)净化方法:浓硫酸(除水蒸气) (4)收集方法:排水集气法 (5)尾气处理:收集法(塑料袋) (6)检验方法:无色气体,暴露于空气中立即变为红棕色 实验室制取二氧化氮(NO 2 ): (1)反应原理:Cu+4HNO 3 (浓)==Cu(NO 3 ) 2 +2NO 2 ↑+2H 2 O (2)发生装置:固+液→气 (3)净化方法:浓硫酸(除水蒸气) (4)收集方法:向上排空气法 (5)尾气处理:碱液吸收 (3NO 2 +H 2 O==2HNO 3 +NO;NO+NO 2 +2NaOH===2NaNO 2 +H 2 O) 实验室制取氯化氢(HCl): (1)反应原理:2NaCl+H 2 SO 4 Na 2 SO 4 +2HCl? (2)发生装置:固+液→气 (3)净化方法:浓硫酸(除水蒸气) (4)收集方法:向上排空气法 (5)尾气处理:水(防倒吸装置) (6)检验方法:①能使湿润的蓝色石蕊试纸变红 ②靠近浓氨水冒白烟 实验室制取硫化氢(H 2 S): (1)反应原理:FeS+2HCl→H 2 S↑+FeCl 2 (2)发生装置:固+液→气(启普发生器) (3)净化方法:饱和NaHS(除HCl),固体CaCl 2 (除水蒸气) (4)收集方法:向上排空气法 (5)尾气处理:CuSO 4 溶液或碱液吸收(H 2 S+2NaOH==Na 2 S+H 2 O或H 2 S+NaOH==NaHS+H 2 O) (6)检验方法:①湿润的蓝色石蕊试纸变红 ②湿润的醋酸试纸黑 乙烯的制取: (1)实验室里是把酒精和浓硫酸按1:3混合迅速加热到170℃,使酒精分解制得。浓硫酸在反应过程里起催化剂和脱水剂的作用。 制取乙烯的反应属于液--液加热型 C 2 H 6 O CH 2 =CH 2 ↑+H 2 O (2)装置图:
(3) 注意事项: ①酒精和浓硫酸按体积1比3混和,使乙醇利用率提高,必须使用无水酒精,而且必须控制170摄氏度才能制得乙烯。装置连接时由下至上,由左至右。温度计插入液面下。 ②烧瓶内加沸石以避免暴沸。 ③温度计水银头插入液面下,但不要接触烧瓶底部,以测定液体温度。 ④要使液面温度迅速升到170摄氏度,以避免副反应发生。 (4)收集方法:乙烯的密度与空气相当,所以不能用排空气取气法,只能用排水法收集。 检验:点燃时火焰明亮,冒黑烟,产物为水和CO 2 ;通入酸性高锰酸钾溶液中,紫色高锰酸钾褪色。 (5)实验现象:生成无色气体,烧瓶内液体颜色逐渐加深。 (6)两点说明 ①实验室中用无水乙醇和浓硫酸制取乙烯气体,加热不久圆底烧瓶内的液体容易变黑,原因是:浓硫酸将无水乙醇氧化生成碳单质等多种物质,碳单质使烧瓶内的液体带上了黑色。制得的C2H4中往往混有 等气体。 ②实验时要求使反应温度迅速卜升到170℃并稳定在170℃左右,因该温度下主要产物是乙烯和水,而在140℃时主要产物是乙醚和水,当温度高于170℃ 时,乙醇和浓硫酸发生的氧化反应更加突出,反应产物有 等多种物质。相关反应方程式为: 返回搜狐,查看更多 |
【本文地址】
今日新闻 |
推荐新闻 |