测元素价态, 你还只会用XPS吗? |
您所在的位置:网站首页 › 氮的一般价态 › 测元素价态, 你还只会用XPS吗? |
测元素价态, 你还只会用XPS吗?
|
测元素价态, 你还只会用XPS吗?
来源:本站
时间:2021-04-23 14:00:47
浏览:16002次
1 引言 价态又称化合价或原子价,简称价,是各种元素的一个原子或原子团、基(根)与其他原子相互化合的数目。 价态的概念最初来自于17世纪末开始的定比定律,普罗斯等人根据实验的结果,指出天然的和人造的盐基性碳酸铜的组成是完全相同的。从这一事实引导出这样的结论:两种或两种以上元素相化合物成某一化合物,其重量的比例是一定的,不能或增或减。 到19世纪中叶,德国人迈尔建议将“原子数”和“原子亲和力单位”用“原子价”代替。至此,原子价学说便正式建立了。原子价学说的建立提示了各种化学元素性质的一个极其重要的方面,阐明了各种元素相互化合物时在数量上遵循的规律。 价态有正负之分,给出电子的为正价,获得电子的为负价。正价一般是金属元素在化合物中显现的价态(例:Fe2O3中的Fe就显现出+3价)。也有些非金属元素的价态会显现出正价,一般是氢、碳、硅这些最外层电子数为满电荷数一半的元素。既可以失电子,也可以得电子。所以也可以显现出正价(例:CO2中的C就显现出+4价);负价一般是非金属元素在化合物中显现的价态(例:NaCl中的Cl就显现出-1价)。所有非金属元素中,只有氟元素(F)是永远显负价的,因为氟元素是所有非金属元素中,电负性最强的。 通常,以氢的化合价等于1作为标准。例如,水分子(H2O)中氧原子为-2价,氢原子为+1价。一般硫酸根为-2价,氢氧根为-1价。同一元素的不同价态在环境中的化学行为与生物效应有很大的不同。如重金属在微生物酶的氧化还原反应中,可形成几种不同的价态混合存在于环境或生物体中;如钴同时有+1、
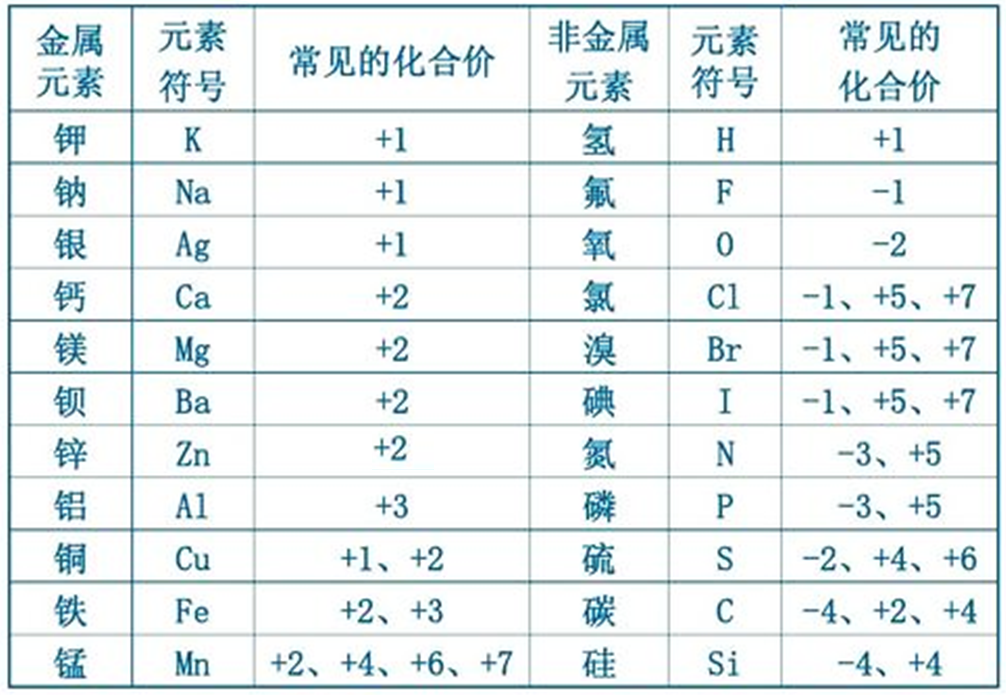
+2和+3价,铬有+2、+3和+6价,砷有+3和+5价等。不同价态的毒性差别很大;如+6价铬毒性最强,+3价铬次之,+2价铬和元素铬(单质)几乎无毒性;+3价砷的毒性很强,比+5价砷高0.8倍,这是由于不同价态物质的溶解度、与巯基的亲和力等物理化学性质有较大的不同所致。如表1,是一些常见元素的化合价。 表1 常见元素化合价
一般来说,元素的化合价分为三种情况: 1、最高化合价:失去最外电子层的所有电子,使自身达到相对稳定状态,例如高氯酸,它的氯元素失去了最外电子层的所有7个电子,达到最高价态+7价。 2、中间价态:得到或失去一定数目的电子,同样可以使自身达到相对稳定状态,例如一氧化碳,它的碳元素没有达到最高的+4价,也没有达到最低的-4价,而是处于一种中间价态。 3、最低化合价:得到一定数目的电子,使最外电子层的电子数达到饱和,使自身达到相对稳定状态,例如甲烷,它的碳元素得到了4个电子达到了最低价态-4价。
但凡涉及到化合物,那就避不开元素价态,目前,在金属加工、生物医学、材料工程、化学化工等各个领域均涉及到元素的价态。但是,关于价态的表征方法,包括价态的定性、定量,以及性质与性能的关联等还缺乏系统研究。在此,笔者结合自己的科研经验对元素价态的常见表征方法(图1)进行汇总,并给出一些典型实例,希望能给大家带来启发。
图1 常见元素价态表征技术
2 X射线光电子能谱(XPS)
X射线光电子能谱技术(XPS)是电子材料与元器件显微分析中的一种先进分析技术,而且是和俄歇电子能谱技术(AES)常常配合使用的分析技术。由于它可以比俄歇电子能谱技术更准确地测量原子的内层电子束缚能及其化学位移,所以它不但为化学 研究提供分子结构和原子价态方面的信息,还能为电子材料研究提供各种化合物的元素组成和含量、 化学状态、分子结构、化学键方面的信息。它在分析电子材料时,不但可提供总体方面的化学信息,甚至还能给出表面、微小区域和深度分布方面的信息,作用巨大。 XPS主要应用是测定电子的结合能来鉴定样品表面的化学性质及组成的分析,其特点在光电子来自表面10 nm以内,仅带出表面的化学信息,具有分析区域小、分析深度浅和不破坏样品的特点,因此广泛应用于金属、无机材料、催化剂、聚合物、涂层材料矿石等各种材料的研究,以及腐蚀、摩擦、润滑、粘接、催化、包覆、氧化等过程的研究,尤其是对于元素价态,XPS有着独特的优势。
图2 Pt18Ni26Fe15Co14Cu27纳米粒子的XPS结果 Hong dong Li等人[1]采用简单的低温油相策略,在大气压力下合成了均匀的超细(~3.4 nm) HEAs高熵合金Pt18Ni26Fe15Co14Cu27纳米颗粒。为了分析材料中元素的组成含量及价态信息,作者对Pt18Ni26Fe15Co14Cu27纳米粒子进行了X射线光电子能谱(XPS)测试,显示了Pt、Ni、Fe、Co和Cu
元素的存在(图2a),Pt、Ni、Fe、Co和Cu的原子比为21.2: 27.4: 15.2: 13.7: 22.5,进一步证明HEA材料被成功制备。图2b中Pt 4f7/2和Pt 4f5/2峰值分别位于71.3和74.7 eV处,表明铂主要以零价和少量+2价的形式存在。Ni 2p光谱显示Ni0(852.8 eV)和Ni2+(855.6 eV)共存,卫星峰位于861.6 eV,由于Ni的高化学活性,Ni0的含量低于Ni2+的含量。图2d中的Fe 2p光谱显示了711.6 eV和724.8 eV处的两个峰值,分别归因于Fe 2p3/2和Fe 2p1/2。此外,Co 2p峰可归因为Co 2p3/2(780.8 eV)和Co 2p1/2(797.0 eV)(图2e)。Cu 2p光谱(图2 f)也显示样品中存在Cu0(931.7 eV)和Cu2+(933.5 eV)峰。
3 紫外光电子能谱(UPS)
光电子能谱技术自二十世纪六十年代迅速发展起来,并成为研究固体材料表面态的最重要和有效的分析技术之一,主要包括前文提及的X射线光电子能谱(X-ray Photoelectron Spectroscopy,XPS)和紫外光电子能谱(Ultraviolet Photoelectron Spectroscopy,简称UPS)两个分支体系。UPS和XPS获得的信息既是类似的,也有不同之处,因此在分析化学、结构化学和表面研究以及材料研究等应用方面,它们是相互补充的。 UPS测量的基本原理与XPS相同,都是基于爱因斯坦光电定律。对于自由分子和原子,遵循EK=hn-EB-Φsp,其中,hn为入射光子能量(已知值),EK为光电过程中发射的光电子的动能(测量值),EB为内层或价层束缚电子的结合能(计算值),Φsp为谱仪的逸出功(已知值,通常在4 eV左右)。但是所用激发源的能量远远小于X光,因此,光激发电子仅来自于非常浅的样品表面(~10 Å),反映的是原子费米能级附近的电子即价层电子相互作用的信息,可以在高能量分辨率(10~20 meV)水平上探测价层
电子能级的亚结构和分子振动能级的精细结构,是研究材料价电子结构的有效方法之一。 西班牙佩斯瓦斯科大学Miguel博士和Stefano博士[2]为了更好地理解锂金属负极与其加工环境之间的相互作用机制,结合了X射线光电子能谱(XPS)、紫外光电子能谱(UPS)和密度泛函理 论(DFT)表征了锂金属在O2,CO2,N2氛围下的影响,为系统化和可重复性研究金属锂负极钝化策略奠定了基础。
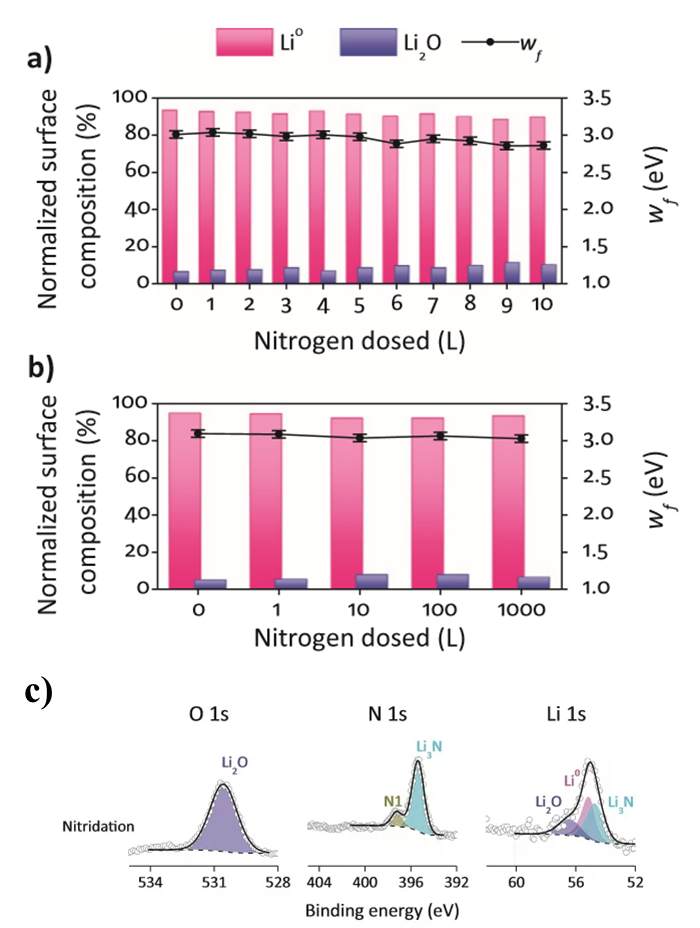
图3 暴露于不同剂量的N2的金属锂的归一化表面组成(左垂直轴)和功函数演变(右垂直轴):a)低剂量范围为0-10 L,b)中剂量范围为 10-1000L;c)氮离子注入后在锂表面上测得的N 1s,O 1s和Li 1s光电子峰。
以N2为例,作者观察到,对于任何研究的N2剂量,均未观察到金属锂与N2之间的相互作用。在暴露于1至1000 L的N2剂量期间,表面成分以及因此的功函数(图3 a-b)几乎保持恒定。 从图3 c中对由锂金属和氮化锂组成的表面中的Li 1s,O 1s和N 1s的分析,可以发现其中归一化表面成分为68.4% Li0、19.8% Li3N,8.1% Li2O和3.7%的少量杂质。Li3N的形成导致由UPS确定的Wf值从含Li3N的表面的Li0的3.01 eV变为2.49 eV。考虑到最终表面还包含8.1%的Li2O,人们可以认为Wf的下降是由于氧化锂的形成,也就是说金属锂从0价变成了+1价。但是,这样的表面Li2O量应导致Wf = 2.97 eV,远高于测得的2.49 eV。因此,氮化锂的形成也减少了功锂金属的功函数。
4 X射线吸收光谱(XAS)
XAS是X-ray Absorption Spectra的缩写,全称为X射线吸收光谱。X射线透过样品后,其强度发生衰减且其衰减程度与材料结构、组成有关。这种研究透射强度I与入射X射线强度Io之间关系的光谱,称为X射线吸收光谱;由于其透射光强与元素、原子质量有关,故可以用于元素的定性,甚至定量分析。XAS可以表征许多不同的材料,包括晶体或非晶态结构的液体和固体,从块状到纳米级甚至单个原子。 XAS包括两种:样品通过吸收X射线激发其核心电子跃迁到空轨道(XANES)或者跃迁到连续态与周围原子形成波的干射(EXAFS)。其中,EXAFS可知邻近原子结构,而XANES则可以告诉我们化学价态和电子结构。 当入射X射线能量低于元素s轨道(即s轨道)中电子的结合能时,电子不会被激发到最高未占据状态或真空状态。强X射线和电子
相互作用的缺乏导致了如图4a所示的平坦区域;然而,在过渡金属中,一些不利的跃迁,如1s到3d,将出现一个前边缘峰(图4a)。一旦X射线能量足够高,将核心电子激发到未占据状态(图4b), X射线被强吸收,导致光谱发生大跳跃,这被称为X射线吸收近边缘结构(XANES)(图4a)。该区域对被测元素的氧化态和电子结构敏感,可以用来检测元素价态。
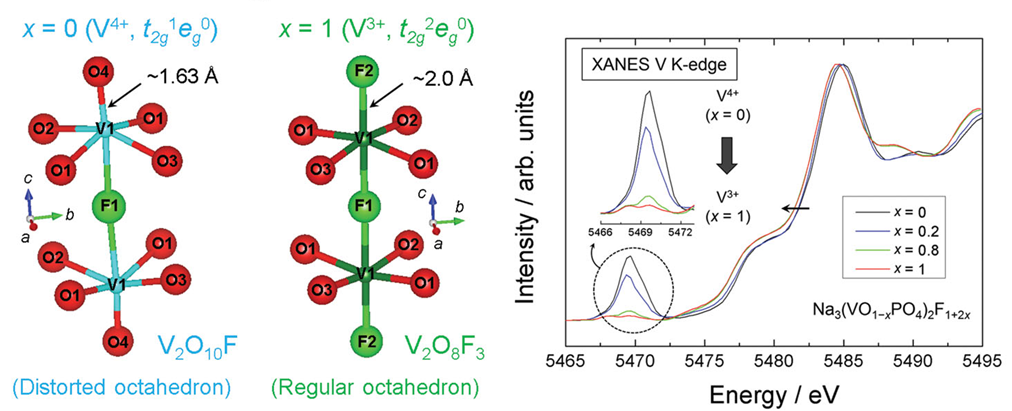
图4 (a)XAS的原理图,(b)X射线吸收过程和电子激发过程 Park等人[3]首次成功合成了一系列Na3(VO1−xPO4)2F1+2x (0≤ x ≤1)的化合物作为新型高性能钠离子电池阴极材料。测试表明,该阴极电极材料具有高能量密度和良好的循环寿命,在新能源储能领域应用潜力巨大。作者采用XANES对其中钒元素的价态进行了表征分析,如图5所示。 Na3(VO1−xPO4)2F1+2x (0≤ x ≤1)离子含量的变化改变了钒的氧化态,最终影响了电化学反应机理。通过对钒K边的X射线吸收近边结构(XANES)分析,钒的氧化态随着氟含量(x)不断变化。当x从0增加到1时,光谱的边缘向能量较低的方向移动,说明钒离子的还原。插图中显示的前边缘区域变化更明显,随着x的增加,前边缘峰逐渐变小,最终在x = 1处消失。 这一观察结果与XANES对含V4+和V3+离子的化合物的分析一致。畸变V4+八面体的化合物通常表现出一个大的前边缘峰,而那些V3+八面体的化合物由于较弱的1s到3d三维跃迁而表现出一个
微小的前边缘峰。随着x的增加,前缘峰逐渐消失,结合结构分析表明,V4+O5F八面体比V3+O4F2八面体变形更严重。
图5 x = 0时V2O10F八面体的几何形状,x = 1时V2O8F3八面体的几何形状,以及不同氟含量Na3(VO1−xPO4)2F1+2x样品的钒K边XANES光谱:黑色的x = 0.0,蓝色的x = 0.2,绿色的x = 0.8,红色的x = 1.0, 插图为前边缘区域的放大图
5 俄歇电子能谱(AES)
当一定能量的电子束轰击固体样品表面时,如果样品中原子的内层电子被击出,原子将处于高能的激发态,此时,外层电子将会跃迁到内层的电子空位,同时以两种方式释放能量:发射特征X射线;或引起另一外层电子电离,使其以特征能量射出固体样品表面,此即俄歇电子。通过检测俄歇电子的能量和强度,从而获得有关材料表面化学成分和结构的信息的方法,即为俄歇电子能谱(Auger Electron Spectrometry,简称AES)。 俄歇跃迁通常涉及三个能级,元素化学态变化时,能级状态有小的变化,从而导致这些俄歇电子峰与零价状态的峰相比有几个电子伏特的位移。因此,由俄歇电子峰的位置和形状可得知样品表面区域原子的化学环境或化学状态的信息。故而利用AES可以研究固体表面的能带结构、表面物理化学性质的变化(如表面吸附、脱附以及表面化学反应);常用于材料组分的确定、纯度的检测、材料尤其是薄膜材料的生长分析等。
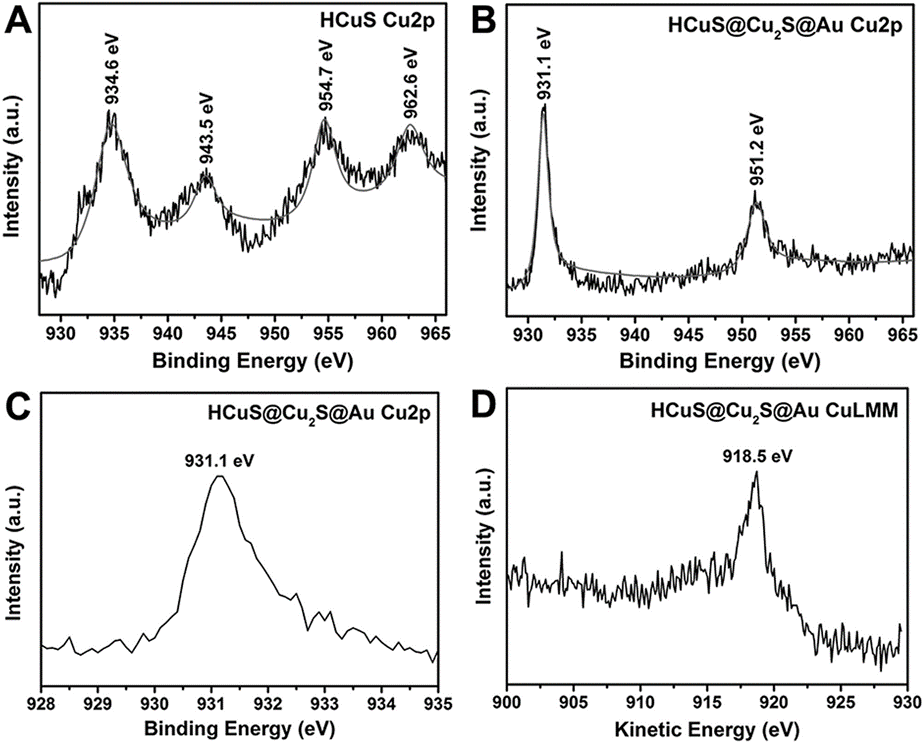
中国科学院长春应用化学研究所的林君研究员和程子泳研究员等人[4]设计并合成了中空结构的CuS@Cu2S@Au纳米壳/卫星纳米颗粒,用于改善癌症治疗领域的光热疗法和靶向治疗。 作者通过XRD分析确认了CuS和CuS@Au的形成。然而,制备出的CuS和CuS@Au在X射线光电子能谱(XPS)中的结果明显不同(图6)。CuS显示四个Cu 2p峰,包括在934.6 eV的Cu 2p3/2峰和在943.5 eV卫星峰,以及在954.7 eV的Cu 2p1/2峰和在962.6 eV的卫星峰。相比之下,CuS@Au的XPS谱显示了931.1 eV的Cu 2p3/2峰和951.2 eV的Cu 2p1/2峰(图6B),这对应于典型的Cu+或Cu0价态。 为此,作者通过计算修正的俄歇电子能谱来确定铜在CuS@Au上的价态。经Au纳米粒子修饰后,得到的Cu的光电子结合能(931.1 eV,图6C)和俄歇动能(918.5 eV,图6D)之和为1849.6 eV,清楚地表明Cu+在CuS@Au上的存在。
图6 HCuS (A)和HCuS@Cu2S@Au (B)中Cu 2p峰的XPS高分辨率 扫描;(C) HCuS@Cu2S@Au中Cu 2 p3/2的详细光谱; (D) HCuS@Cu2S@Au Cu LMM的俄歇电子谱(AES)
6 电子顺磁共振谱(EPR)
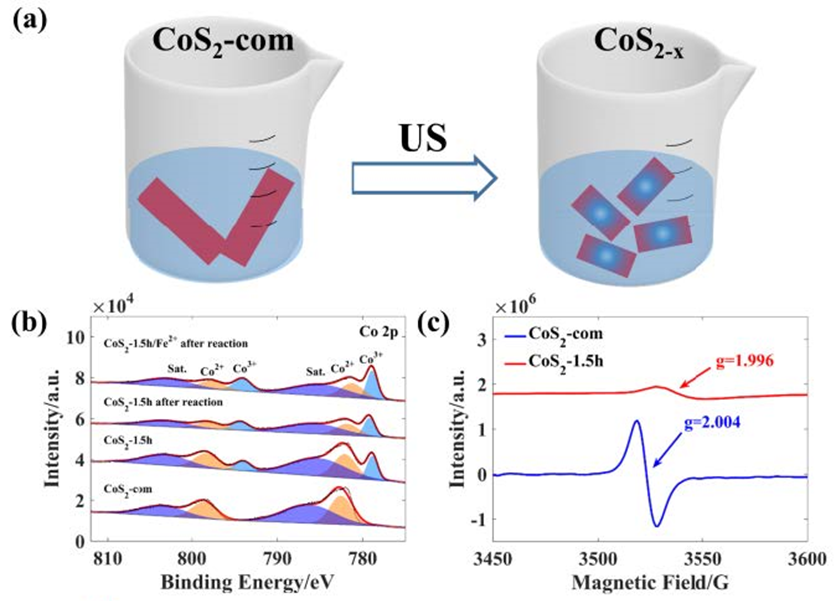
电子自旋共振波谱仪(EPR)是一项检测具有未成对电子样品的波谱方法。即使是在正在进行的化学和物理反应中,它也能获得有意义的物质结构信息和动态信息,且不影响这些反应。 当含有未成对电子的物质放在谐振腔内,然后置于外磁场中(由磁体和电源产生,磁场控制器控制)时,未成对电子会发生能级分裂(具有能级差),然后在磁场的垂直方向加上微波(有微波桥产生),当微波的能量与前面叙述的能级差相等时,有一部分低能级中的电子就会吸收微波能量跃迁到高能级,也就是说发生了电子顺磁共振。然后我们就检测被吸收的能量,并对检测的信号进行进一步的处理(由信号通道完成),最终有数据系统输出。 EPR很多应用于研究过渡金属配合物,因为过渡金属具有未充满的d壳层,其配合物常有未配对电子。用EPR可以研究配合物中过渡元素的价态、电子组态、配合物结构等。目前已在物理学、化学、生物学、生物化学、医学、环境科学、地质探矿等许多领域得到广泛应用。 邢明阳教授研究团队[5]通过对商品化的CoS2(CoS2-com)进行简单的超声处理,实现了对CoS2-x表面缺陷的调控,成功引入“双中心”缺陷活性位点。 作者利用电子顺磁共振(EPR)技术来检测CoS2-com和CoS2-x缺陷浓度和种类的变化(图7c)。CoS2-com在g=2.004处有一个很强的S的缺陷峰,其暴露Co3+活性位点并主要表现为“氧化”活性中心。有趣的是,超声处理后CoS2-x的EPR图谱在g=1.996处出现了一个新的Co的缺陷峰,该缺陷携带电子,主要表现为“还原”活性中心。
图7 (a) CoS2-x的超声制备方法;(b) CoS2-com与CoS2-1.5h (超声前后)以及CoS2-1.5h体系和CoS2-1.5h/Fe2+体系反应后的Co 2p XPS谱图;(c) 室温下CoS2-com和CoS2-x中缺陷的EPR谱图 同时,g=2.004处信号峰的消失,作者分析,可能是由于超声使得Co3+转化为Co4+(氧化活性中心)造成的(电荷守恒)。
7 其它检测方法
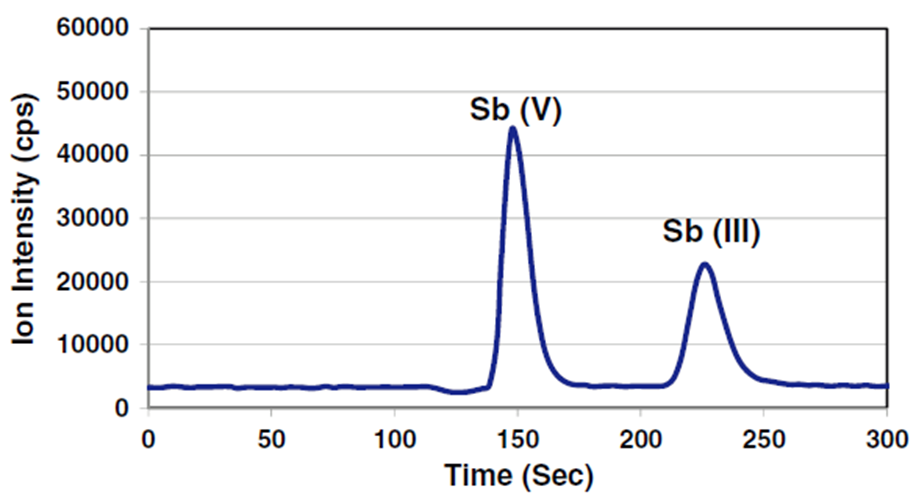
由于元素价态的重要性以及其在不同领域的测试差异,许多其他方法也可用于元素价态的测定。例如离子色谱与质谱联用可以测量许多特定元素的价态。 Pema等人[6]为了证明纳米零价铁(nZVI)具有优异的有机材料降解能力和无机吸附能力,利用合成的nZVI对Sb进行了吸附实验。作者利用IC-ICP-MS联用技术,测试了Sb的元素价态,如图8是典型的Sb3+和Sb5+离子色谱。Sb5+的保留时间(tr)为~154 s,Sb3+的保留时间为~226 s。Sb5+的峰高而锐利;而Sb3+的峰更短更宽。这可能是由于合成的Sb3+和EDTA阴离子复合物被阴离子交换柱吸附,同时也阻止了Sb3+氧化成Sb5+导致的。
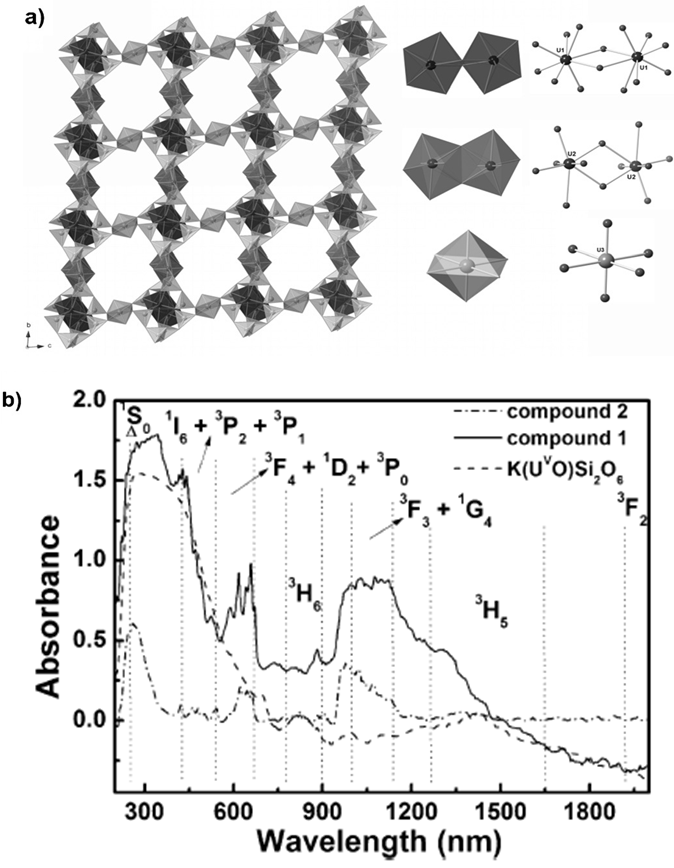
图8 Sb的离子色谱图 再比如说紫外-可见分光光度法(UV-vis),可以在190~800 nm波长范围内测定物质的吸光度。根据吸收光谱,可以确定最大吸收波长λmax和最小吸收波长λmin。物质的吸收光谱具有与其结构相关的特征性。因此,可以通过特定波长范围内样品的光谱与对照光谱或对照品光谱的比较,或通过确定最大吸收波长,或通过测量两个特定波长处的吸收比值而鉴别物质。 Chen等人[7]利用溶剂热法合成一种同时含有U4+、U5+和U6+的复杂而稀有的混合价膦酸铀化合物,作者分别利用XPS、EPR、FTIR和UV-vis等证实了U的三种价态,如图9b是制备得到化合物的UV-vis-NIR图。 将其与紫外基准K(U5+O)Si2O6比较,证实了化合物1中U5+的存在。从图中观察到化合物1在200 nm到400 nm之间有一个较宽的电荷转移峰,而在该范围内化合物2的电荷转移峰相对较窄。这种从O 2p轨道到U 6d/5f轨道的电荷转移特征,通常是由U4+引起的,这些特征在一些具有U5+离子的化合物的光谱中十分常见,如K(U5+O)Si2O6,以及由阳离子相互作用引起的铀酰键延长的U4+化合物等。
图9 (a)化合物1的多面体视图,(b)UV-vis-NIR光谱
8 总结
即使笔者提及到了大部分常见的元素价态检测方法,但实际应用时依然经常需要我们根据所需检测的材料特性进行调整。当然,也有一些特殊的方法笔者没有一一列出,比如说由于氟磷酸钒钠系列化合物的2个端点化合物的晶胞参数不同,用X 射线衍射精
修得到样品晶胞参数后可根据Vegard 定律计算2个端点化合物的比例,进而确定钒的表观价态;再比如说MnZn铁氧体中由于Mn和Fe极易变价(Fe:Fe2+、Fe3+,Mn:Mn2+、Mn3+),因此常用电位滴定法来定量分析其中Mn、Fe元素的价态及含量,此外还有中子活化法、电化学分析法等特定检测技术。 总之,笔者希望通过本文的归纳总结,能进一步激发相关科研人员更深层次的了解并掌握元素价态检测常见表征方法,为研究、开发出更先进便捷的定性、定量的元素表征手段提供借鉴,为科研开路添砖加瓦。
[1] Hongdong Li, Yi Han, Huan Zhao et al. Fast site-to-site electron transfer ofhigh-entropy alloy nanocatalyst driving redox electrocatalysis. Nat. Commun. DOI: org/10.1038/s41467-020-19277-9. [2] Miguel, Stefano et al. Work Function Evolution in Li Anode Processin. Adv. Energy Mater. DOI: 10.1002/aenm.202000520 [3] Young-Uk Park, Dong-Hwa Seo, Hyungsub Kim. A Family of High-Performance Cathode Materials for Na-ion Batteries, Na3(VO1−xPO4)2F1+2x (0≤ x ≤1): Combined First-Principles and Experimental Study. Adv. Funct. Mater. 2014, 24, 4603–4614. [4] Xiaoran Deng, Kai Li, Xuechao Cai et al. A Hollow-Structured CuS@Cu2S@Au Nanohybrid: Synergistically Enhanced Photothermal Efficiency and Photoswitchable Targeting Effect for Cancer Theranostics. Adv. Mater. DOI:10.1002/adma.201701266. [5] Jiahui Ji, Qingyun Yan, Pengcheng Yin. Tuning Redox Reactions via Defects on CoS2-x for Sustainable Degradation of Organic Pollutants. Angewandte Chemie International Edition. DOI:10.1002/anie.202013015. [6] Pema Dorjee, Dulasiri Amarasiriwardena, Baoshan Xing. Antimony adsorption by zero-valent iron nanoparticles (nZVI): Ion chromatography–inductively coupled plasma mass spectrometry (IC–ICP-MS) study. Microchemical Journal. DOI: org/10.1016/j.microc.2014.03.010. [7] Lanhua Chen, Tao Zheng, Songsong Bao, et al. A Mixed-Valent Uranium Phosphonate Framework Containing UIV, UV, and UVI, Chem. Eur. J. DOI: 10.1002/chem.201602863.
|
【本文地址】