通过磷酰胺酯桥合成氨酰核酸酯的前生源化学 |
您所在的位置:网站首页 › 氨酰trna合成酶活化氨基酸的氨基 › 通过磷酰胺酯桥合成氨酰核酸酯的前生源化学 |
通过磷酰胺酯桥合成氨酰核酸酯的前生源化学
|
通过磷酰胺酯桥合成氨酰核酸酯的前生源化学
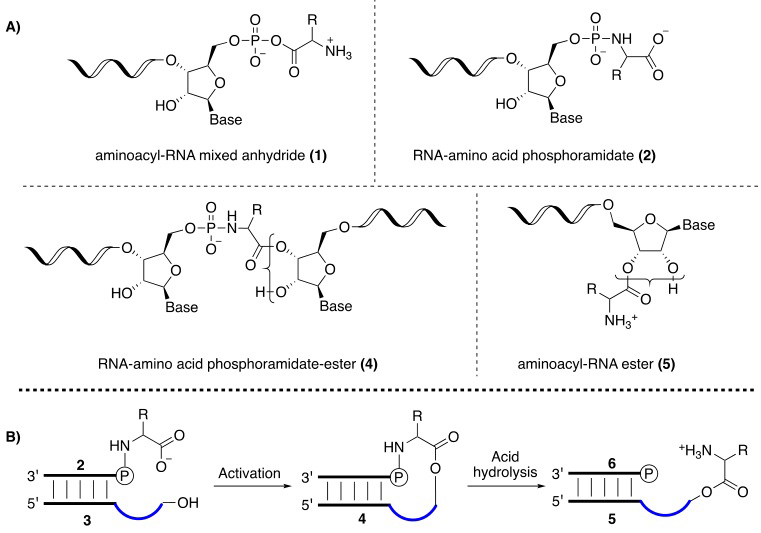
氨酰tRNA(aminoacyl-tRNA)是现代生物体内编码蛋白质翻译过程中的一个重要中间体。正确的氨基酸与之对应的tRNA之间形成的酯键是由氨酰tRNA合成酶(aminoacyl-tRNA synthetase)完成的。但是在早期地球环境中,氨酰tRNA是如何通过非酶化学合成出来的?最近,Journal of the American Chemical Society 在线发表的英国剑桥分子生物学实验室(MRC Laboratory of Molecular Biology)John Sutherland教授(点击查看介绍)课题组的研究论文,展示了一种全新的氨酰核酸酯的前生源合成过程。 由于氨基酸自身的特性导致氨基酸本身很难被活化直接生成氨酰核酸酯,而氨基保护的氨基酸的活化则相对容易,因此作者利用短链核酸上的5'端磷酸作为氨基酸氨基的保护基形成磷酰氨基酸(2)。而该短链核酸的互补核酸链(3)通过碱基配对作用(图1B)可以拉近其3'端的羟基与氨基酸羧基的距离。在活化试剂的作用下,氨基酸的羧基被活化并形成磷酰胺酯桥(4),将两个核酸链连接到一起形成氨基酸核酸杂化的茎环结构。之后该磷酰胺酯桥(4)在酸性条件下可以选择性的将磷酰胺键切断,形成最终的氨酰核酸酯(5)。
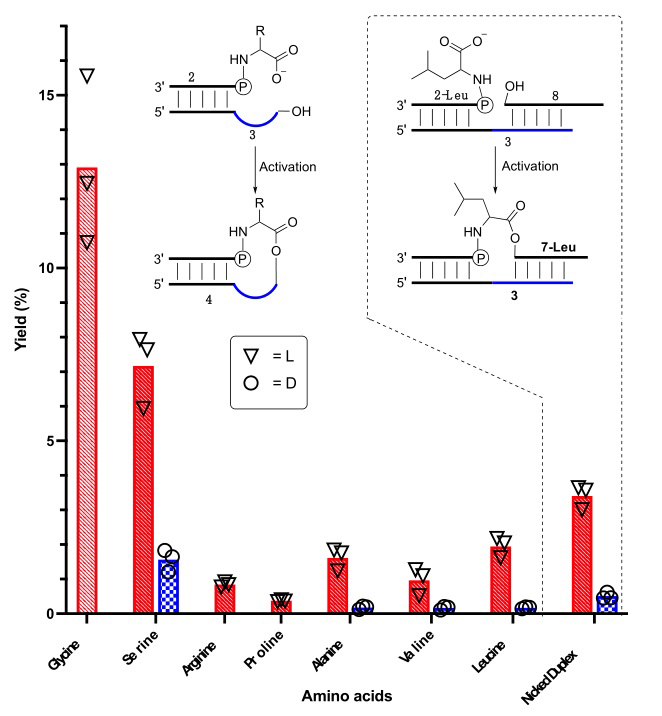
图1. A) 四种氨基酸-核酸杂化物的结构;B) 通过磷酰胺酯桥合成氨酰核酸酯的合成过程。 作者测试了不同的磷酰氨基酸形成磷酰胺酯桥(4)的能力。如图2所示,不同氨基酸形成磷酰胺酯桥(4)的能力有很大的区别。并且在所有测试的氨基酸中,L-构型的氨基酸均比D-构型的氨基酸更容易形成磷酰胺酯桥(4)。作者还测试了不同核酸结构对磷酰胺酯桥(4)形成的影响。利用亮氨酸作为保护的氨基酸,分别在环状缺口区(图2,Leucine)和双链缺口区(图2,Nicked Duplex)进行磷酰胺酯桥(4)或进行磷酰胺酯桥(7)的合成。虽然在双链缺口区磷酰胺酯桥(7-Leu)的产率(3.5%)略高于环状缺口区磷酰胺酯桥(4)的产率(2%)。但环状缺口区的磷酰胺酯桥(4)的L-构型与D-构型的比例(12:1)比在双链缺口区磷酰胺酯桥(7-Leu)的L-构型与D-构型的比例(7:1)略高。作者推测,这是由于环状缺口区的构型所导致的。作者还意外的发现,冷冻在-16 ℃冰箱里的样品形成磷酰胺酯桥(4)的产率很高。作者推测在该条件下,溶液形成了共晶相,使得磷酰胺酯桥(4)的产率有所提高。有趣的是,在这一条件下,L-构型的磷酰胺酯桥(4)的产率比D-构型的磷酰胺酯桥(4)的产率提高的多,因此导致L-构型与D-构型的磷酰胺酯桥(4)的比例最高可达48:1。
图2. 室温条件下不同氨基酸形成磷酰胺酯桥(4)的产率。 随后作者测试了不同氨基酸的磷酰胺酯桥(4)水解成氨酰核酸酯(5)的效率。在pH为3的甲酸缓冲溶液中,室温条件下,经过一夜的反应,所有氨基酸的磷酰胺酯桥(4)均全部水解,部分生成氨酰核酸酯(5)。其中除精氨酸和丝氨酸以外的磷酰胺酯桥(4)均以氨酰核酸酯(5)为主要产物。精氨酸和丝氨酸的水解产率则比较差,分别为24%和39%。精氨酸是由于侧链上的氨基使其磷酰胺酯桥(4)的稳定性较差,容易水解成为磷酰精氨酸(2)与核酸(3)。而丝氨酸由于在反应过程中得到了其他未知的化合物,而这些化合物在碱性条件下也会水解,导致其计算产率变低。 这一工作展示了一条全新、高效的前生源条件下氨酰核酸酯的合成路线。这一合成路线对于L-构型的氨基酸有着极高的选择性。当环状缺口区的核酸序列固定,导致不同氨基酸的产率有所不同。因此作者结合之前的工作(J. Am. Chem. Soc., 2021, 11836-11842),推测该环状缺口区的核酸序列与氨基酸种类或许有某种关联。另外,在酸性条件下不仅可以将磷酰胺酯桥(4)水解成氨酰核酸酯(5),还可以将双链核酸打开(Biochemistry, 2018, 6382-6386),使得氨酰核酸酯(5)可以在溶液中重新组合,在其他核酸的帮助下形成多肽(Nucleic Acids Res., 2022, gkac052)。因此,该工作为揭示如何在非酶条件下进行编码蛋白质合成提供了重要的线索。 该工作由John Sutherland教授课题组的Samuel J. Roberts博士与刘紫微博士作为共同第一作者合作完成。 原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):
Potentially Prebiotic Synthesis of Aminoacyl-RNA via a Bridging Phosphoramidate-Ester Intermediate Samuel J. Roberts, Ziwei Liu, and John D. Sutherland* J. Am. Chem. Soc., 2022, DOI: 10.1021/jacs.2c00772 导师介绍 John Sutherland https://www.x-mol.com/university/faculty/284061 如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载! 点击分享 收藏 取消收藏 评论: 0 |
【本文地址】
今日新闻 |
推荐新闻 |