【科技前沿】陈晓伟团队报道冠状病毒的代谢弱点及潜在的广谱抗病毒药物 |
您所在的位置:网站首页 › 普洛莱西尔 › 【科技前沿】陈晓伟团队报道冠状病毒的代谢弱点及潜在的广谱抗病毒药物 |
【科技前沿】陈晓伟团队报道冠状病毒的代谢弱点及潜在的广谱抗病毒药物
|
人类和病毒的拉锯亘古不变。病毒借助自身的不断变异,来适应环境、逃逸免疫、乃至对抗药物。因此,仅仅针对病毒自身蛋白来开发药物,不但有“计划赶不上变化”的可能,还存在诱导病毒进化、催生抗药毒株的风险。在肆虐全球的新冠疫情中,疫苗及治疗药物的成功研发凸显了科学的力量;但由于当前的疫苗及药物均针对病毒本身进行设计,对疫苗产生免疫逃逸、对药物耐受的病毒突变株已出现【1, 2】。相对病毒的高突变性,其依赖的宿主细胞通路则相当稳定、不易突变,故可供开发广谱的抗病毒药物。然而,靶向宿主蛋白的抗病毒药物,必须兼顾有效性和安全性、实现“杀敌而不伤己”。因此,发现冠状病毒的生命弱点、暨安全的宿主靶点,方可研发广谱抗病毒药物、以期防治未知突变乃至全新病毒。 磷脂双层膜是生命的根本特征,在微观层面界定了“非我”和“自我”;磷脂双层膜生成的最终步骤是磷脂的高效跨膜翻转,一直是细胞生物学的未解难题(Alberts et.al. Mol. Biol. of the Cell,图1)。而病毒作为非自主的生命形式,其对生物膜的需求必须依靠宿主细胞的供给;冠状病毒的基因组为RNA,则更需要大量生物膜供其构建独特的复制小体,来严密的保护病毒复制中生成的大量RNA。2021年,多个课题组通过遗传筛选,分别报道了细胞中TMEM41B的缺失可广谱的抑制包括新冠病毒在内的一系列RNA病毒的复制,进而推测该蛋白或可作为抗病毒药物的靶点【3, 4】。然而,北京大学陈晓伟团队基于血脂分泌这一独特过程,揭示了TMEM41B为领域长期探寻的内质网磷脂翻转酶(Bioart链接:陈晓伟、杨洪远等发现TMEM41B和VMP1是促磷脂翻转酶),并发现其缺失可引发“脂层不平衡反应”,导致剧烈的组织损伤、代谢疾病、乃至机体死亡【5】。因此,TMEM41B自身难以作为药物靶点;如何安全的利用其缺失产生的高效抗病毒活性,代表了宿主靶向抗病毒药物开发的一个普遍难题。 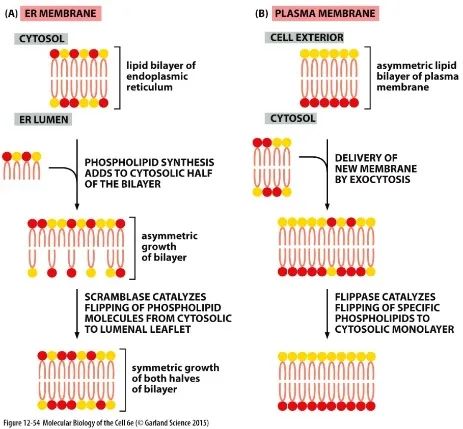 图1. 生物膜在内质网发生的最终步骤需要高效磷脂翻转,由Scramblase而非Flippase介导(取自Alberts et. al. 《细胞的分子生物学》) 2022年12月10日,北京大学未来技术学院陈晓伟团队在bioRxiv预印本杂志发表文章A Host-Harbored Metabolic Susceptibility of Coronavirus Enables Broad-Spectrum Targeting,揭示了由两个核心宿主因子SREBP1和TMEM41B组成的“脂-膜衔接”通路;从而设计靶向性筛选得到病毒特异必需 (viral-specific-essential, VSE)基因,并暴露出冠状病毒生命周期的代谢弱点;最终发现人群中广泛使用的心血管药物普萘洛尔 (Propranolol) 可阻断SREBP1-TMEM41B通路,故可在实验体系中广谱的抑制包括非典、新冠在内的冠状病毒复制子的扩增及寨卡、登革热等黄病毒。 陈晓伟团队从探寻TMEM41B的调节机制着手,意外的发现了脂代谢的核心转录因子SREBP1可直接且特异的上调TMEM41B,进一步功能实验发现TMEM41B可翻转由SREBP1诱发合成的大量磷脂、从而形成新的生物膜,从而构建了一个将磷脂代谢(metabolism) 和生物膜组装 (manufacture) 高效偶联的“脂-膜衔接”通路(图2,左)。 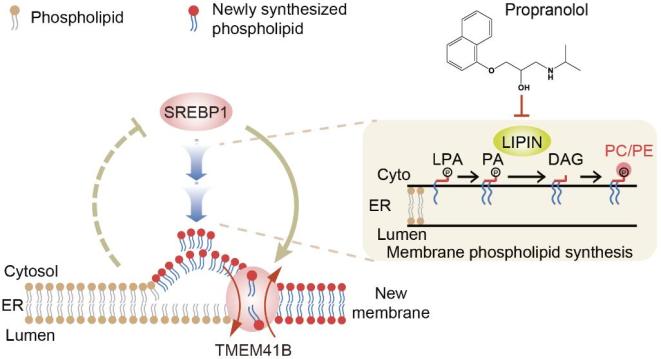 图2. 核心宿主因子SREBP1和TMEM41B构建的“脂-膜衔接”通路,高效偶联了磷脂合成和生物膜组装。 值得一提的是:SREBP1及TMEM41B均为冠状病毒的核心宿主因子(4, 6),提示了病毒或通过上述“脂-膜衔接”的宿主通路来最大限度的获取生物膜。在利用化学生物学的技术验证了上述猜想后,作者进而推测:通过限制涌向TMEM41B的磷脂代谢流,或可针对冠状病毒对生物膜的嗜求,实现一个“断薪救火”、但无伤宿主的抗病毒策略。因此,作者设计了靶向筛选,针对SREBP1-TMEM41B通路中囊括的磷脂合成基因中,寻找潜在的病毒特异必需 (Viral-specific-essential, VSE) 的宿主因子。上述筛选发现了SREBP1-TMEM41B通路的代谢酶中包含了数个VSE基因,进一步提示了该通路代表了冠状病毒的代谢弱点;其中,磷脂酸去磷酸酶Lipin1则脱颖而出:其失活可有效抑制冠状病毒复制、但Lipin缺失在从酵母到人类都可被容忍,且已知其活性可被人群中广泛使用的药物普萘洛尔所抑制,故可满足“杀敌而不伤己”的抗病毒需求(图2,右)。 作者进而发现普萘洛尔在细胞中可抑制冠状病毒诱导的磷脂合成、并且在安全剂量内有效的抑制病毒复制。进一步的机制解析显示:普萘洛尔能够清除冠状病毒在细胞中诱导出的复制小体、将内质网维持在正常形态(图3)。因复制小体为多种RNA病毒所必须,故而作者进一步发现:除了非典、新冠等冠状病毒的复制子之外,普萘洛尔在细胞中还可广谱的抑制登革、寨卡等黄病毒的复制。作者进一步锁定了普萘洛尔的手性异构体 (R-Propranolol),可独立于其心血管功能而发挥代谢抑制介导的抗病毒效用。值得注意的是,普萘洛尔的发明在1988年被授予了诺贝尔奖,其作为心血管药物在人群中使用已逾半个世纪;因此,作者在UK Biobank的真实世界数据中,发现普萘洛尔的使用可能对黄热病及登革热具有潜在的防护作用。最后,作者利用小鼠冠状病毒 (MHV) 感染的模型,发现普萘洛尔可有效减少99.7%的冠状病毒载量;当给予等同人体日常用量用于预防用途时,小鼠体内MHV病毒量被降低近万倍、并实现了多器官保护。 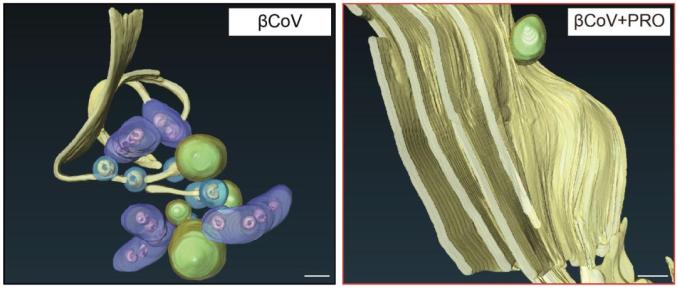 图3. 普萘洛尔(PRO)代谢性的阻断宿主“脂-膜衔接”通路、破坏冠状病毒复制小体 【研究局限】该预印本中的研究从鉴定内质网磷脂翻转酶TMEM41B出发,寻找到SREBP1-TMEM41B这一“脂-膜衔接”的调节通路,进而发现限制上述通路的代谢流量可作为靶向宿主的广谱抗病毒策略,为研发靶向“脂-膜衔接”通路及Lipin1的药物提供了理论基础。在上述机制研究的基础上,作者提供了普萘洛尔可能被赋新为广谱抗病毒、乃至预防性药物的前期证据,但目前尚未能以新冠活病毒开展研究、抑或有临床数据支持。在UK Biobank等大规模真实世界研究中、新冠相关的数据正在被深入分析;如本研究中小分子药物的结果能在人群中得到进一步验证,或可为抗击未来疫情提供药物及技术的储备。 陈晓伟团队方欢博士及博士生王镛伦、刘璐、程昆仑为该研究的共同第一作者,钱朝晖(医科院病原所)及陈晓伟为通讯作者;清华大学的谭旭团队、华中科技大学的王超龙团队也发挥了重要作用。在研究及成文过程中也得到了Randy Schekman (UC Berkeley), Jun Liu (Mayo Clinic), David Ginsburg (U of Michigan) 的建议。 原文链接: https://www.biorxiv.org/content/10.1101/2022.12.07.519404v1 参考文献 1. S. Gandhi et al., De novo emergence of a remdesivir resistance mutation during treatment of persistent SARS-CoV-2 infection in an immunocompromised patient: a case report. Nat Commun 13, 1547 (2022). 2. D. Planas et al., Considerable escape of SARS-CoV-2 Omicron to antibody neutralization. Nature 602, 671-675 (2022). 3. H. H. Hoffmann et al., TMEM41B Is a Pan-flavivirus Host Factor. Cell 184, 133-148.e120 (2021). 4. W. M. Schneider et al., Genome-Scale Identification of SARS-CoV-2 and Pan-coronavirus Host Factor Networks. Cell 184, 120-132.e114 (2021). 5. D. Huang et al., TMEM41B acts as an ER scramblase required for lipoprotein biogenesis and lipid homeostasis. Cell Metab 33, 1655-1670 e1658 (2021). 6. S. Yuan et al., SREBP-dependent lipidomic reprogramming as a broad-spectrum antiviral target. Nat Commun 10, 120 (2019). 本文转载自公众号“BioArtMED” 中国生物物理学会官方订阅号,为BSC会员及生物物理领域专业人士服务。 投稿及授权请联系:[email protected]。 原标题:《【科技前沿】陈晓伟团队报道冠状病毒的代谢弱点及潜在的广谱抗病毒药物》 阅读原文 |
【本文地址】
今日新闻 |
推荐新闻 |