临床研发信息检索 |
您所在的位置:网站首页 › 临床数据查询app › 临床研发信息检索 |
临床研发信息检索
|
找到对的参考,持续的自学提升对任何一个职场新人来说都是基本且重要的。本文将介绍在临床研发工作中,如何在一些公开且免费的渠道上,找到有价值的学习资料。首先从FDA官网的信息检索说起。 浏览器搜索“FDA”或直接打开链接www.fda.gov,进入FDA官网。
官网中,找到“Drugs”并点击,如果是查找器械、疫苗等的产品信息则点击相对应入口。
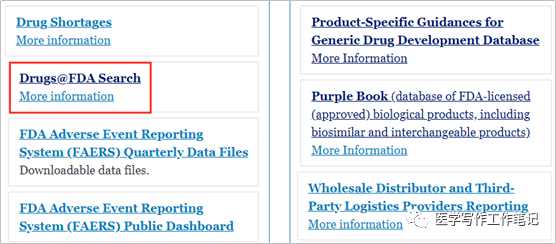
进入“Drugs”后,以下两个红框圈出的,是药物研发经常会用到的入口。
(一)
先是“Drug Approvals and Databases”。里面的“Drugs@FDA”,可能是药物研发尤其是临床研发最常用到的一个数据库。其他的例如“橙皮书”“紫皮书”“非活性成份数据库”,也是CMC研发经常使用的。
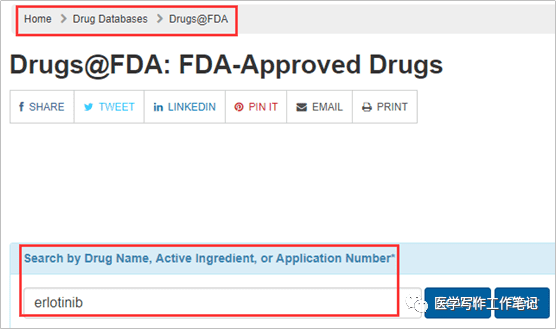
进入“Drugs@FDA Search”,在检索框里输入你想查询的药物通用名、或商品名、或活性成份,可以检索到对应的原研药品或仿制药品、复方药品的FDA批准信息。这里以“erlotinib”为例。
可以看到有多个产品出来。 最下面这个Tarceva是原研公司OSI pharms开发的erlotinib,Tarceva是它的商品名,也展示了它的NDA号。这一产品Roche也参与了共同开发,所以在中国会查到进口的厄洛替尼片(特罗凯)是由罗氏生产的。
上面的9个盐酸厄洛替尼,则都是仿制药,带有ANDA号,仿制的厂家有我们熟知的Mylan、Teva、印度太阳制药等。仿制药品点进去看到的信息比较简单,有获批的时间、规格。
要看盐酸厄洛替尼片的详细获批信息,还是要点击原研产品。 在获批历史中,可以看到初始获批上市的时间,经历了优先审评,初始获批的药品说明书和“Review”,以及在补充申请记录里可以找到当前最新的说明书、以及既往版本的说明书。
点击初始获批时的“Review”。可以看到FDA公开的审评报告。临床研发常查阅的是“Medical Review”、“Statistical Review”、“Clinical PharmacologyBiopharmaceutics Review”,点击进去都可以查看并下载PDF文件。
“MedicalReview”通常会讲解该产品支持上市批准的关键性临床试验及支持性试验的开展情况,主要的试验设计和结果结论,以及FDA审评员的评论,这都主要围绕着疗效和安全性试验。厄洛替尼的“Medical Review”还把它的关键Ⅲ期试验方案作为了附件,是个额外的收获。
“StatisticalReview”可以作为“Medical Review”的补充,主要围绕着关键性试验的临床数据从统计角度所作的审评。
“Clinical PharmacologyBiopharmaceutics Review”则是关注早期临床的数据,包括早期的剂量递增、剂量发现试验、特殊人群PK研究、生物利用度或生物等效性试验等的临床药理学发现。
(二)
药品信息查询了解到这,再回到前面提到的进入“Drugs”后,还有一处查询Guidance的入口。
如下图右侧红框,点击进去可查询FDA发布的指导原则、指南等规范性文件。
先看“Newly Added GuidanceDocuments”,可以查看FDA近期发布的指南,比如这篇新发布的双特异性抗体研发指南。
再看“Product-SpecificRecommendations for Generic Drug Development”,可译为仿制药开发的特定产品指南,可以检索到某一具体产品、FDA对其的仿制药开发指南,多是对生物等效性研究的指导建议,对于一些特殊剂型如喷雾剂,也有对CMC开发的建议。
这次以“empagliflozin”为例,可以通过该通用名的首字母“E”来查找、也可以输入“empagliflozin”来检索,当然直接输入的检索效率更高。
点进去,小小一份指南,建议了BE研究的设计、推荐的检测物质,这是做仿制药临床开发必查的一份文件。
最后看的是“Guidances (Drugs)”,放到最后,是因为这里的资料就不是那么好找了,而终极原因还是因为FDA的guidance太多太多。下图中的两处入口是一样的,点击进去进行具体的检索。
比如,我想查找FDA对于ANDA的申报资料要求,输入“ANDA”,显示110条结果,找起来还是太费劲了。如果我们知道或者猜测出这份指南名称里的更多词汇,如“ANDA content”,显示只有5条结果,找起来就方便一些。
另外一个小技巧,就是在检索时可以选择一下guidance的主题分类,缩小查找范围。
(三)
若是想了解FDA对于各种申报类型(IND、NDA、BLA、ANDA)的申报要求,除了上述的检索方法,还可以从以下入口进行检索。
回到前面提到的进入“Drugs”后,有一处查询“Drug Development and ReviewProcess”的入口,如下图红框。
找到“How Drugs AreDeveloped and Approved”并进入。
可以看到FDA整理了不同申报类型下,申报的流程和要求。根据FDA的指引,可以比较系统的查到到围绕着这一申报类型的指南文件。
|
【本文地址】
今日新闻 |
推荐新闻 |