有机人名反应 |
您所在的位置:网站首页 › tollens反应原理 › 有机人名反应 |
有机人名反应
|
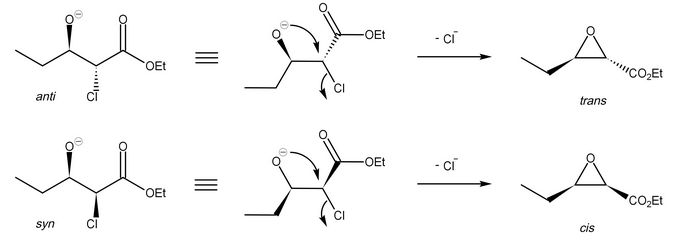
氧上的负电荷以分子内SN2机理进攻α-碳,卤离子离去,最终生成环氧丙酸酯类化合物:
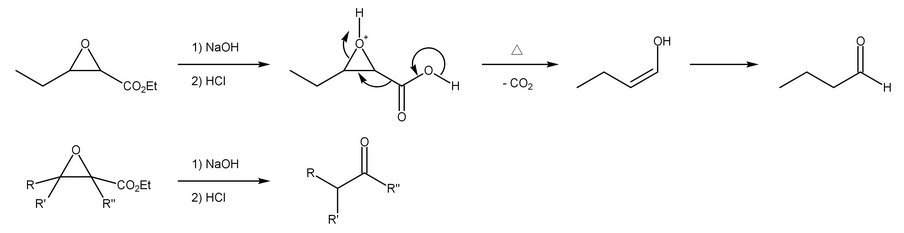
通常,环氧化物形成的顺式:反式比例在1:1和1:2之间。 在过去,Darzens反应主要用于合成醛和酮,作为同系反应,不考虑环氧化物形成中的立体控制。 对于该序列,皂化α,β-环氧酯,然后脱羧,得到取代的羰基化合物:
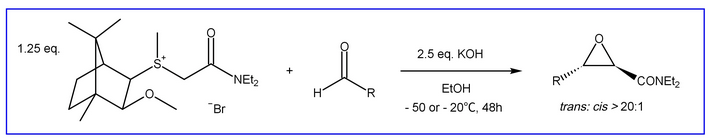
Darzens方法也可用于α-卤代羰基化合物或类似化合物,这些化合物可以进行脱质子化并带有吸电子基团。此外,反应可以用重氮乙酸酯进行,其中N2是离开基,或硫叶立德与SR2作为离开基(见Corey Chaykovsky)。 如Aggarwal所述,在以下特定的取代模式中,反应的结果取决于加成,旋转和闭环过渡态的能量。 尽管给出了非对映选择性的解释,但樟脑衍生的锍基团诱导的对映选择性尚未得到充分理解:
V. K. Aggarwal, G. Hynd, W. Picoul, J.-L. Vasse, J. Am. Chem. Soc., 2006, 128, 2105-2114. DOI Arai提出了另一个非对映选择性和对映选择性转换的概念:
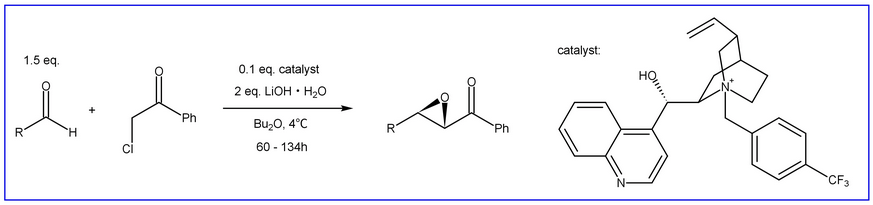
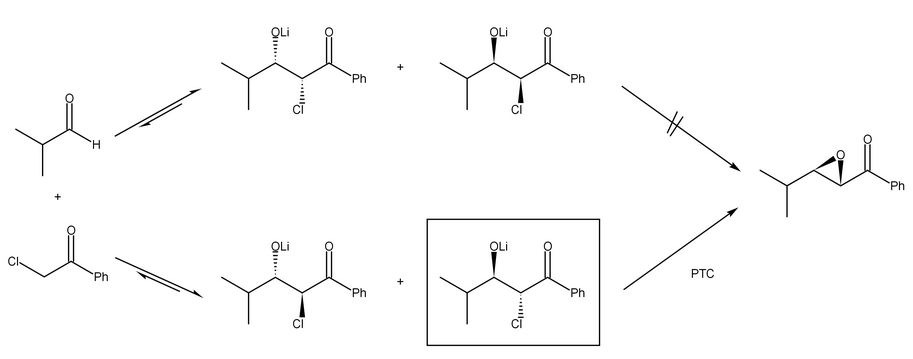
S. Arai, Y. Shirai, T. Ishida, T. Shioiri, Tetrahedron, 1999, 55, 6375-6386. 在该系统中,手性相转移催化剂(PTC)能够选择性识别一种醛缩醛。通过逆向羟醛加成,顺式和 反式醛醇酸酯之间达到平衡,并且形成稳定的螯合锂盐会阻止后续的非催化反应生成环氧化物产物:
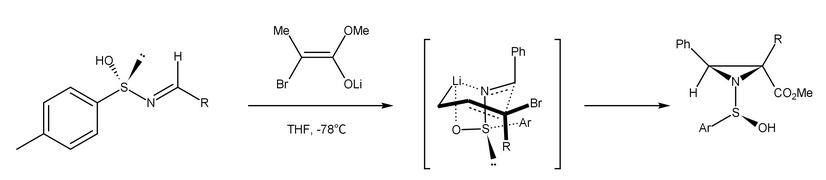
以下aza-Darzens反应中,预先形成的α-溴烯酸锂与亚磺胺反应生成氮丙啶,其六元过渡态具有很高的非对映选择性:
F. A. Davies, H. Liu, P. Zhou, T. Fang, G. V. Reddy, Y. Zhang, J. Org. Chem., 1999, 64, 7559-7567. DOI 对映选择性方法的发展仍然具有挑战性。原则上,也可以在Darzens反应中测试用于立体选择性羟醛加成的任何方法,因为第一步是羟醛加成。
|
【本文地址】
 返回搜狐,查看更多
返回搜狐,查看更多