2.1:原子、同位素、离子和分子 |
您所在的位置:网站首页 › h的同位素区别在哪里 › 2.1:原子、同位素、离子和分子 |
2.1:原子、同位素、离子和分子
|
化学反应和分子
根据八位组法则,当所有元素的最外壳充满电子时,所有元素的稳定性最高。 这是因为原子处于这种构型在能量上是有利的,并且可以使它们保持稳定。 但是,由于并非所有元素都有足够的电子来填充其最外层的外壳,因此原子与其他原子形成化学键,从而获得获得稳定电子构型所需的电子。 当两个或多个原子相互化学结合时,由此产生的化学结构就是分子。 熟悉的水分子 H 2 O 由两个氢原子和一个氧原子组成;它们结合在一起形成水,如图所示\(\PageIndex{8}\)。 原子可以通过捐赠、接受或共享电子来填充其外壳来形成分子。 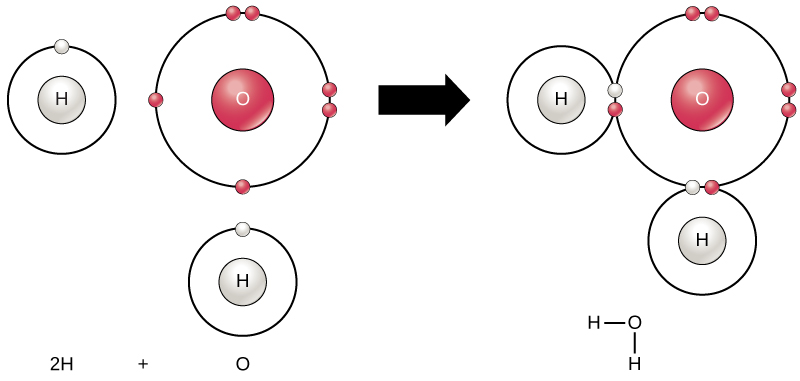 图\(\PageIndex{8}\):两个或多个原子可能相互结合形成分子。 当两个氢和一个氧气通过共价键共享电子时,就会形成一个水分子。
图\(\PageIndex{8}\):两个或多个原子可能相互结合形成分子。 当两个氢和一个氧气通过共价键共享电子时,就会形成一个水分子。
当两个或多个原子结合在一起形成分子或当键合的原子分解时,就会发生@@ 化学反应。 化学反应开始时使用的物质称为反应物(通常位于化学方程式的左侧),反应结束时发现的物质被称为产物(通常位于化学方程的右侧)。 通常在反应物和产物之间画一个箭头来表示化学反应的方向;这个方向并不总是 “单行道”。 要生成如上所示的水分子,化学方程为: \[\ce{2H + O \rightarrow H_2O} \nonumber\] 简单化学反应的一个例子是过氧化氢分子的分解,每个过氧化氢分子由两个与两个氧原子(H 2 O 2)结合的氢原子组成。 反应物过氧化氢被分解成水,其中包含一个与两个氢原子(H 2 O)结合的氧原子,以及由两个键合的氧原子(O 2)组成的氧。 在以下方程中,该反应包括两个过氧化氢分子和两个水分子。 这是一个平衡化学方程的示例,其中方程两侧每个元素的原子数是相同的。 根据物质守恒定律,化学反应前后的原子数应相等,这样在正常情况下就不会产生或破坏任何原子。 \[\ce{2H_2O_2\: (hydrogen\: peroxide) \rightarrow 2H_2O\: (water) + O_2\: (oxygen)} \nonumber\] 尽管这种反应的所有反应物和产物都是分子(每个原子都与至少一个其他原子结合),但在这种反应中,只有过氧化氢和水是化合物的代表:它们含有不止一种元素的原子。 另一方面,如图\(\PageIndex{9}\)所示,分子氧由两个双键合的氧原子组成,不被归类为化合物,而是单核分子。 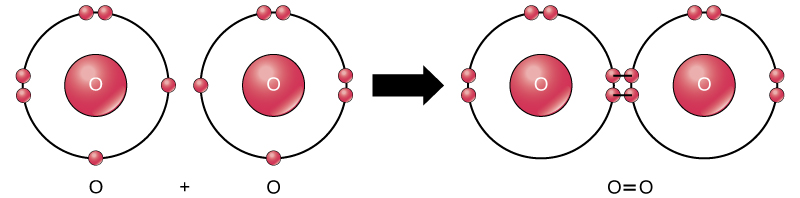 图\(\PageIndex{9}\):O 2 分子中的氧原子通过双键连接。
图\(\PageIndex{9}\):O 2 分子中的氧原子通过双键连接。
一些化学反应,例如上面所示的化学反应,可以朝一个方向进行,直到反应物全部用完。 描述这些反应的方程包含一个单向箭头,并且是不可逆的。 可逆反应是指可以朝任一方向发展的反应。 在可逆反应中,反应物被转化为产物,但是当产物的浓度超过一定阈值(特定反应的特征)时,其中一些产物将被转化为反应物;此时,产物和反应物的名称被颠倒了。 这种来回一直持续到反应物和产物之间出现一定的相对平衡,这种状态称为平衡。 这些可逆反应的情况通常用化学方程表示,双头箭头指向反应物和产物。 例如,在人体血液中,过量的氢离子(H +)与碳酸氢根离子(HCO 3 -)结合,形成与碳酸(H 2 CO 3)的平衡状态。 如果将碳酸添加到该系统中,其中一些碳酸将被转化为碳酸氢盐和氢离子。 \[\ce{HCO^{-}_3 + H^+ \leftrightarrow H_2CO_3} \nonumber\] 但是,在生物反应中,很少能实现平衡,因为反应物或产物或两者的浓度在不断变化,通常一种反应的产物是另一种反应的反应物。 回到血液中氢离子过多的例子,碳酸的形成将是反应的主要方向。 但是,碳酸也可以作为二氧化碳气体(通过呼气)离开人体,而不是转化回碳酸氢根离子,从而根据称为质量作用定律的化学定律将反应推向右边。 这些反应对于维持我们血液的稳态很重要。 \[\ce{HCO_3^- + H^+ \leftrightarrow H_2CO_3 \leftrightarrow CO_2 + H_2O} \nonumber\] |
【本文地址】