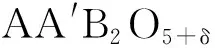钙钛矿氧化物ABO3的结构调控与电催化性能研究进展 |
您所在的位置:网站首页 › 钙钛矿的应用前景和主要困难有哪些方面 › 钙钛矿氧化物ABO3的结构调控与电催化性能研究进展 |
钙钛矿氧化物ABO3的结构调控与电催化性能研究进展
|
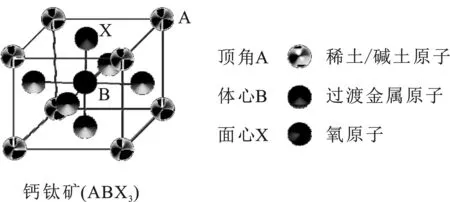
柳欢,高薪羽,白杰,李春萍 (1.内蒙古工业大学 化工学院,内蒙古 呼和浩特 010051;2.内蒙古工业催化重点实验室,内蒙古 呼和浩特 010051) 现如今化石燃料的消耗与能源需求的增加及环境问题受到人们的日益关注[1-4]。能源转换技术包括燃料电池、金属空气电池等都依赖于析氧反应(OER)和氧还原反应(ORR),而电催化剂是这些反应的关键[2]。然而贵金属(Pt、Ru等)催化剂因经济问题,较高的过电位及缓慢的动力学限制了其实际应用[5-6]。因此寻求高效非贵金属电催化剂是十分必要的。 近年来非贵金属钙钛矿材料在电催化、金属空气电池等领域得到广泛研究,例如La0.5Sr0.5CoO2.91和SrCoO3等均被报道用于电解水或金属空气电池[7]。本文综述了钙钛矿型氧化物的结构与电催化性质,从反应机理出发,总结了钙钛矿氧化物近年来在电催化领域等方面的研究进展,包括掺杂、缺陷等方法对电催化活性的影响,并展望了它的前景和发展趋势。 1 钙钛矿氧化物的结构与电催化性能1.1 钙钛矿氧化物的结构钙钛矿氧化物是对与CaTiO3具有相似结构氧化物的统称,其通式为ABO3,理想钙钛矿的晶体结构一般为立方相Pm3m空间群,是由B为中心与6个O离子构成的八面体规则交替排列而成,A离子位于氧八面体空间的空隙位置,其中A位可以是碱金属、碱土金属或稀土金属元素,B位是过渡金属元素(图1)[8]。A、B位的离子种类繁多具有可调变性,其组分和价态可进行灵活设计调控,使得钙钛矿结构在电催化领域表现出优异的本征催化活性与结构稳定性。但不能随意替代钙钛矿A位或B位原子,钙钛矿结构中的所有离子必须满足结构容限因子t:
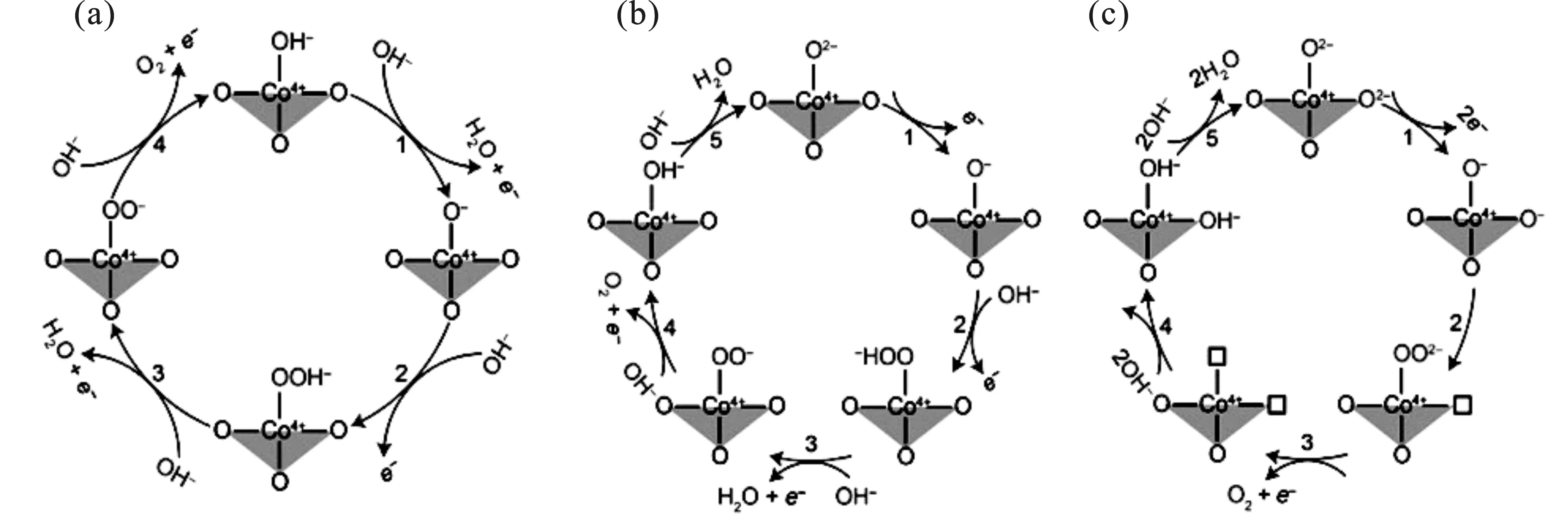
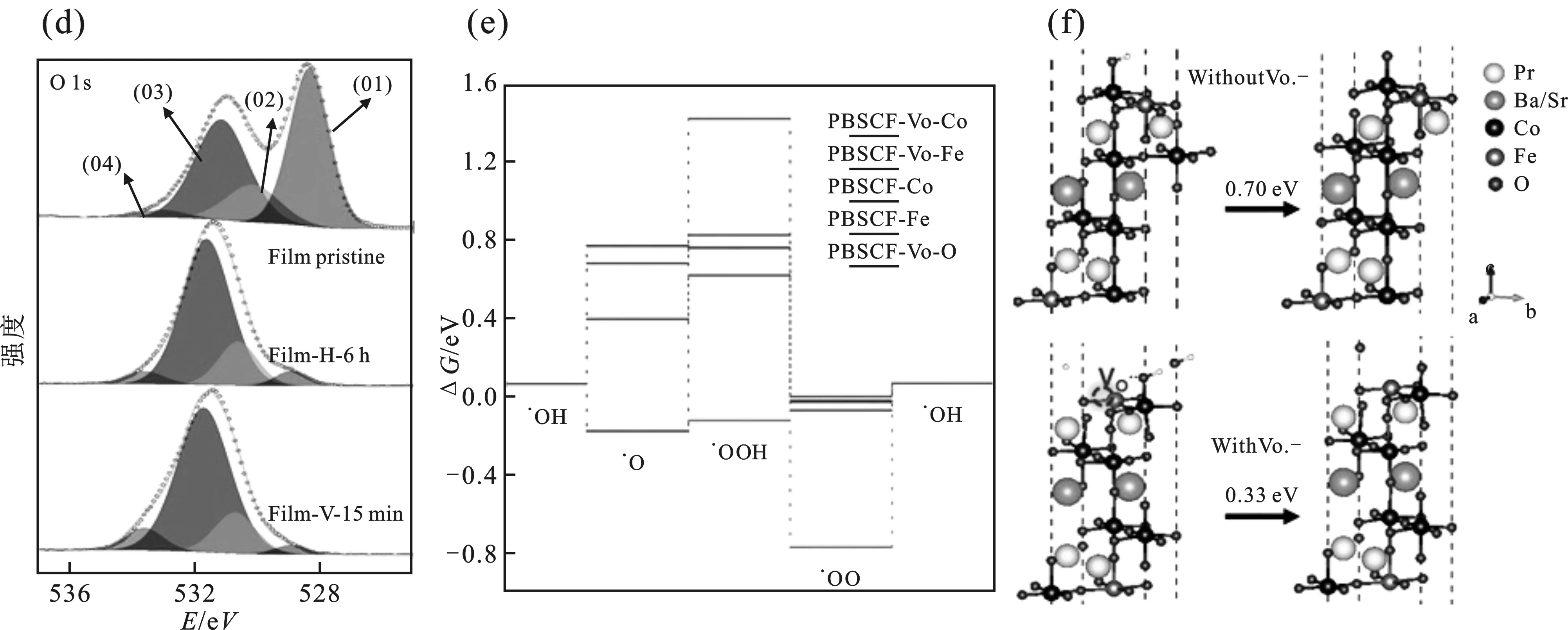
图1 钙钛矿的晶体结构示意图Fig.1 Schematic diagram of crystal structure for perovskite 1.2 钙钛矿氧化物的电催化性能钙钛矿氧化物的电催化性能与其电子结构密切相关,电子结构又取决于钙钛矿的晶胞组成。A、B位金属可分别被不同金属替代,由于不同离子半径大小的差异,钙钛矿材料的晶体结构容易发生畸变形成四方晶系、正交晶系、单斜晶系或其它结构。组成元素的多样性导致其晶体结构和电子结构的灵活性,因此在设计高活性电催化材料时更加具有实际操作性,由此钙钛矿氧化物受到了电催化领域研究者们的青睐[10]。同时钙钛矿氧化物具有结构稳定、耐高温等性质是一种稳定的催化剂。例如Zhao等制备了一种新型钙钛矿结构Sr2(Mg1/3Fe2/3)(Mo2/3Fe1/3)O6-δ用作固体氧化物燃料电池阳极材料,非活性元素Mg的掺入使材料不仅具有良好的氧化还原结构稳定性,而且晶格中产生的反位缺陷使材料具有良好的电化学活性[11]。由此可见,钙钛矿氧化物在电催化领域表现出优异的性能和广阔的应用前景,为新型高效非贵金属电解水催化剂的开发设计提供了一种可行性策略。 1.3 能源领域应用装置1.3.1 固体氧化物燃料电池 固体氧化物燃料电池(SOFCs)相当于电解水的逆反应,是将各种燃料(H2、O2、CO2)氧化后的化学能转换产生电能。相比于其他类型的燃料电池,固体氧化物燃料电池具有以下几个突出方面,如能量转换效率高、燃料灵活性、全固态结构、高功率密度和无污染等,未来有望得到广泛普及应用的新一代燃料电池[12]。然而,由于制造成本高、维护成本高、使用寿命短等缺点,SOFCs技术的广泛商业化仍十分困难[13]。传统电极材料在相对低温范围内工作表现出的低性能是降低SOFCs操作温度的一个障碍。因此开发替代性的新型电极材料,既能承受SOFCs的操作条件,又能在高温下表现出优异的性能具有重要的意义。 1.3.2 锌空电池 锌空气电池的阳极是糊状锌粉,阴极为碳材料,相比于锂离子电池具有更高的理论容量(1 084 Wh/kg),大约相当于目前锂离子电池的5倍,并且金属锌相比于金属锂更廉价易得、更安全与环境友好,因此作为清洁能源存储与转化装置受到研究者们的广泛关注。但是发生在空气正极的氧还原和氧析出反应本身动力学缓慢,导致过电位大、可逆性差,输出功率密度低,能源效率利用有限,严重阻碍了锌空电池的实际应用发展[14]。 1.3.3 电解水 氢气作为一种清洁、高效的可再生能源,是所有化学燃料中能量密度最高(142 MJ/kg)的,其燃烧产物无污染、可循环利用,是未来能源发展的必然趋势[1-4]。电解水制氢是目前极具潜力的制氢技术,然而高能耗以及贵金属催化剂带来的经济问题等限制了电解水在实际应用中的发展,特别是阳极析氧反应(OER)表现出的大过电位以及缓慢的动力学是电解水制氢的瓶颈问题,直接导致电解水制氢成本的上升[5-6,15]。 2 钙钛矿氧化物ABO3的电催化性能研究2.1 研究现状研究催化剂的本质催化活性如何受到限制,并开发设计具有更高活性的电催化剂对于未来新型能源的发展具有重要示范意义。钙钛矿氧化物作为电催化剂,其催化性能主要受表面催化位点活性和电导率等因素的重要影响[16]。钙钛矿材料表面催化位点活性较低,是由于其表面活性位点被催化活性不高的A位原子所占据,而且暴露的大多为低指数晶面[17-18]。另外常规合成法制备的产物粒度大、比表面积小等,都是导致钙钛矿氧化物表面催化活性位点暴露不足的主要因素,限制了其在电催化领域的应用。 其次催化剂材料的导电率影响催化过程中的电子传输,电导率主要与原子的自由电子数有关,尤其与最外层电子数有关。在钙钛矿型金属氧化物中,B位金属离子一般为 Fe,Ni,Mn,Co,Cr。实验发现当 B位的过渡金属为Fe 和Cr时,钙钛矿型金属氧化物活性较弱,所以 B位过渡金属为 Mn、Ni、Co 研究得较多。研究者们认为,钙钛矿结构的电催化析氧活性与其中B位过渡金属eg轨道的电子填充程度有着紧密的联系[19]。根据杂化轨道理论,过渡金属d轨道和氧原子2p轨道杂化,由于钙钛矿材料的电子结构分布(过渡金属eg轨道的电子填充程度)决定了其与电催化反应物中间态的成键能力,eg轨道上填充的电子可以有效与含氧中间体相互作用,从而促进电子在表面活性位点和被吸附中间体之间的转移[20-21]。Yang Shao-Horn教授研究发现钙钛矿氧化物B位过渡金属eg轨道上的电子填充数目接近于1.2~1.3时电催化析氧性能最佳,钙钛矿B位金属eg轨道上的电子填充数目与其达到50 uA/cm2析氧电流密度所需的电压成火山图关系[22]。 高效催化剂的开发设计能够降低电解水反应的能量势垒,催化剂主要通过改变反应路径降低反应活化能,从而加快反应动力学,提升能量转换效率。催化剂活性位点上的表面电荷可以调节中间体的吸附和脱附,异质原子掺杂可以调节局部电子结构,诱导电荷转移到邻近的掺杂位点,引起电荷重新分布,从而调节催化活性位点与反应物分子相互作用[23]。因此,实验与理论计算相结合研究催化剂表面活性位点与反应物分子以及活性中间体之间相互作用更加科学合理。 2.2 A、B位掺杂鉴于此,科研人员提出了一系列的优化策略提高钙钛矿氧化物的电催化性能。文献中已报到的方法有掺杂或缺陷调控,例如A、B位阳离子掺杂或氧离子缺陷调控等[24-25]。钙钛矿A、B位金属原子可被不同氧化态或不同半径大小的金属全部或部分替代,双钙钛矿结构为保持电中性,会诱导产生氧缺陷或B位金属离子的价态升高。因此当使用其他金属阳离子取代A位金属时,可以调节B位金属离子的氧化状态或氧缺陷的含量。碱土金属与镧系金属的离子半径基本相同,因此稀土金属可用于替代A位的碱土金属。例如,Shao-Horn教授研究了一系列双钙钛矿氧化物(Ln0.5Ba0.5)CoO3-x(Ln= Pr,Sm,Gd和Ho),相比于Ba0.5Sr0.5Co0.8Fe0.2O3-x这类双钙钛矿材料表现出更高活性与稳定性,研究结果表明从Pr到Ho随着镧系元素离子半径的增大钴氧化态随之增大,双钙钛矿中Co—O键的杂化也随之增大,其中Pr0.5Ba0.5CoO3-x催化活性最高[26]。He等研究了A位离子对LaMnO3钙钛矿材料作为锌空电池双功能氧电极电催化活性的影响,结果发现当A位离子处于缺失状态时,有利于提升LaMnO3的氧催化活性;而当A位离子处于富余状态时,则不利于提升LaMnO3钙钛矿材料的电催化活性[27]。Liu等系统研究了A位离子缺陷对LaNiO3晶体结构、电子结构的影响,研究发现A位诱导的空位缺陷增强了NiO6八面体的压缩应变,对Ni—O共价键具有正向增强作用;此外Ni离子的eg电子填充和Ni 3d-O 2p杂化重叠态也得到优化,增强氢氧/氧表面吸附和σ*电子转移能力,这是LaNiO3钙钛矿氧化物作为双功能氧催化剂性能提升的根本原因[28]。Nam等分别对比了A位含锶(Sr)和不含锶(Sr)对LaMn0.5Ni0.5O3钙钛矿氧化物晶体结构以及形貌的影响,研究发现Sr掺杂后颗粒尺寸减小并且表面的Ni3+价态增加,同时Sr掺杂后La0.8Sr0.2Ni0.5Mn0.5O3的电催化ORR电流密度增加以及起始电位正向偏移[29]。黄小青课题组制备了LaFexNi1-xO3双钙钛矿纳米棒状结构用于电催化析氧催化剂,由于纳米棒的高比表面积以及Fe的掺入对钙钛矿电子结构的优化,该催化剂材料表现出仅需302 mV过电位就能产生10 mA/cm2析氧电流密度[30]。 2.3 氧缺陷的调控调节钙钛矿结构中氧缺陷的浓度是提升性能的又一有效策略,氧缺陷浓度增加随之BO6八面体畸变越严重,并且O 2p和B 3d轨道之间的杂化更加接近费米能级。例如,Goodenough教授课题组分别制备了CaCoO3和SrCoO3立方相钙钛矿结构,虽然二者具有相似的CoIV中间自旋态,但更小的晶格参数以及更短 的表面氧分离路径使CaCoO3的电催化析氧活性更高。作者研究了可能的反应路径机理见图2(a~c):第1种反应路径,催化剂表面—O-与电解液中的OH-相互作用形成—OOH-;第2种反应路径,催化剂表面两个—O-形成一个—OO2-和一个氧空位,从—OO2-分离出O2并留下了氧空位再与电解质OH-作用。CaCoO3催化剂材料的表面氧分离路径更短,所以第2种反应路径更快[图2(a~c)][7]。刘美林教授利用表征技术结合第一性原理计算,系统研究了氧缺陷调控对PrBa0.5Sr0.5Co1.5Fe0.5O5+δ双钙钛矿材料析氧反应速率的提升机理,适量氧空位既可以增强对OH-的吸附能,又可以降低O*在表面形成所需的活化能,从而极大地促进析氧反应动力学;而过量氧空位会增加钙钛矿材料的带隙并降低O 2p价带中心,阻碍析氧反应动力学的发展;因此只有协同调控才能实现氧空位对PrBa0.5Sr0.5Co1.5Fe0.5O5+δ双钙钛矿材料析氧活性的增强图2(d~f)[22-23,31-32]。Gang Wu教授通过高温氢气处理实现了对钙钛矿BaTiO3材料中氧缺陷的调控,该方法显示氧缺陷是优化钙钛矿电子填充状态和提高导电性的有效方法,对于提高钙钛矿电催化性能至关重要,电化学测试显示该钙钛矿材料在低于1.6 V的低电压区间表现出优于IrO2的析氧活性以及起始电压低为1.32 V时相同电位下表现出更大的电流密度,因此实现了高效双功能氧催化剂的制备[33]。Zhao等合成了La0.5Sr0.5CoO2.91纳米线用作电催化析氧反应与氧还原反应(ORR)的催化剂,作者解释氧空位的产生降低了晶格氧和非晶格氧之间的排斥从而强化对电催化过程中中间体氧吸附,因此该催化剂表现出优异的催化性能[34]。邵宗平课题组通过在La1-xFeO3-x中调控A位阳离子缺陷,因A位阳离子缺陷所产生的额外氧空位可以促进氧离子的传输以及表面产生少量Fe4+离子,从而实现了氧还原和氧析出反应电催化活性的提升[35]。吴长征教授利用元素掺杂和氢气处理相结合的方法使Ca0.9Yb0.1MNO3-x产生晶格氧缺陷实现了钙钛矿材料电子结构的优化,Mn eg轨道电子填充状态高达0.81,并且提高了导电性,相比于未处理前的催化剂,含有晶格氧缺陷的Ca0.9Yb0.1MnO3-x在500 mV过电压处的电流密度提升100倍,实现了电催化析氧活性显著增强并且在碱性介质中表现出优良的稳定性[22]。Ramezanipour等以4种不同结构类型的SrMNO3-δ为例研究了氧空位以及结构和电催化析氧活性之间的相关性,其中OER活性最高的是最缺氧的SrMnO2.5化合物,其结构为以锰周围的方锥体配位结构;SrMnO2.6的结构是MnO5三角双锥体和MnO6八面体,其OER活性居中;立方相SrMnO3的OER性能第三;OER活性最不活跃的是六边形SrMnO3,表明电催化活性与氧缺乏程度以及多面体结构有关[36]。Kim等通过钙钛矿亚表面氧空位诱导的金属d带中心提升增强双功能ORR/OER电催化活性,仅将其作为Sm0.5Sr0.5CoO3-δ(SSC)钙钛矿氧化物中氧空位浓度的函数,以检查δ和电子结构之间的密切关系。研究发现ORR/OER的一个重要因素仅受钙钛矿氧化物中过渡金属的氧化状态的影响,而不受氧空位浓度的影响[37]。
图2 (a~c)ACoO3(A=Ca,Sr)中可能的OER机制,(a)传统的OER机制涉及在活性表面金属位点上的四个 质子-电子转移步骤,(b和c)两种提出的基于Co4+—O2-键的OER机制[7];(d~f)PrBa0.5Sr0.5Co1.5Fe0.5O5+δ 双钙钛矿材料的O1s XPS谱图以及四电子OER机制的吉布斯自由能图与计算模型[32]Fig.2 The possible OER mechanism in ACoO3 (A=Ca,Sr) (a~c).(a) The traditional OER mechanism involves four proton-electron transfer steps at the metal active sites.(b and c) Two proposed OER mechanisms based on the Co4+-O2- bond [7].(d~f) O1s XPS spectrum and Gibbs Free Energy Model of PrBa0.5Sr0.5Co1.5Fe0.5O5+δ double perovskite material [32] 3 结论与展望尽管钙钛矿材料在各种催化领域应用中取得了较大的研究进展,但仍然存在着一些机遇和挑战。在电催化领域尤其是关于氧氧化还原反应中,关于钙钛矿氧化物催化活性位点的调控以及其性能增强机制的研究还不够深入。另外,对于钙钛矿结构在电催化过程中催化活性中心的确定以及催化剂表面活性位点与反应物分子或活性中间体的相互作用的研究,以及钙钛矿高效与稳定的电催化析氧催化机制的阐明,也有待更进一步深入研究,从而实现未来高效钙钛矿基电催化材料的合理开发设计。 |
【本文地址】
今日新闻 |
推荐新闻 |