【重磅综述】间歇性禁食对健康、衰老和疾病带来的影响 |
您所在的位置:网站首页 › 身体应激反应一般多长时间 › 【重磅综述】间歇性禁食对健康、衰老和疾病带来的影响 |
【重磅综述】间歇性禁食对健康、衰老和疾病带来的影响
|
以下文章来源于老顽童说 ,作者老顽童说  老顽童说 公众号致力于传播衰老相关的前沿科研进展和趣味科普,帮助大家更深入地了解衰老背后的科学故事~  关注我们,获取更多相关资讯 翻译 By 刘黎啸、平佳乐、车姗姗、孙国强 “减去浮华两三分,便的自在悠然心”,为了这份悠然自在,如今越来越多的人尝试各种方法去减肥,其中间歇性禁食是近年来“火出圈儿”的减肥方案之一,科学家们也逐渐发现了它对人们总体健康指标的积极影响,不仅体重有所减轻,甚至有利于减缓或逆转衰老和许多疾病发生发展的进程。2019年11月,来自约翰霍普金斯大学医学院的Mark P. Mattson研究团队在The NEW England Journal of Medicine发表了题为“Effects of Intermittent Fasting on Health, Aging, and Disease”的综述,阐明了间歇性禁食对机体健康、衰老和疾病的影响机制。 通讯作者:Mark P. Mattson(图源网络) 前言 根据Weindruch和Sohal于1997年发表的一篇文章,减少食物供应(热量限制)会对动物的衰老和寿命产生显著的影响。文章提出,限制热量摄入对健康有益的原因是有害氧自由基的减少。此后,人们又进行了数百项动物研究和数十项间歇性禁食控制的临床研究,结果表明,禁食期间每天或每周的几天都发生着代谢方式的转变即肝源性葡萄糖代谢转变为脂肪细胞源性酮类物质代谢。尽管间歇性禁食对延长寿命的作用是受性别、饮食和遗传因素等多方面影响,但起码目前在小鼠和非人灵长类动物中进行的研究表明,限制热量对它们健康寿命影响是一致的。 在动物和人身上的研究表明,间歇性禁食的许多健康益处不仅仅源于自由基产生减少或体重减轻。相反,间歇性禁食引发了进化上保守的、适应性的细胞反应,这些反应以一种改善葡萄糖调节、增加抗应激性和抑制炎症的方式整合在器官之间及器官内部。禁食期间,细胞会激活一些通路应答,包括内在抗氧化代谢压力防御及受损分子清除或修复相关的途径(图1)。在喂食期间,细胞参与组织特异性的生长和可塑性过程。然而,对于大多数人来说,每日三餐必不可少,外加零食点心,因此间歇性禁食基本不会发生。 临床前研究一致表明,在动物模型上,间歇性禁食对广泛的慢性疾病(包括肥胖、糖尿病、心血管疾病、癌症和神经退行性脑疾病)具有强大的改善效果。新陈代谢转换的周期性启动不仅可以在禁食期间为细胞提供燃料所必需的酮,而且还引发了高度协调的系统和细胞反应,并将其带入进食状态,以增强精神和身体性能以及抗病能力。 本文中,作者回顾了在动物和人类身上进行过的相关研究,这些研究说明了间歇性禁食是如何影响总体健康指标,减缓或逆转衰老和疾病进程的。首先,文章描述了最常被研究的间歇性禁食的方案以及间歇性禁食带来的代谢和细胞反应。接着,文章介绍并讨论了临床前研究和最近的临床研究结果,尤其是在正常人和代谢紊乱(肥胖、胰岛素抵抗、高血压等)患者中测试的间歇性禁食方案。最后,文章提供了关于间歇性禁食方案的制定和实施方法。不过,文章没有讨论关于长期禁食(从几天到几周)的相关实践性研究,建议感兴趣的读者可以参考欧洲临床经验的禁食方案。 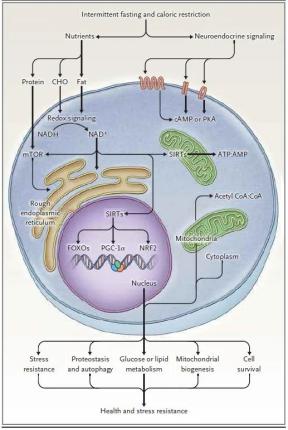 图1:细胞对热量限制的反应将进食和禁食周期与新陈代谢结合起来。总能量摄取量、膳食组成和两餐之间的禁食时间导致了生物能量传感器烟酰胺腺嘌呤二核苷酸(NAD+)与NADH、ATP与AMP、乙酰辅酶A与辅酶A水平的波动。这些中间能量载体激活下游蛋白,调节细胞功能和应激抵抗,包括转录因子如叉头框O蛋白家族(FOXOs)、过氧化物酶体增生激活受体γ协同刺激因子1α(PGC-1α)和核因子红细胞2相关因子2(NRF2);激酶如AMP激酶(AMPK);以及去乙酰酶如sirtuins家族(SIRTs)。间歇性禁食引发神经内分泌反应和适应,其特征是低水平的氨基酸、葡萄糖和胰岛素。胰岛素-胰岛素样生长因子1(IGF-1)信号通路的下调和循环氨基酸的减少可以抑制哺乳动物雷帕霉素受体(mTOR)的活性,从而抑制蛋白质合成以及刺激自噬。禁食期间,AMP与ATP的比例增加,AMPK被激活,触发系统修复,以及合成代谢受阻。乙酰辅酶A(CoA)和NAD+是表观遗传修饰因子如SIRTs的辅助因子。SIRTs使FOXOs和PGC-1α去乙酰化,导致参与逆境抵抗和线粒体生物发生相关基因的表达。总的来说,机体对间歇性禁食的反应是尽量减少合成代谢过程(合成、生长和繁殖),提升系统维护和修复,增强抗逆性,回收受损分子,刺激线粒体生物发生,促进细胞生存,所有这些都有助于改善健康和抗病能力。cAMP:环磷酸腺苷;CHO:碳水化合物;PKA:蛋白激酶A;redox:氧化还原。 间歇性禁食和代谢转换 葡萄糖和脂肪酸是细胞的主要能量来源。饭后,葡萄糖被用于能量的产生,脂肪以甘油三酯的形式储存在脂肪组织中。在禁食期间,甘油三酯被分解为脂肪酸和甘油以提供能量,肝脏脂肪酸则转化为酮体,为许多组织尤其是大脑提供主要的能量(图2)。在饱食状态下,人体血液中的酮含量很低,在禁食后的8到12小时内会上升,24小时内会达到2-5 mM的水平;在啮齿动物中,禁食后4到8小时内血浆酮水平开始升高,24小时内升高至mM的水平。在间歇性禁食疗法中,这种反应的时间为制定合理的禁食时间提供了一定的指导。 在人体上,研究最广泛的3种间歇性禁食方案是隔日禁食、5:2间歇性禁食(每周禁食2天)和每日限时进食。如果每周有一天或更多的时间在饮食上明显减少热量的摄入(例如每天减少500到700卡路里),那么这些日子里身体内的酮水平就会升高。由葡萄糖转变为脂肪酸和酮体产生能量从而导致换气比值(二氧化碳产生和氧耗的比例)的降低,表明脂肪酸和酮体来源的能量产生,提高了代谢的灵活性和效率。 酮体不仅仅是在禁食期间机体所消耗的燃料,它们还是影响细胞和器官功能的重要信号分子。酮体调节了许多已知影响健康和衰老的蛋白质和分子的表达和活性,包括过氧化物酶体增生激活受体γ协同刺激因子1α(PGC-1α)、成纤维细胞生长因子、烟酰胺腺嘌呤二核苷酸(NAD+)、去乙酰化酶、聚(腺苷二磷酸[ADP] -核糖)聚合酶1(PARP1)、ADP核糖环化酶(CD38)。通过影响这些主要的细胞途径,在禁食期间产生的酮体对系统代谢有深远的影响。此外,酮体刺激脑源性神经营养因子基因的表达(图2),与大脑健康和精神以及神经退行性疾病有关。 那么,间歇性禁食带来的益处有多少是由代谢转变引起的?又有多少是得益于体重减轻呢?但其实,很多研究已经表明,间歇性禁食带来的诸多益处如改善血糖调节、血压和心率,提升耐力训练的功效以及减少腹部脂肪等都与体重减轻没有太大关联。 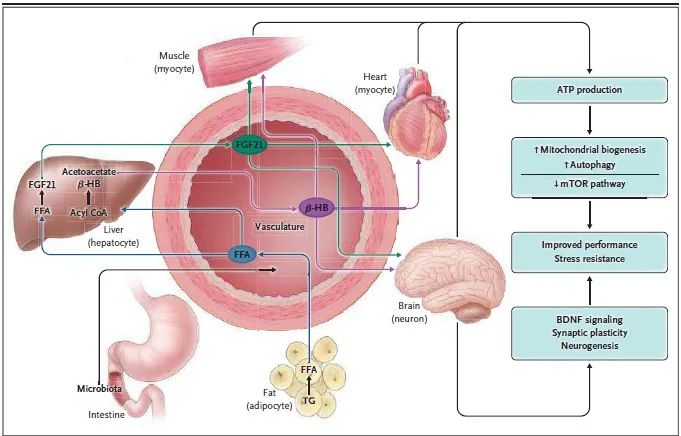 图2:新陈代谢对间歇性禁食的适应。10至14小时或更长时间的热量限制会导致脂肪细胞中肝糖原储备的消耗和甘油三酯(TGs)水解为游离脂肪酸(FFAs)。释放到循环系统中的游离脂肪酸被转运到肝细胞,在那里它们产生酮体乙酰乙酸酯和β-羟基丁酸酯(β-HB)。FFAs还激活转录因子过氧化物酶体增殖激活受体α(PPAR-α)和转录激活因子4(ATF4),导致成纤维细胞生长因子21(FGF21)的产生和释放,这是一种对机体和大脑细胞都有广泛影响的蛋白质。β-HB和乙酰乙酸被主动地运输到细胞中,进而代谢为乙酰辅酶A,进入三羧酸(TCA)循环并产生ATP。β-HB也具有信号功能,包括促进转录因子如环AMP反应元件结合蛋白(CREB)和核因子κB(NF-κB)的激活,以及脑源性神经营养因子(BDNF)在神经元中的表达。空腹时葡萄糖和氨基酸水平的降低导致mTOR通路活性的减弱和自噬的增加。此外,热量限制还会刺激线粒体生物发生和线粒体解偶联反应。 间歇性禁食和抗压能力 与当今人们的生活方式相比,人类祖先并没有每天按规律的时间间隔食用三餐和点心,也没有过着久坐不动的生活。与之相反,他们忙于在食物分布稀少的生态领域获取食物。随着时间的推移,智人经历了进化上的改变,以适应这种环境,如大脑的进化,使其拥有了创造力、想象力和语言能力;身体的变化使物种成员能够利用自己的肌肉力量远距离跟踪猎物。 本文回顾了以往的研究,并通过更详细地讨论表明,大多数器官系统对间歇性禁食的反应,使机体能够耐受或克服损伤变化,然后恢复体内稳态。反复处于禁食期会导致持久的适应性反应,从而赋予抵抗后续损伤变化的能力。细胞通过参与协调的适应性应激反应来响应间歇性禁食,从而增加抗氧化防御、DNA修复、蛋白质质量控制、线粒体生物发生和自噬水平、以及下调炎症(图3)。这些对禁食和进食的适应性反应在整个物种分群中都是保守的。维持间歇性禁食习惯的动物身体和大脑中的细胞均表现出更佳的状态,并且对各种潜在的破坏性侵害具有强大的抵抗力,包括涉及代谢、氧化、离子、创伤和蛋白毒性应激的损伤。间歇性禁食能够刺激自噬和有丝分裂的发生,同时抑制mTOR(哺乳动物雷帕霉素受体)蛋白合成途径。这些反应使细胞能够去除氧化损伤的蛋白质和线粒体并回收未损坏的分子成分,同时暂时减少整体蛋白质的合成以节省能量和分子资源(图3)。进食过量且久坐的人的上述分子机制尚未激活或已被抑制。 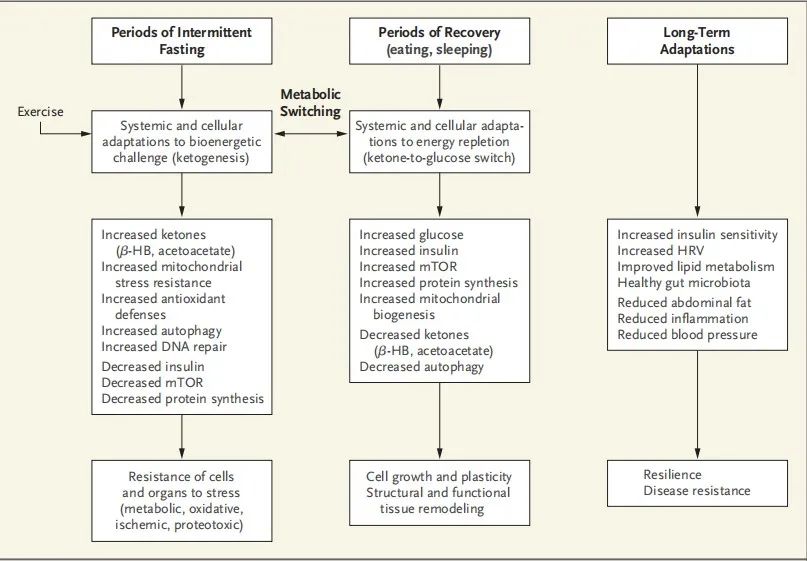 图3:利用间歇性代谢转换来改善器官功能和对压力和疾病的抵抗力的细胞和代谢机制。饮食热量限制足以引起肝糖原存储的消耗,从而触发了使用脂肪酸和酮体进行代谢的转换。细胞和器官系统通过增强线粒体功能、激活抗逆性和抗氧化剂防御能力的信号传导途径,同时上调自噬以去除受损分子并回收其成分,从而适应这一生物能量挑战。在热量限制期间,细胞的抗应激模式表现为减少胰岛素信号传导和整体蛋白质合成。同时配合运动可以增强禁食产生的以上效果。在从禁食中恢复(进食和睡眠)时,葡萄糖水平增加,酮水平达到饱和,并且细胞增加蛋白质合成,进行生长和修复。维持间歇性禁食的方法,特别是与定期锻炼相结合时,会诱导身体产生许多长期适应能力,从而改善精神和身体机能并增加疾病抵抗力。HRV:心率变异性。 间歇性禁食对健康和衰老的影响 截至目前,对热量限制和间歇性禁食的研究还集中在衰老和寿命上。在对动物热量限制进行了近一个世纪的研究之后,总的结论是大幅度减少食物摄入量可以延长寿命。 在最早的间歇性禁食研究中,Goodrick及其同事发现,从年轻时开始,每天交替禁食,老鼠的平均寿命可增加80%。但是,热量限制对健康寿命和寿命长度的影响程度各不相同,并且会受到性别、饮食、年龄和遗传因素的影响。对1934年至2012年期间可获得的数据进行的荟萃分析显示,热量限制使大鼠的中位寿命延长了14%至45%,而使小鼠的中位寿命仅增加了4%至27%。一项对41只重组近交系小鼠的研究显示出对寿命影响的巨大差异,从寿命的延长到寿命的缩短,都取决于种系和性别。但这项研究只使用了一种热量限制方案(40%的热量限制),没有评估健康指标、死亡原因或潜在机制。肥胖与寿命之间存在反比关系,这表明寿命较短的动物在受到如此严格的热量限制时,其脂肪减少的幅度更大,并且更容易饥饿,而寿命较长的肥胖动物的脂肪减少幅度最小。 而在以猴子作为模式生物进行的研究中,两个具有里程碑意义的研究结果差异挑战了健康寿命延长及寿命延长与热量限制之间的联系。其中一项来自威斯康辛大学的研究显示,热量限制对于机体的健康和寿命具有积极效应,而另一项来自美国国家衰老研究所的研究显示,热量限制对总体健康状况确实有明显改善,但死亡率没有显著降低。在这两项研究中,每日热量摄入、干预发生、饮食组成、进食方案、性别和遗传背景因素上的差异可能可以解释两项研究中热量限制对寿命的不同影响。 在人类中,间歇性禁食干预可以改善肥胖、胰岛素抵抗、血脂异常、高血压和炎症,可见,间歇性禁食给健康带来的益处似乎远远超出了仅仅减少热量摄入所能带来的好处。在一项试验中,16名健康成年人参与了隔日禁食22天的方案,他们减少了2.5%的初始体重和4%的脂肪质量,而空腹胰岛素水平降低了57%。在另外两项试验中,超重女性(每项试验中约有100名女性)被分配为5:2的间歇性禁食方案或每日热量摄入减少25%。两组女性在6个月内体重减轻相同,但被分配到间歇性禁食5:2方案中的女性成员,其胰岛素敏感性增加幅度更大,且腰围减少幅度更大。 间歇性禁食对生理和认知的影响 在动物和人类中,间歇性禁食可改善身体机能。例如,尽管体重相似,但是隔日禁食的老鼠比没有食物的老鼠具有更好的跑步耐力。在每天限时喂食或隔天禁食的动物中,身体的平衡和协调性也得到改善。每天禁食16小时的年轻男性,在进行阻力训练2个月后,可以在保持肌肉质量不变的同时减掉脂肪。 动物身上的研究表明,间歇性禁食可增强多个方面的认知能力,包括空间记忆、联想记忆和工作记忆。隔日禁食和每日热量限制可以逆转肥胖、糖尿病和神经炎症对空间学习和记忆的不利影响。 在一项临床试验中,短期热量限制的老年人提高了语言记忆力。在一项涉及轻度认知障碍的超重成年人的研究中,热量限制12个月可改善言语记忆、执行功能和整体认知能力。最近,一项大型的多中心随机临床试验表明,2年的每日热量限制会促进工作记忆的显著改善。当然,目前还需要进一步研究老年人的间歇性禁食对认知的影响,特别是考虑到缺乏影响大脑衰老和神经退行性疾病进展的药理学治疗。 临床应用 在本节中,作者简要回顾了在临床前的疾病动物模型以及各种疾病患者中进行间歇性禁食研究的结果。 肥胖和糖尿病 在动物模型中,间歇性进食可以提高胰岛素敏感性,防止高脂饮食引起的肥胖症,并改善糖尿病视网膜病变。在冲绳岛上,原住居民通常保持间歇性禁食的方式,并且肥胖和糖尿病的发生率很低,而且寿命也很长。冲绳人通常进食能量低但营养丰富的食物,特别是冲绳岛的红薯、其他蔬菜和豆类。同样,遵循CRON(最佳营养热量限制)饮食的卡路里限制协会的成员,糖尿病发生率较低,而且胰岛素样生长因子1(IGF-1)、生长激素、炎症和氧化应激标志物水平较低。 一项多中心研究表明,每日热量限制可改善非肥胖人群的许多心脏代谢危险因素。此外,6项涉及超重或肥胖成年人的短期研究表明,间歇性禁食对减肥的效果与标准饮食一样有效。最近的两项研究表明,每日热量限制或4:3间断禁食(每周3天禁食)可逆转糖尿病前期或2型糖尿病患者的胰岛素抵抗。但一项为期12个月的研究比较了隔日禁食、每日热量限制和控制饮食的效果,与对照组相比,2个干预组参与者的体重都减轻了,但胰岛素敏感性、血脂水平或血压没有任何改善。 心血管病 间歇性禁食可以改善动物和人类心血管健康的多种指标,包括血压、静息心率、高密度和低密度脂蛋白(HDL和LDL)、胆固醇、甘油三酯、葡萄糖、胰岛素水平和胰岛素抵抗。此外,间歇性禁食可减少与动脉粥样硬化相关的全身炎症和氧化应激的标志物的体内含量。对心电图记录的分析表明,间歇性禁食可通过增强大鼠和人类的副交感神经张力来增加心率变异性。CALERIE(能量摄入减少的长期效应的综合评估)研究表明,在2年内,每天减少12%的卡路里摄入量可以改善非肥胖人群的许多心血管危险因素。Varady等人发现,隔日禁食对体重正常和超重的成年人具有有效的减重和心脏保护的作用。心血管健康指标的改善通常在开始隔日禁食后2至4周内变得明显,然后在恢复正常饮食后的数周内消失。 癌症 一个多世纪以前,Moreschi和Rous发现禁食和热量限制在动物模型上有抑制肿瘤的作用。 此后,大量动物研究表明,每日热量限制或隔日禁食可减少啮齿类动物在正常衰老过程中自发性肿瘤的发生,并抑制多种诱导性肿瘤的生长,同时提高它们对化疗和放疗的敏感性。同样,间歇性禁食被认为会破环癌细胞的能量代谢,抑制癌细胞生长并使其对临床治疗更敏感。其潜在机制包括通过胰岛素和生长激素受体减少信号传导,增强叉头框 O蛋白(FOXO)和核因子红细胞2相关因子2(NRF2) 转录因子的表达。NRF2或FOXO1的基因缺失破环了间歇性禁食对诱发癌症的保护作用,但延长了寿命,而FOXO3的缺失保留了抗癌保护作用,但降低了延长寿命作用。通过间歇性禁食激活这些转录因子和下游靶点,可以产生抵抗癌症的能力,同时增强正常细胞的抗应激能力(图1)。 癌症患者间歇性禁食的临床试验已经完成或正在进行。大部分初始试验都集中在生物标志物的依从性、副作用和表征上。例如,一项针对前列腺癌患者的每日热量限制试验显示,患者的依从性良好(95%),且无不良事件发生。几项涉及胶质母细胞瘤患者的研究案例表明,间歇性禁食可以抑制肿瘤生长并延长生存期。ClinicalTrials.gov(美国临床试验注册中心)上列出的正在进行的间歇性禁食试验集中在患有乳腺癌、卵巢癌、前列腺癌、子宫内膜癌、结直肠癌和胶质母细胞瘤患者中。具体的间歇性禁食方案因研究而异,但均涉及在化疗期间间歇性禁食。尚无研究确定间歇性禁食是否会影响人类癌症的复发。 神经退行性疾病 流行病学数据表明,特别是在中年时期,过度摄入能量会增加中风、阿尔茨海默病和帕金森病发生的风险。大量的临床前证据表明,隔日禁食可以延缓阿尔茨海默病和帕金森病动物模型疾病过程的发生和发展。间歇性禁食通过多种机制增强神经元的抗应激能力,包括增强线粒体功能和刺激自噬、神经营养因子产生、抗氧化防御和DNA修复。此外,间歇性禁食可增强GABAergic抑制性神经递质(即与γ-氨基丁酸相关的抑制性神经递质),并预防癫痫发作和兴奋性中毒。但目前对有神经退行性疾病风险或受神经退行性疾病影响的人进行间歇性禁食试验的数据是缺乏的。理想情况下,应在疾病过程的早期开始进行干预,并持续足够长的时间(例如,为期1年)以检测干预措施对疾病的治疗作用。 哮喘、多发性硬化症和关节炎 减肥可减轻肥胖患者的哮喘症状。在一项研究中,坚持隔日禁食的患者在热量限制当日的血清酮体水平升高,并在2个月内体重下降,在此期间哮喘症状和气道阻力得到缓解。症状的减轻与血清中炎症和氧化应激标志物水平的显著降低有关。多发性硬化症是一种自身免疫性疾病,其特征是中枢神经系统中的轴突脱髓鞘和神经元变性。在多发性硬化症(实验诱导的自身免疫性脑脊髓炎)小鼠模型中,隔日禁食和连续3天的周期性热量限制可减少自身免疫性脱髓鞘作用并改善功能效果。最近两项初步研究表明,坚持间歇性禁食治疗的多发性硬化症患者的病症在2个月内减轻。因为它能减少炎症,所以间歇性禁食对类风湿性关节炎也是有益的,且的确存在证据支持它在关节炎患者中的作用。 手术和缺血性组织损伤 间歇性禁食可减少动物模型中的组织损伤、改善创伤性和缺血性组织损伤的功能结果。术前禁食可减少组织损伤和炎症,改善手术结果。在血管外科损伤的动物模型中,禁食3天可减少肝脏和肾脏的缺血再灌注损伤,并且在损伤前,可减少由创伤引起的颈动脉内膜增生。一项随机、多中心化研究表明,术前2周每日热量限制可改善接受胃旁路手术患者的预后。这些发现表明术前间歇性禁食是一种安全有效的、改善手术预后的方法。 一些研究表明,间歇性禁食在颅脑外伤或脊髓损伤的动物模型中具有有益作用。损伤后间歇性禁食也可有效改善颅脑外伤小鼠模型的认知功能障碍。在颈或胸脊髓损伤前后,开始间歇性禁食可减少组织损伤并改善大鼠的功能效果。新的证据表明,间歇性禁食可以增强运动效果,并可能是减少运动员脑部和脊髓外伤所致发病率和死亡率的一种实用方法。动物研究表明,间歇性禁食可以保护大脑、心脏、肝脏和肾脏免受缺血性损伤,但其对中风或心肌梗死患者的潜在治疗效果仍有待检验。 实际问题 尽管有证据表明间歇性禁食对健康有好处,并且适用于许多疾病,但在社区群众和患者中,广泛采用这些饮食方式仍然存在障碍。首先,一日三餐加零食的饮食习惯在我们的文化中根深蒂固,病人或医生很少会考虑改变这种饮食习惯。发达国家的富足粮食和广泛市场营销也是需要克服的主要障碍。第二,如果采用间歇性禁食法,很多人在禁食期间会感到饥饿、易怒,且注意力下降。然而,这些开始的副作用通常在1个月内消失,应该告知患者这一情况。第三,大多数医生没有受过专门的间歇性禁食治疗的训练。医生可以建议患者在几个月的时间内逐渐减少每天进食的时间段,目标是每天禁食16到18小时(图4),或者医生可以推荐5:2间歇性禁食的饮食方式,第一个月每周1天摄入900到1000卡路里,第二个月每周2天,第三个月每周2天进一步减少到750卡路里,最后第四个月每周2天摄入500卡路里。医生应咨询营养师或营养学家,以确保满足患者的营养需求,并提供持续的咨询和教育。与所有的生活方式干预一样,医生提供足够的信息、有效的沟通和支持以及定期的积极强化干预是很重要的。 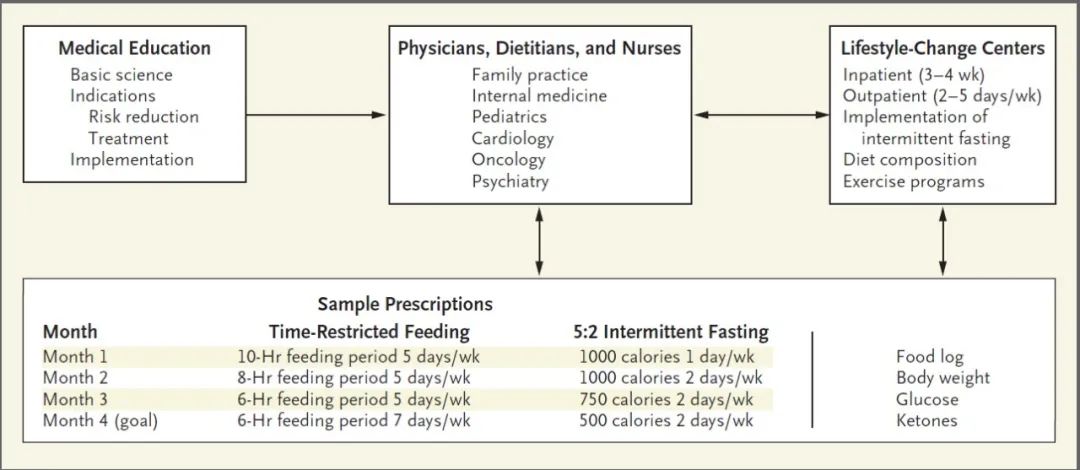 图4:将间歇性禁食方式纳入保健措施和生活方式。作为医学院疾病预防培训的一个组成部分,医学生可以学习间歇性禁食如何影响新陈代谢、细胞和器官,如何适应间歇性禁食、间歇性禁食的主要适应症(肥胖症、糖尿病、心血管疾病和癌症),以及如何实施间歇性停药,实现长期效益最大化。医生可以结合间歇性禁食处方,对患有慢性疾病或有此类疾病风险的患者进行早期干预,特别是那些与暴饮暴食和久坐生活方式相关的疾病。可以设想在住院和门诊设施配备饮食、营养、运动和心理学方面的专家,帮助患者过渡到可持续的间歇性禁食和运动方案(由基本健康保险政策覆盖)。作为一个特定处方的例子,患者可以选择每日限时进食(18小时禁食期和6小时进食期)或5:2间歇性禁食方式(禁食[或,摄入500卡路里]每周2天),过渡期为4个月,来实现预期目标。为便于处方的执行,医生等工作人员应在4个月期间与患者频繁联系,并密切监测患者的体重、葡萄糖和酮水平。 结论 临床前研究和临床试验表明,间歇性禁食对许多健康状况有广泛的益处,如肥胖、糖尿病、心血管疾病、癌症和神经系统疾病。动物模型研究表明,间歇性禁食可以改善整个生命周期的健康状况,而目前的临床研究主要涉及持续数月的相对短期的干预措施,人们是否能连续多年保持间歇性禁食,并有可能获得从动物模型中看到的益处,还有待确定。此外,临床研究主要集中在超重的年轻人和中年人,作者认为不能将在这些研究中观察到的间歇性禁食的益处和安全性推广到其他年龄组,以及正常体重的普通人。 虽然人们还不完全了解具体的机制,但是间歇性禁食的有益影响涉及代谢转换和细胞应激抵抗。然而,有些人不能或不愿意坚持间歇性禁食方案。通过进一步了解间歇性禁食与广泛的健康益处之间的联系,也许能够开发出有针对性的药物疗法,模拟间歇性禁食的效果,而无需实质性地改变饮食习惯。 对动物模型中热量限制和间歇性禁食机制的研究已经引起了药物干预措施的开发和测试,这些干预措施模拟了间歇性禁食对健康和疾病的改善作用。例如采用温和的代谢调控药物(2-脱氧葡萄糖、二甲双胍和线粒体解偶联剂)、增强线粒体生物能量的药物(酮酯或烟酰胺核糖)或抑制mTOR途径的药物(西罗莫司)。然而,动物模型的相关数据表明,这些药理学方法的安全性和有效性可能不如间歇性禁食。 最后,小编在这里提醒大家,虽然目前的多项研究都表明间歇性禁食对机体的有益作用,但并不一定适用于所有人,尤其是身体有疾病或者营养不良的人群,要遵守医嘱,谨慎尝试!  来源:老顽童说 原标题:《【重磅综述】间歇性禁食对健康、衰老和疾病带来的影响》 阅读原文 |
【本文地址】