科学网 |
您所在的位置:网站首页 › 蚀刻率公式 › 科学网 |
科学网
|
Arrhenius 方程与活化能
已有 14725 次阅读 2022-5-25 15:25 |系统分类:教学心得 本文拟探究Arrhenius 方程与活化能Ea的由来,并介绍化学动力学中Arrhenius 方程的两个重要应用. 1. Arrhenius 方程 19世纪末瑞典人Arrhenius根据大量实验数据,在Van't Hoff近似规律的基础上,提出了温度对化学反应速率常数影响的经验公式――Arrhenius 方程, 参见式(1). 式(1)中k为反应速率常数;T代表绝对温度; R为摩尔气体常数,R=8.314J・mol-1・K-1;Ea称活化能. 式(1)积分,可写成Arrhenius 方程的指数形式,参见式(2). 式(2)中A称指前因子,也称频率因子;其单位与化学反应速率常数k相同. 将(k1,T1)及(k2, T2)两组数据分别代入式(2),并整理可得: 式(3)可用于k2, k1,T1,T2及Ea五个变量之间的相互换算. 2. 活化能Ea 活化能Ea也称反应阻力,在一定温度范围内,化学反应的Ea是一个与温度无关的常数. 式(1)可变形为: 式(4)常被称为活化能的定义式. 另式(2)两边同取自然对数可得: 动力学研究中,常通过绘制lnk~1/T线段,利用式(5)获取化学反应的表观活化能Ea. 需明确Arrhenius 方程是一个纯数学拟合式,过度探寻“指前因子A及表观活化能Ea物理意义” 的研究价值不高. 3. Arrhenius 方程的应用 例1:已知某化学反应速率常数k与其三步基元反应的速率常数k1、k2、k3定量关系如下,
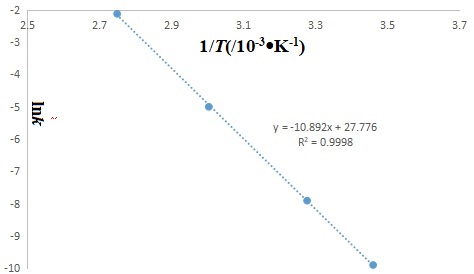
解:依 式(6)两边同取自然对数可得: 式(7)两边同时对温度求导可得: 将式(1)代入式(8)可得: 式(9)两边同乘以R・T2得: 例2:在乙醇溶液中进行如下反应:C2H5I + OH- → C2H5OH+I-,实验测得不同温度下的k如下,求该反应的活化能[1]. t/℃15.8332.0259.7590.61k(/10-3・dm3・mol-1・s-1)0.05030.3686.71119解:由化学反应速率常数单位可推断该反应为二级反应. 另由表中数据换算可得表1: 表1. lnk~1/T关系 1/T(/10-3・K-1)3.46043.27693.00392.7490lnk-9.8976-7.9075-5.0042-2.1287以lnk~1/T作图可得:
图1. lnk~1/T关系图 图1为lnk~1/T关系图,图中斜率,k斜率=-10.892. 由式(4)可得:k斜率=-Ea/R=-10.892 Ea=10.892×8.314×103=90.556(kJ・mol-1) 4. 结论 Arrhenius 方程是一个纯数学拟合式,过度探寻“指前因子A及表观活化能Ea物理意义” 的研究价值不高. 参考文献 [1]天津大学物理化学教研室编. 物理化学(下册,第四版).北京: 高等教育出版社, 2001,12:293 https://blog.sciencenet.cn/blog-3474471-1340174.html 上一篇:n级反应速率方程积分式推导下一篇:非基元反应速率方程通式 收藏 IP: 27.19.11.*| 热度| |
【本文地址】