乙酸路易斯结构:绘图和详细说明 |
您所在的位置:网站首页 › 简化路易斯结构式怎么写 › 乙酸路易斯结构:绘图和详细说明 |
乙酸路易斯结构:绘图和详细说明
|
在本文中,我们将了解乙酸路易斯结构。 乙酸的化学式为 CH3COOH 是一种简单的有机或一元羧酸,由两个碳、两个氧和四个氢组成。 它是一种弱酸,也称为乙酸,呈白色液体,带有强烈的醋臭味。 它腐蚀金属和组织。 如何构建CH的Lewis点结构3分阶段 COOH(乙酸):长期接触醋酸会导致眼睛、皮肤、鼻子、喉咙和其他身体部位等受到严重刺激。 当醋酸达到40摄氏度时,它变得易燃易爆。 在液态时,乙酸是一种极性或质子溶剂。 最低价的 路易斯结构 本文将讨论乙酸 (CH3COOH) 的或电子点结构。 在 CH3COOH路易斯结构式,官能团(COOH)包含一个双键,周围原子上的四个孤对,以及将一个原子连接到另一个原子的八个键合对。 1.确定CH中的价电子总数3COOH路易斯结构,也称为电子点结构,有助于理解原子或价电子如何在分子中分组。 因此,为每个分子构建路易斯图的第一步是弄清楚存在多少价电子。 价电子是在原子最外层发现的电子。 简单地看一下 CH 中的周期原子群3COOH分子决定价电子。  刘易斯点结构 乙酸 刘易斯点结构 乙酸因为碳在元素周期表的第14族,氧在第16族,氢在元素周期表的第一族,所以碳的价电子是4,氧的价电子是6,化合价电子氢的电子为1。 在碳中,价电子总数为 4。在氧气中,价电子总数为 6。在氢中,价电子总数为XNUMX。可访问的价电子总数 路易斯结构 CH3COOH = 4(2) + 6(2) + 1(4) = 24 个价电子 [CH3COOH分子包含两个碳原子、两个氧原子和四个氢原子]。 2. 找出带负电荷最少的原子,放在中间因为电负性较小的原子更容易与相邻原子交换电子,所以电负性最小的原子总是占据路易斯图的中间位置。 CH3COOH 分子包含三种不同类型的原子:氢、氧和碳。 值得注意的是,在刘易斯图中,氢原子总是在外面移动,这意味着它们总是占据周围的位置,无论场景如何。 这是因为在它们的最外层,氢只能保留两个价电子。 因为碳原子的负电荷比氧原子低,所以它在路易斯图中占据中间位置。 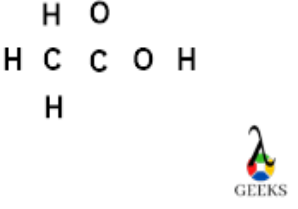 羧基是在 CH 中发现的官能团3COOH 分子 (COOH)。 该基团以结构化方式不断运行。因此,COOH 基团原子在上述结构中排列在一起,而氢始终位于路易斯图中的外部。 3. 使用单键将外部原子连接到核心原子一个单一的连接将所有周围的原子连接到核心原子。 只需使用单键将所有外部原子(氢和氧)连接到中心原子(碳)。只需开始计算我们在上述结构中使用的价电子。 两个价电子形成单键。 采用七个单键将周围的原子连接到上述结构的中心点。  从总共 24 个可用于 CH 的价电子中3COOH,7×2 = 14个价电子用于上述结构。 (10 价电子) = (24 – 14),因此,我们有额外的 XNUMX 个价电子。 4. 从外层原子开始,放置剩余的价电子在这一点上,我们将使用剩余的价电子来完成外部原子的八位字节(氢和氧)。 “八位字节被定义为在其最外层具有八个价电子的原子”。 只有电子对可以在氢原子的最外层被识别,使其成为八位组规则的例外。  图片来源来自 维基百科 图片来源来自 维基百科尽管所有氢原子在其价壳中已经有两个电子,由单个链接引起,但我们将所有剩余的 10 个价电子放在氧外原子上以完成它们的八位字节,如上图所示。 因为每个氧原子有 8 个价电子,每个氢原子有 2 个,所以这些原子很容易完成它们的八位字节。 5. 完成核心原子八位字节,如果需要,形成共价链接在前面的结构中,我们已经完成了外原子的八位字节; 现在我们必须完成内部原子(碳)的八位字节。 为了实现八位字节,碳在其最外层需要 8 个电子。 查看第四步结构时,您可以看到左侧碳已经完成其八位字节,因为它与共享八个电子的四个单键相连。 然而,在碳原子的右侧,只有三个单键,总共有六个电子。 因此,需要另外两个电子来满足对右侧碳的需求。 但是,我们没有任何多余的价电子,因为我们在第四阶段构建中将它们全部用完了。 在这些情况下,孤对将转化为共价键而不会破坏任何原子的八位字节。  我们在不违反任何八位组规则的情况下将一对孤对氧电子转换为共价键,如上述结构所示。 查看上面的结构,我们可以看到我们的右侧碳轻松完成了八位字节,而我们与一对孤对转化为共价键的氧原子同样完成了八位字节。  结果,上述结构中的所有原子都有一个八位字节,我们有我们的 路易斯结构 的 CH3COOH。 6. 质子化乙酸路易斯结构式:在质子化 醋酸,氧原子上存在的孤电子对与质子形成键。 
|
【本文地址】
今日新闻 |
推荐新闻 |