二氧化碳通过与乙烷反应转化为碳纳米管 |
您所在的位置:网站首页 › 碳生成一氧化碳温度 › 二氧化碳通过与乙烷反应转化为碳纳米管 |
二氧化碳通过与乙烷反应转化为碳纳米管
|
二氧化碳通过与乙烷反应转化为碳纳米管
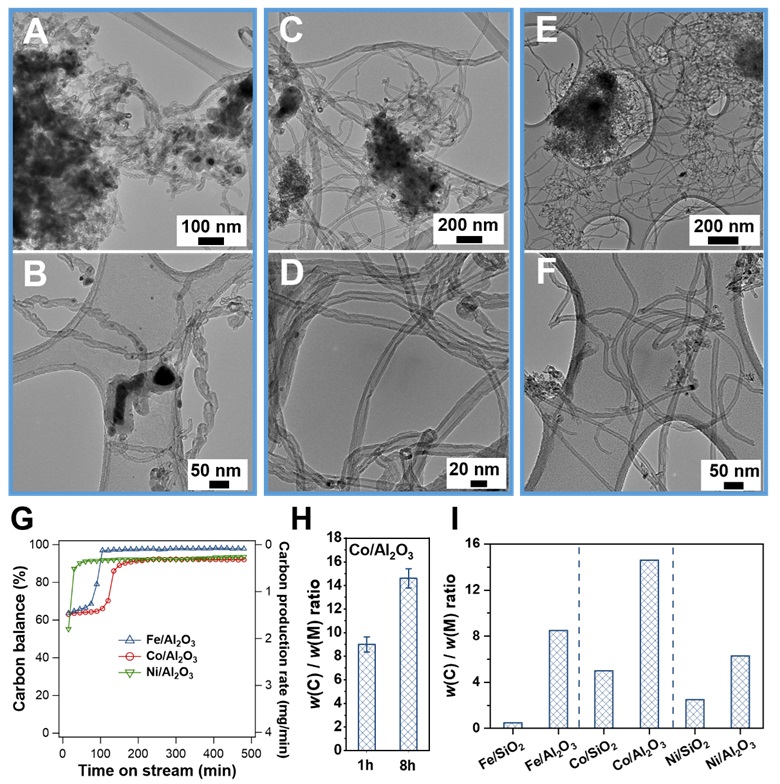
由于大气中二氧化碳浓度增加导致的对气候变化和海洋酸化的不利影响受到越来越广泛的关注。将CO2催化转化为高附加值产品被认为是减少CO2排放的有前景的方法。然而,传统的还原剂H2主要来自化石燃料,其生产过程会伴随CO2的排放,通常会导致CO2净增加。页岩气的持续大量开发提供了丰富的低碳烷烃(主要是甲烷和乙烷),可以作为有效的还原剂,通过与CO2反应为实现净零或净负CO2排放提供了可能。传统的CO2与低碳烷烃的反应主要生成气态(合成气、烯烃)或者液态产品(含氧化合物、芳烃等)。然而,这些产品会被消耗并转化为CO2,最终在几年内重新进入大气。为了提高CO2封存的时间尺度,将CO2和烷烃转化为固体碳是一种有前景的策略。固体碳可以掺杂到例如混凝土中,具有可能超过一个世纪内被封存的优势。 近日,哥伦比亚大学陈经广教授(点击查看介绍)课题组提出了一种有效的方法,利用地球储量比较丰富的金属(Fe、Co、Ni)将CO2通过与乙烷在750 °C下反应转化为碳纳米管(CNT)。研究发现,Al2O3负载的Fe、Co、Ni催化剂均可实现将生成CO2和乙烷转化成CNT(图1A-F),并且CNT的形貌与所用的催化剂有关。Co和Ni基催化剂主要生成直径为20纳米、长度为微米级的CNT(图1C-F),而Fe基催化剂产生的CNT是竹状结构(图1A-B)。同时在化学反应过程中,乙烷和CO2的初始转化率接近100%,气体产品主要包括H2和CO(比例约为1.5),这些气体产物可以通过合成气制甲醇或费托合成技术进一步生成有价值的化学品。CNT的生成速率与理论值接近,高达90mg/h(图1G)。随着反应时间的进行,乙烷和CO2的转化率有所下降,而碳平衡逐渐接近100%,表明CNT的生长在一段时间后停止。总体而言,Co/Al2O3的CNT生成产量高于Fe/Al2O3和Ni/Al2O3(图1I)。此外, Al2O3负载的催化剂比SiO2作为载体表现出更高的固体碳生成量。通过对反应温度以及进料比(CO2:C2H6)进行研究发现较低的温度能够生成更多的固体碳(图2A-D),但由于温度所限,该固体碳主要是碳纳米纤维(CNF)。此外,CO2的存在对固体碳的生成表现出促进作用。在没有CO2的条件下,尽管固体碳迅速生成,然而该过程在30分钟之内失活。随着CO2浓度的增加,初始碳产率在失活之前保持了更长时间(超过100分钟),同时得到了2.7倍的CNT产量(图2E-H)。这一观察表明,CO2的存在促进了固体碳的持续生产。
图1. Al2O3 负载的 Fe、Co、Ni在750 °C 下 通过CO2-C2H6 反应生成CNT。(A-F) 反应后催化剂的 TEM 图。(A、B) Fe/Al2O3,(C、D) Co/Al2O3,(E、F) Ni/Al2O3。(G) 750 °C下 CO2-C2H6反应的碳平衡和碳生成速率。(H) 反应 1 小时和 8 小时后 Co/Al2O3 催化剂的碳与金属比例(w(C)/w(M))。(I) 反应 8 小时后不同催化剂的 w(C)/w(M) 比。
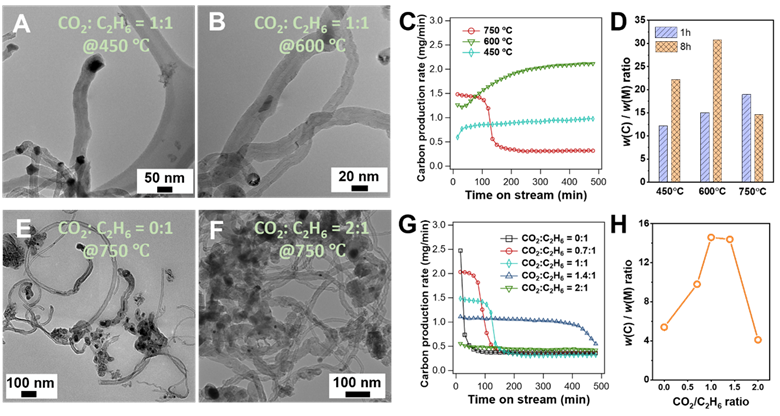
图2. 反应温度和 CO2/C2H6 进料比对 Co/Al2O3上固体碳形成的影响。(A-B) Co/Al2O3催化剂分别在 (A) 450 °C 和 (B) 600 °C 反应后的 TEM 图,(C)碳生成速率,(D) 反应 1 小时和 8 小时后 Co/Al2O3催化剂的重量随反应温度的变化。(E-F) Co/Al2O3 催化剂 (E) 不含 CO2和 (F) CO2/C2H6比率为 2:1 反应后的TEM 图。(G)碳生成速率以及(H) 反应 8 小时后 w(C)/w(M) 比随 CO2/C2H6比的变化。 通过使用同位素标记实验(13CO2和12C2H6)和随后的程序升温氧化(TPO)研究了CNT中固体碳的来源。结果显示,CNT中的碳部分来自CO2的贡献(图3A-B):使用Fe/Al2O3催化剂时,来自CO2的碳占37%,而使用Co/Al2O3和Ni/Al2O3催化剂时分别为28%和24%。因此,CO2在CNT合成中发挥了双重作用:增强催化剂的稳定性并贡献约30%的CNT产量。在反应过程中,一个可能的途径是CO2首先被乙烷还原为一氧化碳,然后存在的一氧化碳通过竞争性吸附减缓了乙烷的分解,并通过Boudouard反应分解产生CNT(图3C)。
图3. 通过使用13CO2同位素进行CO2-C2H6反应,然后进行 TPO 分析,确定 CNT 形成过程中碳的来源。(A) 在 750 °C 下分别使用12CO2-12C2H6和13CO2-13C2H6作为反应物的反应后Fe/Al2O3 催化剂的 TPO 曲线。(B) 在不同催化剂和反应温度下产生的固体碳的碳分布。(C) CO2和 C2H6 反应产生 CNT 的示意图。 此外,原位XRD和原位XAFS实验提供了催化生成CNT的活性位的见解。Fe/Al2O3在750 °C经过H2/Ar还原后生成金属Fe。引入CO2和C2H6后,金属Fe显著转变为Fe3C,表明Fe和Fe3C的混合可能是CNT生成的活性位点。相同条件下,金属Co和Ni在引入反应物后没有进一步变化,明确了金属Co或Ni作为反应的活性中心。 总之,本研究提出的将CO2与乙烷反应转化为CNTs的方法具有环境和经济效益。CO2不仅提高催化剂的寿命,并且直接参与了CNT的合成,同时强调了通过催化剂设计提高CO2固定效率和控制CNT形貌的潜力。这一成果近期发表在Angewandte Chemie International Edition 上,文章的第一作者是布鲁克海文国家实验室博士后袁勇,通讯作者是哥伦比亚大学陈经广教授。 原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):
Converting Carbon Dioxide into Carbon Nanotubes by Reacting with Ethane Yong Yuan, Erwei Huang, Sooyeon Hwang, Ping Liu, Jingguang G. Chen Angew. Chem. Int. Ed., 2024, DOI: 10.1002/anie.202404047 导师介绍 陈经广 https://www.x-mol.com/university/faculty/37845 如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载! 点击分享 收藏 取消收藏 评论: 0 |
【本文地址】
今日新闻 |
推荐新闻 |