《自然》重磅:癌细胞能量来源百年谜团告破!选择能效低的供能方式,竟然是为了转移的更爽 |
您所在的位置:网站首页 › 癌细胞到底是什么样子 › 《自然》重磅:癌细胞能量来源百年谜团告破!选择能效低的供能方式,竟然是为了转移的更爽 |
《自然》重磅:癌细胞能量来源百年谜团告破!选择能效低的供能方式,竟然是为了转移的更爽
|
分子内分泌学之父 1924年,德国生理学家Otto Warburg提出了(比起诺奖)让他留名后世的理论——Warburg效应。他认为,癌细胞之所以生长速度远大于正常细胞,就是因为能量的获取方式不同。一般,正常细胞会选择有氧呼吸的方式供能,而癌细胞却倾向于使用糖酵解。所以癌细胞的线粒体应当与正常细胞有所不同,这种差异应该就是癌症真正的起源。 要知道,同样是一分子葡萄糖,有氧呼吸能够产生36分子ATP,但是糖酵解就只能产生2分子ATP。高达十几倍的能量差距啊,更何况癌细胞疯狂增殖、流窜,这都需要大量的能量。癌细胞为什么要选择这种效率低下的途径? 无疑,这是个反直觉的理论,因此Warburg也“收获”了大量来自同行的口诛笔伐。现在主流研究者一般认为,癌症为突变引起。在恶性转化过程中,基因突变导致表达的变化,进而造成细胞的无节制生长。而代谢选择的变化,只是癌细胞适应实体瘤内缺氧环境的结果而已。 无论真相如何,癌细胞偏爱糖酵解是不争的事实,由此而来的问题就是,糖酵解是否确实对癌症进展有帮助?如果真的有,那么这又是如何实现的呢?
Otto Warburg本瓦 朋友圈包含爱因斯坦等大牛,差点拿了两次诺奖 癌变的两个最大的特征就是代谢和转录的变化,它们又分别与癌症的增殖和转移相关[2],不过这二者之间的关系就有些不那么能说清楚了。而本项研究的发现,说起来还有点意外。 在几年前,O’Malley教授实验室确定了一种转录蛋白在癌症中的作用。这种蛋白名为类固醇受体共激活因子3(SRC-3,也称为NCOA3等),SRC-3是一种重要的基因表达调控因子,能够上调基因的表达,在许多癌细胞中都存在过表达现象[3]。而且对SRC-3进行磷酸化修饰,还能够进一步提升它的转录活性,SRC-3的磷酸化也是许多癌症的生物标志[4]。 为了搞清楚影响SRC-3转录活性的激酶,研究者们开始了大海捞针。他们利用反义RNA对636种人类激酶与SRC-3的相互作用进行了筛选,成功找到了对SRC-3影响最大的一种激酶,PFKFB4。 这可令人惊讶了。PFKFB4固然是一种激酶,却并不是一种蛋白激酶,而是在糖酵解过程中起关键作用的一种果糖激酶!此前可没人知道,这种酶还能作用于蛋白质。
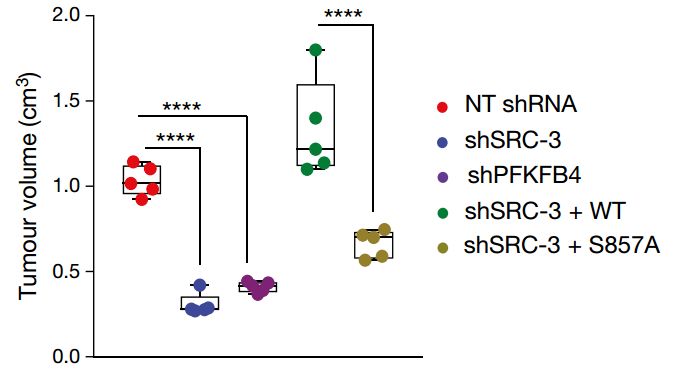
进一步的研究显示,PFKFB4可以在SRC-3蛋白857号位的丝氨酸上添加磷酸基团,从而增加SRC-3的转录活性,促进乳腺癌的增殖和转移。那么反过来想想,限制住这两种蛋白,是不是可以控制癌症发展呢? 研究者设计了一组人源乳腺癌细胞,细胞中能够稳定地表达靶向PFKFB4或SRC-3的短发卡RNA。这就有效地沉默了癌细胞中PFKFB4和SRC-3。 研究者将这种癌细胞移植给小鼠,并持续观察肿瘤组织的生长情况。与对照组小鼠相比,任意一者被沉默的小鼠肿瘤组织发展都明显受到抑制(下图左1、2、3)。如果给SRC-3沉默的小鼠补充正常的SRC-3,那么小鼠的肿瘤生长也会恢复正常(下图左4)。 除此之外,研究者还设计了一种无法被PFKFB4磷酸化的SRC-3(S857A)。利用这种改造的SRC-3替换正常SRC-3也能够一定程度上阻止癌症发展(下图左5)。
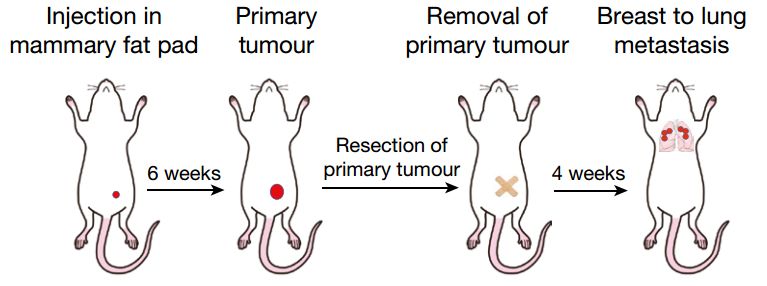
在预防癌症复发转移上,这种方法也起到了良好的效果。 研究者给小鼠植入癌细胞6周后,再为小鼠手术清除原发瘤,并在接下来的4周里持续观察小鼠复发的情况。正常小鼠普遍表现为大规模的肺部的转移复发。
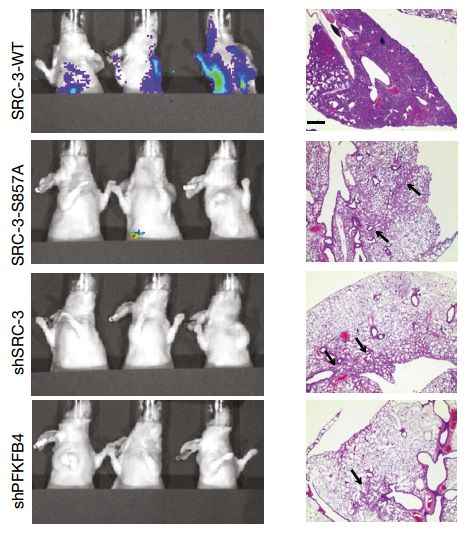
实验流程 但是对于那些植入“改造”癌细胞的小鼠来说,它们的肺部只是发现了几个零星的转移灶,而且在手术之后的四周内并没有出现什么健康问题。 这些结果足以说明PFKFB4—SRC-3通路在乳腺癌增殖和转移过程中的重要作用了。
影像学检查和组织病理学检查 这条新发现的通路在临床上也能够得到一定的验证。研究者对癌症基因组图谱数据库(TCGA)中的数据进行了分析,发现在所有乳腺癌的亚型中,都存在PFKFB4表达增加;而与正常组织相比,肿瘤组织中PFKFB4、SRC3、磷酸化SRC-3水平都有显著的增加,并且与不良预后有关。 现在让我们回到Warburg效应上来。现在我们知道,癌细胞到底为什么选择了看起来吃力不讨好的糖酵解,自然是因为糖酵解途径会协助癌细胞壮大自己咯。去年《自然通讯》也曾发表一项研究,发现糖酵解过程中产生的1,6-二磷酸果糖能够促进RAS基因的超活化[5]。 将近百年前的理论,现在拿出来仍有可探讨之处,奇点糕觉得这也是科学的魅力啊~ 编辑神叨叨 明天休息吗?不休息! 参考资料: [1] https://www.nature.com/articles/s41586-018-0018-1 [2]Ward, P. S. & Thompson, C. B. Metabolic reprogramming: a cancer hallmark even Warburg did not anticipate. Cancer Cell 21, 297–308 (2012). [3] Xu, J., Wu, R. C. & O’Malley, B. W. Normal and cancer-related functions of the p160 steroid receptor co-activator (SRC) family. Nat. Rev. Cancer 9, 615–630(2009). [4] Lonard, D. M. & O’Malley, B. W. The expanding cosmos of nuclear receptor coactivators. Cell 125, 411–414 (2006). [5] https://www.nature.com/articles/s41467-017-01019-z
|
【本文地址】
今日新闻 |
推荐新闻 |

 返回搜狐,查看更多
返回搜狐,查看更多