非洲猪瘟:快速激增还是缓慢而稳定传播? |
您所在的位置:网站首页 › 病原体特征疾病特征传播速度和范围 › 非洲猪瘟:快速激增还是缓慢而稳定传播? |
非洲猪瘟:快速激增还是缓慢而稳定传播?
|
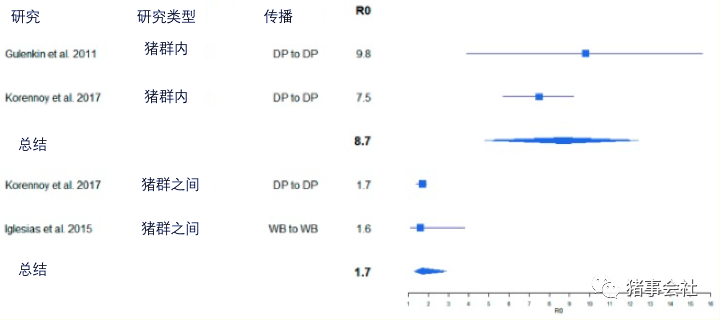
自2007年将ASF引入格鲁吉亚之后,最初假设ASF可能表现为一种自限性疾病(就是疾病在发生发展到一定程度后,靠机体调节能够控制病情发展并逐渐恢复痊愈),并且由于其高死亡率和病死率而迅速消失,或者相反,ASF可能迅速传播。实际情况证明这两种预测都是错误的。目前,非洲以外的至少14个国家受到ASF的影响,其中包括欧盟的几个成员国。2018年8月,在生猪生产和生猪产品消费发挥重要作用的中国,首次报告了猪瘟疫情。两个月后,已经通报了33起疫情。2019年5月,报告了134例ASF暴发,并且在相对较短的时间内,ASF已在全国大面积传播,表明传播速度很快。此外,据推测,通过从中国走私的猪肉,ASF已传播到其他亚洲国家的猪,包括柬埔寨、蒙古、朝鲜、老挝、菲律宾和越南。这种流行病大概在2007年起源于乔治亚州的一个港口,但在全世界范围内仍未得到控制。 迄今为止,许多研究出版物和科学观点将ASF描述为一种高传染性、高死亡率的疾病。然而,最近的研究和受影响国家的病程对ASF是一种高度传染性疾病的观点提出了挑战。ASF的特点似乎是病死率高(即在美国,大多数受感染的动物都会死亡),同时也伴随着低至中等的死亡率(只有一小部分种群会受到感染,至少在野猪中是这样)。 我们的目标是收集和总结关于这些不确定性的已发表的信息,方法是检索关于商业养猪、野猪病例和试验研究数据中ASF暴发的传播率、传播速度和死亡率的文献。 2.ASF及其传播速度 一种疾病的传播及其传播速度是非常复杂的。它取决于许多不同的特性。它们不仅包括病原体的特征,还包括宿主的特征,即易感猪或野猪种群的特征,以及环境的特征。我们回顾了与ASF传播相关的流行病学术语的不同定义和描述,并对其中一些定义进行了改进。因此,我们的目标是确保对提出的术语有统一的理解。在这个过程中,我们将术语的数量减少到那些可能被认为对描述或解释ASF的传播速度至关重要的术语。更多一般性术语的定义载于补充文件S1。 2.1基本繁殖数(R0) 基本生殖数R0是疾病在畜群中传播能力的量度。它被定义为一个传染病个体在整个感染期间在一个完全易感畜群中所引起的继发病例的平均数量,是一种流行病的重要定量特征。如果R0的值小于1,则表明该疾病将从种群中消失,而值大于1则表明该疾病将在种群中持续存在或扩散。R0的计算方法是确定传播概率、平均接触人数和感染持续时间的乘积。R0的计算是基于种群中均匀混合的假设,即种群中所有动物的接触次数都是相同的。Cross等人指出,R0可能是一个较差的病程预测因子,而其他因素,如群体内传播或群体规模,对预测病原体的传播同样重要。 2.2 ASF爆发情况下的R0 如前所述,R0高度依赖于多种因素。例如,这取决于感染宿主的传染性,即感染的持续时间,患病动物周围易感个体的数量以及正在传播的ASF病毒(ASFV)株或分离株的毒力。 最早发表的一项研究根据俄罗斯联邦暴发的现场数据对ASF的R0进行了估计,导致猪场中ASF感染的R0值相对较高(8-11)。在同一研究中确定的农场之间传播的R0较低(2-3)。在几个田间和试验研究也获得了相似的值,从而农场之间R0传输的值低于农场内传播(图1)。在间接传播的情况下,R0值也同样适用(图2)。相比之下,在一项试验传输研究中确定了一个非常高的R0 (18.0)。然而,该估计值的置信区间很宽(6.90-46.9)(图2),这可能是由于可以包含在这种试验环境中的试验动物数量有限。
图1 从ASF试验研究获得的非洲猪瘟(ASF)计算R 0计算值的变化。方框表示计算出的R。这些线表示置信区间。DP =家猪,WB =野猪
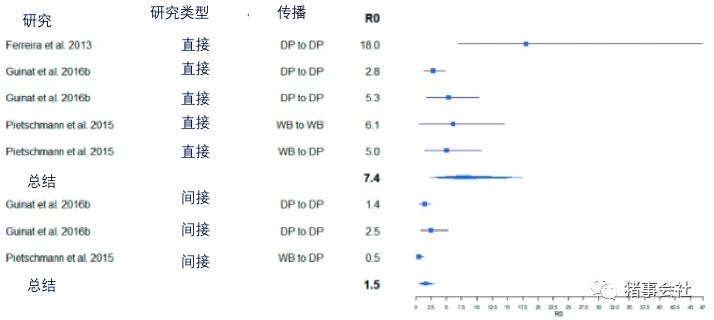
图2 从ASF试验研究获得的非洲猪瘟(ASF)计算R0计算值的变化。方框表示计算出的R。这些线表示置信区间。DP =家猪,WB =野猪 对已发表的研究结果的总结分析表明,到目前为止,文献中描述的ASF 的R0的点估计值覆盖了0.5到18.0的较宽范围。这种宽泛的变化尤其可能取决于不同病毒分离株的特性(例如毒力和传染性),而且取决于用于确定R0的方法,而这些方法差异很大。但是,无论研究设置(田间或试验)如何,在畜群/直接传播研究中计算出的R0值似乎具有可比性。同样,在畜群/间接传播之间的R0计算得出相似的值(图1和图2)。这些结果表明,尽管使用了不同的方法和材料,但该分析中包括的研究仍获得了相当合理的ASF的R0值。不幸的是,我们无法调查发表偏倚是否可能影响了该分析的结果,大多数现有的原始出版物没有包含关于研究规模所需的原始数据。 将ASF的R0值与其他猪疾病的R0值进行比较,发现计算口蹄疫的R0值的研究显示其R0值往往大于20(由于口蹄疫被认为是高传染性疾病)。经典型猪瘟也被描述为一种高度传染性的疾病。在几项研究中,R0值与ASF值相似。与ASF中一样,舍内感染和舍间感染之间的值也不同。在Klinkenberg等人的研究中,断奶仔猪舍内R0高达100(95%置信区间(CI)54.4–186)。但是,对于这两种疾病,R0高度依赖于其他几个因素,例如研究设计、病毒株等。 2.3 时空分布与疾病传播 疾病传播和传播的特征不能脱离时空邻近而独立观察。如果处于危险中的个体彼此住得很近,与相隔很远的情况相比,传播的可能性更大。通常仅使用地图可视化空间分布。然而,有几种分析工具,如空间聚类检测或时空建模,其可被用于包括声音时空分析成流行病学调查。一些研究发表描述使用不同的模型来研究动物疾病的时空趋势。此外,模拟模型被广泛用于描述动物疾病的时空传播。它们还可用于分析地方病和流行病的模式或评价控制措施的成功与否。 2.4 ASF的时空分布和传播 在本节中,我们试图总结主要关注ASF传播速度的出版物的结果。传播速度很大程度上取决于已经讨论或将在后面讨论的几个因素。因此,一些关于ASF传播速度或传播速率的研究被纳入了以上或以下的讨论。 Fekede等人对野猪种群中ASF的空间传播进行了建模,表明温度低于0°C的季节有助于ASF的发生,因此也有助于疾病的传播。在其它几项研究中,ASF阳性的野猪在冬季的检出也有所增加。与野猪不同的是,多数家猪ASF的爆发主要发生在夏季。 ASF在波兰野猪种群中的空间传播被认为是缓慢的。Podgorski等人假设,这种缓慢的传播可能是由于野猪之间接触的空间限制。在对俄罗斯野猪中ASF病例的聚类分析中,Iglesias等人发现,单个野猪病例在方圆130.79公里内,最多在90天内存在空间关联。观察到的传播方式是通过直接和间接野猪接触来解释的,但也可能是由于狩猎增加导致被感染野猪的潜在传播所致。Sardinia等人的一项类似研究发现,假定每天移动距离为2-10公里的野猪中,ASF病例之间的最大空间关联为25公里。在同一研究中,生猪养殖场ASF通知的空间关联最大距离为15 km。在模拟模型研究中,畜群之间的传播距离估计低于10 km。但是,在俄罗斯联邦,Korennoy等人计算了两次相关的家养猪疫情之间的平均距离为156公里,平均时间为7.5天。按照俄罗斯兽医当局的声明,Blome等人在2011年就已经报道了ASF每年在俄罗斯联邦内的传播速度为350公里。这些结果表明该疾病迅速传播。然而,在Ošvskis等的研究中,描述了ASFV在受感染猪群中的缓慢传播。此外,Nurmoja等报道了在受影响的猪群中传播较慢,表明其传染性相对较低。 以下术语的通用术语可以在补充文件S1中找到。 2.5 ASF疫情中的发病率 发病率可以用来描述ASF的传播速度。在一定时期内的高发病率需要一定程度的传染性和较高的毒力。因此,我们假设一种高发病率的疾病很可能在目标猪群中快速传播。 由于ASF的病死率高,预计其发病率与死亡率相当。低毒力或中等毒力的病原体感染很可能导致较高的发病率,但死亡率较低。因此,高的发病率在试验研究中,这也表现出了高死亡率。然而,在少数研究中,感染后出现临床症状的动物完全康复,因此发病率高于观察到的死亡率。 2.6 ASF的死亡率和病死率 死亡率和病死率是提供有关传播的ASF病毒和疾病动态信息的参数。但是,在解释研究结果时,应牢记两个术语经常被混淆或被错误地用作同义词。 ASF的迅速传播并不一定取决于高病死率,因为后者仅指患病动物中死亡病例的比例。同样,高死亡率与ASF的快速传播并没有必然的联系。相反,高死亡率定义了处于危险中的整个种群中死亡动物的比例。因此,这两个术语都应该在其他参数的背景下考虑,例如宿主相关的因素(例如,年龄)和药剂的属性(例如,循环菌株的毒性)。最近的研究表明,在老年猪和感染低毒性毒株的动物中,ASF的死亡率较低。Blome等人描述了ASFV的死亡率在3%到100%之间,这取决于病毒株的毒性。Mebus发现了不同水平的ASFV分离物的毒力和相应的死亡率(从小于20%到100%)。一项用几种中等毒性的ASFV分离株进行的试验导致了几乎所有使用的菌株的中等死亡率。只有巴西的78分离株,尽管被描述为中等毒性,却杀死了所有受感染的猪,也就是说,在这个试验中,它造成了100%的死亡率。Vlasova等研究也证实了死亡率取决于特定ASFV毒株或分离株的毒性。 最早描述ASF的Montgomery研究发现,无论是ASF暴发和试验性感染,ASF的死亡率都很高。 在假设ASF通常具有极高的死亡率的前提下,已提出对猪死亡率进行综合监测是在国内养猪场中对ASF进行监测的最合适方法。在Gallardo等人的试验中,当家猪接种ASFV立陶宛2014基因型II田间分离菌株时,死亡率和病死率均达到94.5%的高值。Pietschmann等使用另一种基因型II分离株,观察到野猪(感染后17天之内)和家猪(感染后36天之内)的100%死亡率。试验暴露于高毒性的高加索ASF分离物(2008年从亚美尼亚分离)导致100%的死亡率。在这项研究中,野猪之间的传播比家猪之间的传播更快。在随后的研究中,Blome等人还发现被ASFV高加索分离株感染的野猪死亡率为100%。Guinat等在使用家猪的试验中,使用相同的隔离株,获得了100%的死亡率。在这里回顾的大多数试验研究也在欧洲食品安全局的科学观点中进行了总结。 与试验感染的结果相似,在现场研究中发现ASF的死亡率很高。1978年在马耳他爆发的ASF疫情表明该病传播迅速,死亡率很高。这种流行病导致马耳他猪只损失了三分之二。最终决定屠杀岛上所有剩余的猪。该分离株(Malta/78)的高毒力在试验研究中得到证实,致死率为93.3%。 当分析2001年尼日利亚ASF暴发的数据时,很明显这种疾病传播得非常快。虽然猪的死亡率因年龄而异,但各年龄组的死亡率均不低于75.9%。在2003年和2004年坦桑尼亚暴发的疫情中,死亡率分别为82%和72% 。 2014年,爱沙尼亚出现了首例野猪ASF病例。爱沙尼亚南部的野猪死亡率较高,而该国东北部的死亡率较低。然而,为了确定在该国东北部传播的毒株的毒力,进行了试验性感染,结果表明该分离株的死亡率仍然很高,因为在10只接种的野猪中有9例死于ASF感染或生病,以致于他们必须被安乐死。 最近的研究结果表明,由于死亡率的增加,可能需要长达一个月的时间才能在猪群中检测到ASF的引入,从而表明目前在各自区域内流行的ASFV毒株的死亡率中等,在本例中为俄罗斯联邦。已经观察到ASF流行期间的低死亡率;Ekue等人使用喀麦隆的一种ASF分离物进行动物试验,发现其死亡率非常低。分析马拉维ASF暴发的研究表明,大多数地区的死亡率明显低于100%。 在1985年比利时发生的疫情中,ASF的传播被认为是缓慢的,不仅是从一个猪圈传播到另一个猪圈,甚至在同一猪圈内也是如此。此外,循环的ASF分离株或毒株的死亡率明显中等。 当总结关于死亡率的文献搜索结果时,似乎很明显,描述循环的ASFV分离株或菌株的高死亡率的研究占主导地位。很明显,死亡率高度依赖于传播的病毒分离株或毒株的毒力。此外,与大多数病原体相似,受影响的宿主物种的特性(特别是年龄以及健康和摄食条件)似乎也起着重要作用。因此,ASF暴发通常(但并非总是)以高死亡率为特征。 2.7 ASF的传染性和潜伏期 在ASF的特定条件下,传染性是指受感染动物可以传播疾病的时间。这个时期持续的时间越长,传播的风险越高,因此,ASF传播的风险也相应增加。传染期在很大程度上取决于病毒株或分离株。这可以一项广泛的传播研究中得到证明,其中确定ASF的最低感染期为6-7天,而最大感染期为20到40天。研究还表明,传染性还取决于传播速率和途径。在较早的研究中,作者通过聚合酶链反应(PCR)在血液和口咽液中检测到ASFV基因组,直到感染后70天,即观察期结束。另外,传染性是由动物排出的病原体的数量来定义的。一些研究表明,血液中的ASFV含量明显高于其他分泌物。 由ASF感染引起的出血性腹泻的猪的传染性要高于单纯发热或食欲不振的猪。这种差异可能是由于ASF在受感染动物的血液中传播极为有效。在Guinat等人在家猪和野猪中开展的几次传播研究中,感染期持续2至14天,而ASFV的潜伏期为被发现是3–6天。Guinat等人也获得了类似的结果,其中感染期从4.5到8.3天不等,潜伏期从5.8到9.7天不等。在Gulenkin等人的研究中的潜伏期为15天。估计结果的差异可能是由于试验设计的差异、ASF病毒分离株或毒株的不同性质以及这些研究中使用的猪或野猪。 从传染性与传播速度的关系来看,关于潜在的ASFV携带者的讨论不容忽视。Sanchez-Vizcaino等人指出,动物可能会发展成慢性形式的ASF,并成为甚至长时间后仍能感染同种异体的携带者。Gallardo等人的研究显示,与感染猪接触过的一头猪在感染后幸存了下来,目前尚不清楚这种动物是否患有传播ASF的潜力。但是,在其他研究中,观察到存活动物和接触动物未发生疾病传播,这表明存活者在ASF传播中的作用微不足道。 就传播速度而言,不仅传染期的长短很重要,潜伏期和潜伏期的长短也很重要。当传播可以在任何临床症状发生之前发生,即在潜伏期和传染期重叠且潜伏期因此短于潜伏期的时间内,疾病传播可能会更快,因为不太可能在此期间内采取了控制措施。但是,这仅适用于家猪,因为很难观察到野猪的临床症状的发作,尤其是在ASF最初进入野猪种群之后。 2.8猪瘟病毒的传染性 ASFV的感染性通常以组织培养物(TCID50)中50%致死剂量(LD50)的量度,在确定ASF传播速度方面也起着重要作用。 可以假定,传染性低的病毒比传染性高的病菌传播速度慢。但是,ASFV的传染性高度依赖于病毒分离株或病毒株的特性(尤其是其毒力)和介质(血液、尿液、其他体液、粪便、组织等)的毒性,以及这种物质任何潜在的加工方法(温度、pH、保存期限等)和传播途径。如前所述,通过直接接触血液传输是最有效的途径。Olesen等人研究,ASFV在研究的猪舍环境中的传染性较低。相应地,与直接接触受感染动物的血液相比,通过尿液、粪便或饲料等其它污染物传播的效果较差。然而,在出血性肠炎的病例中,粪便在ASF的传播中起着重要的作用。这些假设得到了几项研究的支持,这些研究发现血液中的PCR效价高于其他排泄物。与其他排泄物(特别是粪便和尿液)或被ASFV污染的土壤相比,未受感染的猪与另一头猪的血液直接接触的可能性较小。因此,ASF的传播可能比环境中存在大量传染性病毒的疾病传播要慢。 2.9 ASF的接触传染性 关于ASF的接触传染性,在文献中没有发现可以增加已经描述的关于传染性的知识的信息。 2.10 ASFV的毒力 毒力如同感染力一样是病原体的一种特性。中等或低毒力的病毒仍具有高度感染性。不同传播途径的有效性也可能受到病毒株或病毒分离物毒性的影响。当使用高毒性的ASFV毒株时,发现ASF的传播更有效。McVicar发现,感染了高毒性ASFV毒株的猪,其口腔体液中的病毒量要高于感染了低毒株的猪。因此,循环的ASFV毒株的毒力对ASF的传播和传播速度有影响。相比之下,Guinat等总结了几项研究结果发现,不管用于感染猪的分离病毒株的毒力如何,不同体液中的病毒载量都非常相似。 根据病毒株或分离株的毒力,感染ASFV只能导致轻微的临床症状或100%的死亡率或介于两者之间的任何差异。 表1 非洲猪瘟(ASF)的毒株和分离株、毒力、田间感染和试验感染的病程 ASFV株系或隔离株 毒力 病程 田间感染 试验性感染/感染途径 马耳他分离株(Malta / 78) 中/高 该病毒在国内猪群中迅速传播,导致马耳他在一年内宰杀了所有的猪 少于50%的感染猪出现轻微的临床症状,高死亡率/与受感染的供体猪接触 巴西78 低/中 随着时间的推移,家猪的临床病程较轻,死亡率降低。在整个巴西至少有八年的时间广泛分布 高死亡率/鼻内 荷兰'86 中等 找不到信息 低死亡率与相当亚临床病程/口腔和通过接触 乔治亚2007/1 高 大规模流行病,野猪和家猪都受到影响 临床症状温和,死亡率高/肌内 爱沙尼亚15 / WB,塔尔图-14 高 在野猪种群中迅速传播 试验感染的家猪100%死亡。两名与猪有接触的幸存猪/肌内 爱沙尼亚爱达维鲁 高 仅在本地野猪种群中传播 几乎100%的死亡率(一名幸存者)/口鼻 亚美尼亚'08 高 找不到信息 野猪和家猪死亡率为100%/ 口鼻的 表1中的例子说明了几种与毒力有关的参数的复杂性和潜在的相互依赖性,以及不同的ASFV分离株或菌株的田间和试验感染过程。在比较现有结果时,不应忽视不同的感染途径(表1)。然而,无论循环毒株的毒力如何,ASF在野猪中的传播过程可能会持续较长时间。在巴西,在家猪中传播的病毒株被认为是低毒性的,消灭这种疾病花了几年的时间。在这种情况下,疫情蔓延到整个国家,也影响了几个邻国。 2.11 ASFV对环境因素的韧性或抵抗力 多项研究表明,ASFV能够抵抗极端恶劣的环境条件,因此可以在各种基质中长时间保持感染性。例如,在冻肉中,ASFV在低温下的韧性特别高,在冻肉中,该病毒可在数年内保持传染性。即使在室温下,病毒的传染性也能保持数月之久。Dee等人发现,ASFV在不同的饲料和饲料成分中,例如在潮湿的狗粮和猫食中,几天内都具有传染性。众所周知,ASFV可以在腐败中存活。Mebus等人发现ASFV在pH值范围内的抗性在4到13之间。 3.讨论 我们的发现强调了定义传播速度及其相关参数的困难。这不仅是因为可能影响传播速度的参数的不同定义,而且还可能与许多参数对介质的(其他)属性以及与宿主或环境有关的属性之间的相互依赖性有关。当前审查的另一个缺点是,有关指定参数的研究相对较少,甚至很少重复。 病毒分离株和毒株的不同特性、以及宿主因素、环境参数和基质效应的特性很难彼此分离。属性通常容易相互影响,并且如果比较不同的研究,则有时所研究参数的定义会冲突。此外,在不同的研究中,某些术语似乎没有明确定义或以各种有时混淆的方式使用。这主要是指死亡率和病死率之比,但也可能影响毒力、传染性和传染性。关于死亡率和病死率,可能难以确定易感猪群的规模,特别是在野猪中,即使将其定义为生活在某一地区或属于某一群野猪的种群。基于这些参数,通常很难得出有关ASF传播真实速度的可靠结论。 根据ASFV毒株的不同,感染很快导致100%的死亡率,表明在不同的流行病学单位内迅速传播。尽管用于试验感染的ASFV分离株具有高毒力,并观察到相应的高死亡率,但目前在东欧和中欧的ASF病程表明,随着时间的推移,野猪种群的传播相当缓慢。ASFV在血液中含量最大,通过接触受感染动物的血液直接传播是最有效的感染方式。然而,在感染的猪或野猪的和环境中的其他体液中,感染性病毒的量要低得多。由于直接接触受感染动物的血液比接触环境中的其他体液或受污染物质的可能性小,因此可以降低发病率,从而也会降低ASF的传播速度。然而,这可能解释了试验环境和野外环境之间死亡率的差异,因为在试验环境中比在野外环境中更可能直接接触血液。到现在为止,慢性感染动物的野猪ASF的传播中的作用是高度争议。如果从ASF中恢复过来的动物仍然能够传播这种疾病,那么这肯定会影响ASF的传播及其速度。 另一个关于该领域传播缓慢的潜在假设可能是在该地区传播的ASFV的毒力相对较低。然而,在东欧和中欧,使用该地区流通的毒株的试验研究结果并不支持这一假设,这表明该ASFV毒株的毒性很高。 此外,令人费解的是,ASF并没有自我限制,特别是鉴于上述传播中的缺陷。一些研究表明,ASFV在各种组织中具有较长时间的感染性。因此,可以假定传染性ASFV的存在代表了未感染动物接触的风险,并且即使在任何给定时间点暴露的风险相对较低,这种风险也可能随着时间的推移而累积。相应地,ASFV的韧性似乎在ASF的传播中起着重要的作用。 在野猪数量在大片地区受到严重影响的国家,这种疾病经常不断蔓延,导致野猪数量显著减少。因此,值得注意的是,除了本综述中列出的因素外,还有一些其他因素影响着ASF的传播速度。几项研究提到了野猪的种群密度,商业养猪场附近受感染野猪的密度,以及作为ASF更快传播的危险因素的一个确定区域的养猪场密度。然而,人口密度对ASF传播的影响仍然存在争议,目前还没有确定人口密度阈值来阻止ASF的传播。 另外,野猪的行为和生活习惯阻碍了传播速度的计算或估计。野猪通常生活在一个群体中,群体之间有规律的互动,但不同群体之间没有互动。尽管Pfeiffer等人指出,当许多动物紧密生活在一起时,传播的可能性更大,目前关于野猪的行为方面的知识必须被纳入任何评估ASF疾病传播。 在讨论ASF的传输速度时,必须考虑不同的传输周期。感染猪血是ASF最主要的传播媒介。这一事实影响到每一个传播周期。 无论是在畜群内部还是在畜群之间,以动物运动模式形式出现的驯养周期是ASF在驯养猪中传播的主要原因。这一事实和其他事实反过来表明,生物安全措施可以限制ASF的传播。较高的生物安全标准可以减缓甚至阻止ASF的传播,这一假设得到了后院农场中少于50头猪的ASF暴发数量的增加以及通常较低的生物安全措施的支持。因此,可以认为ASF在拥有大量小型私人养猪的国家传播得更快,正如目前在罗马尼亚可以看到的那样。然而,爱沙尼亚的研究人员可以证明,生物安全水平对ASF的引入风险没有可测量的影响。另外,在中国,猪场规模大小似乎对ASF的传播速度没有重大影响。近年来,中国在后院养猪场的数量明显下降。尽管在农村地区养猪的家庭不超过20%,已经观察到ASF在全国范围内迅速蔓延。 钝缘蜱属的软蜱虫在ASF的传播中也起着重要的作用。无疑是这种情况在蜱虫-猪周期和ASF的自然森林型周期在南部非洲疣猪,但也可能是相关的其他地区,如果钝缘蜱存在,必须将这些蜱虫向量可以影响ASF的速度传播。然而,目前没有证据表明蜱在欧洲的ASF传播周期中起作用 最后,正如引言中提到的,最重要的是要强调,人类行为无疑是促进ASF长距离传播的最重要因素。在拥有大量私人后院养猪场的国家中,报告疫情暴发或疑似病例失败可支持ASF的传播,在最坏的情况下,甚至可以通过出售病猪来规避发现ASF后养猪人所期望的问题。考虑到2017年捷克和2018年比利时将ASF引入野猪时,人为因素的影响也变得明显。在这些国家受到影响之前,最近的ASF爆发已在数百公里之外。因此,类似于2001年英格兰的口蹄疫流行,疾病暴发的空间格局通常不仅可以通过距离相关的传播来解释,即通过彼此紧邻的受感染动物,而且还可以通过长距离运输受感染的动物或受污染的物质来解释。显而易见的是,在通过距离无关的机制引入ASFV的情况下,例如在各种人类活动过程中传染性物质的运输,在本文中所讨论的参数不起作用或仅起很小的作用。 4.结论 在现有文献的基础上,我们建议修改ASF通常被称为高传染性疾病的观点。我们试图表明,回答这篇综述提出的问题并不总是容易的,因为答案可能取决于几个流行病学参数。ASF一般既不快也不猛,也不慢也不稳,但ASF的外观可以多种多样。ASFV毒株的毒力各不相同。然而,高毒品系或分离株,也就是目前在东欧和中欧流行、最近被引入中国的品系或分离株,可能具有低发病率的特点,这可能是由于通过病毒载量相对较低的材料传播,导致野猪种群传播缓慢。长距离的ASF跳跃通常是人类活动的结果,因此是不可预测的。 参考文献: 1. Depner, K.; Staubach, C.; Probst, C.; Globig, A.; Blome, S.; Dietze, K.; Sauter-Luis, C.; Conraths, F.J. African Swine fever-epidemiological considerations and consequences for disease control. Tieraerztl. Umschau 2016, 71, 72–78. 2. Ol, ševskis, E.; Guberti, V.; Serzants, M.; Westergaard, J.; Gallardo, C.; Rodze, I.; Depner, K. African swine fever virus introduction into the EU in 2014: Experience of Latvia. Res. Vet. Sci. 2016, 105, 28–30. ...... 100.Vergne,T.; Gogin,A.;Pfei↵er,D.U.StatisticalExplorationofLocalTransmissionRoutesforAfricanSwine Fever in Pigs in the Russian Federation, 2007-2014. Transbound. Emerg. Dis. 2017,64, 504–512. 101.Mur, L.; Martinez-Lopez, B.; Sanchez-Vizcaino, J.M. Risk of African swine fever introduction into the European Union through transport-associated routes: Returning trucks and waste from international ships and planes. BMC Vet. Res. 2012, 8. 返回搜狐,查看更多 |
【本文地址】
今日新闻 |
推荐新闻 |