PLOS Pathog︱四川大学华西医院傅湘辉/田艳团队报道新冠防治潜在药物:拓扑替康和小檗胺靶向RG4,抑制新冠病毒感染 |
您所在的位置:网站首页 › 湘仁医院 › PLOS Pathog︱四川大学华西医院傅湘辉/田艳团队报道新冠防治潜在药物:拓扑替康和小檗胺靶向RG4,抑制新冠病毒感染 |
PLOS Pathog︱四川大学华西医院傅湘辉/田艳团队报道新冠防治潜在药物:拓扑替康和小檗胺靶向RG4,抑制新冠病毒感染
 撰文︱童麒羽,刘 更 责编︱王思珍,方以一 编辑︱杨彬薇 新型冠状病毒感染(Corona Virus Disease 2019,COVID-19)全球持续性大流行严重损害世界公共卫生安全和社会经济发展。针对新型冠状病毒(Severe Acute Respiratory Syndrome Coronavirus 2,SARS-CoV-2),目前已有多款疫苗及抗病毒药物上市,在疫情阻击战中发挥了重要作用。值得指出的是,新型冠状病毒基因组的突变和进化速度极快,容易产生免疫逃逸和药物耐受,可能影响现有疫苗和药物的有效性。因此,寻找更加广谱性的新冠病毒防治策略具有重要意义。 RNA-G四链体(RNA G-quadruplex,RG4)是由富含串联重复鸟嘌呤碱基(Guanine,G)核苷酸链组成的RNA高级结构,在哺乳动物和病毒基因组中广泛存在,可通过调控RNA剪切、转运和翻译等过程调节基因表达,参与疾病发生发展[1]。已有研究发现:SARS-CoV-2感染关键宿主因子TMPRSS2的RG4结构能够显著抑制其蛋白表达,阻碍SARS-CoV-2感染进程[2];SARS-CoV-2基因组RNA也富含RG4结构,从而影响多个病毒结构和非结构蛋白的表达,调控病毒在宿主细胞体内的生物学进程[3],提示RG4是广谱性抗新冠药物的潜在新靶点。截止目前,基于RG4的抗SARS-CoV-2临床药物尚无报道。 四川大学华西医院生物治疗国家重点实验室的傅湘辉教授/田艳副研究员团队长期聚焦人类重大疾病致病新机制和新靶点发现,其前期研究揭示RG4抑制宿主因子TMPRSS2翻译及新型冠状病毒感染[2]。基于“病毒与宿主共靶向、多靶点”防治新冠感染的构想,该团队进一步拓展了RG4对其他宿主因子表达的调节作用,并筛选鉴定了新型RG4靶向药物,为COVID-19防治提供潜在临床用药, 近日在PLoS Pathogens上发表了题为“Targeting RNA G-quadruplex with repurposed drugs blocks SARS-CoV-2 entry”的研究。该研究发现RG4抑制ACE2、AXL、FURIN等宿主因子表达,并基于药物再利用策略,筛选获得了2个临床药物【拓扑替康(Topotecan,TPT)、小檗胺(Berbamine,BBM)】是RG4的新型稳定剂,可在细胞和动物水平阻碍SARS-CoV-2感染,为COVID-19防治提供了新的广谱性抗病毒策略。(拓展阅读:傅湘辉课题组相关研究进展,详见“岚翰生命科学”报道(点击阅读):Nat Commun︱傅湘辉团队发现RG4有望成为新冠防治新靶点  研究团队首先通过生物信息学对影响SARS-CoV-2感染的关键宿主因子进行RG4结构预测,发现ACE2、AXL、DPP4、FURIN、GOLGA7、ZDHHC5等mRNA宿主因子中均富含RG4位点(图1);通过圆二色谱、荧光光谱等实验,证实其中ACE2、AXL、FURIN能够形成RG4结构(图1),结合团队此前在TMPRSS2中发现的RG4结构,提示了RG4在SARS-CoV-2宿主因子中广泛分布。 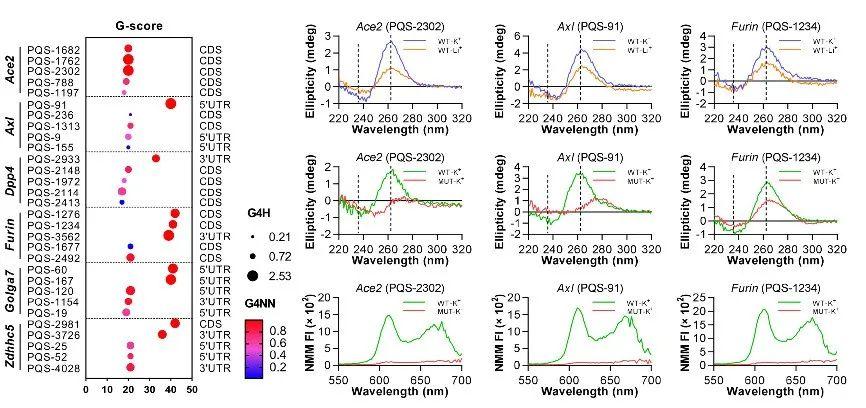 图1. RG4在SARS-CoV-2宿主因子中广泛分布(图源:Qiyu Tong, et al., PLoS Pathog, 2023) 图1. RG4在SARS-CoV-2宿主因子中广泛分布(图源:Qiyu Tong, et al., PLoS Pathog, 2023)基于RG4在SARS-CoV-2基因组和关键宿主因子中普遍存在,以及RG4对基因表达的抑制作用,研究团队采用药物再利用策略,在G-四链体稳定剂化合物库中筛选出5个批准进入临床并且无严重心肺毒性的化合物。进一步通过计算机分子对接,获得2个能够与经典RG4结构结合的G-四链体稳定剂TPT和BBM(图2),并通过微量热涌动实验,在分子水平证实了TPT和BBM能够与宿主因子mRNA的RG4结构稳定结合(图2),提示TPT和BBM可能具有调控SARS-CoV-2宿主因子表达的作用。 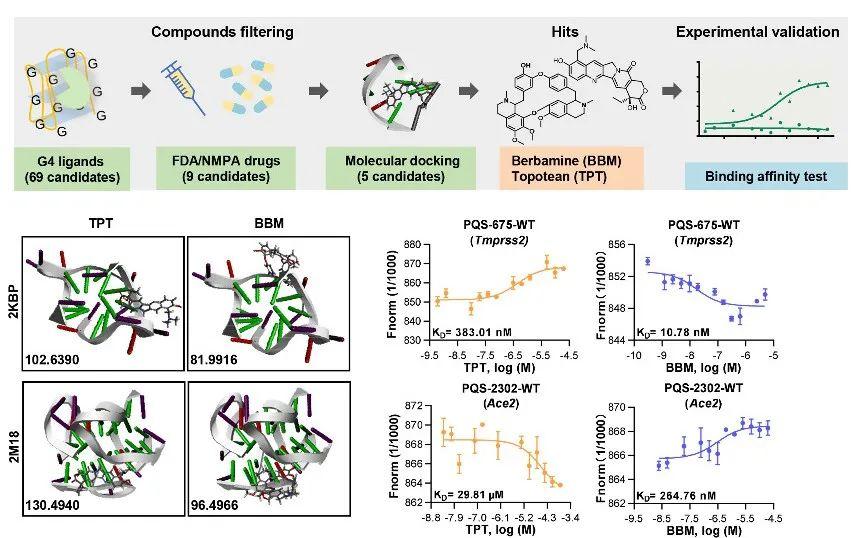 图2. 药物筛选获得宿主因子RG4稳定剂TPT和BBM(图源:Qiyu Tong,et al.,PLoS Pathog, 2023) 图2. 药物筛选获得宿主因子RG4稳定剂TPT和BBM(图源:Qiyu Tong,et al.,PLoS Pathog, 2023)为明确TPT和BBM对宿主因子蛋白表达的调控作用,研究团队在新冠易感细胞H1299中外源性表达了ACE2、AXL、FURIN、TMPRSS2等多种宿主因子,发现TPT和BBM显著抑制宿主因子蛋白表达;突变RG4结构形成关键位点显著促进相应宿主因子蛋白表达,同时导致TPT和BBM的抑制作用失效(图3)。此外,TPT、BBM处理SARS-CoV-2易感细胞H1299、Vero‑E6均显著下调内源性ACE2、AXL、FURIN、TMPRSS2的表达(图3)。上述研究证实TPT和BBM能够通过稳定RG4结构,抑制关键宿主因子表达,提示其抵抗SARS‑COV‑2感染的潜在作用。 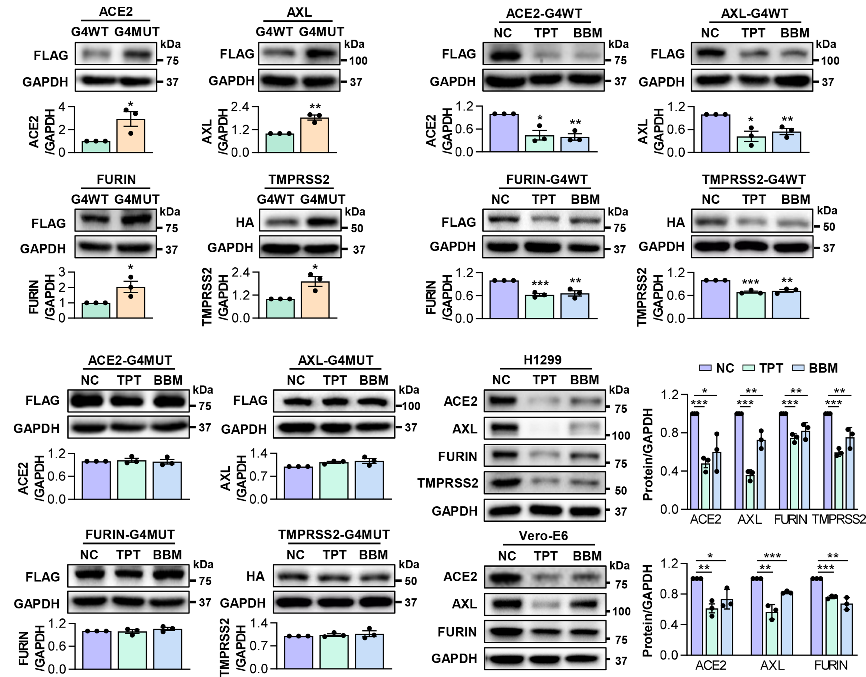 图3. TPT和BBM抑制SARS-CoV-2宿主因子表达(图源:Qiyu Tong,et al.,PLoS Pathog, 2023) 图3. TPT和BBM抑制SARS-CoV-2宿主因子表达(图源:Qiyu Tong,et al.,PLoS Pathog, 2023)最后,研究团队利用SARS-CoV-2假病毒系统分别在细胞和动物水平检测了TPT、BBM对SARS-CoV-2感染的调控作用。研究发现,TPT和BBM显著抑制SARS-CoV-2原始株、突变株P.1和突变株B.1.617.2感染宿主细胞,并在低浓度时表现出比PDS(RG4经典稳定剂)更高的病毒感染抑制效率(图4)。此外,在SARS-CoV-2易感细胞中过表达ACE2、AXL、FURIN和TMPRSS2显著促进SARS-CoV-2感染宿主细胞,TPT和BBM处理能够阻碍其感染;而破坏宿主因子中RG4结构显著抑制了TPT和BBM对病毒感染的调控作用(图4)。在动物水平,研究团队利用AAV9-hACE2构建了SARS-CoV-2易感小鼠模型,同时连续腹腔注射给予TPT和BBM治疗。结果显示TTP、BBM显著抑制病毒感染小鼠肺部,并伴随着AXL、FURIN和TMPRSS2等蛋白在肺组织的表达下降(图4)。 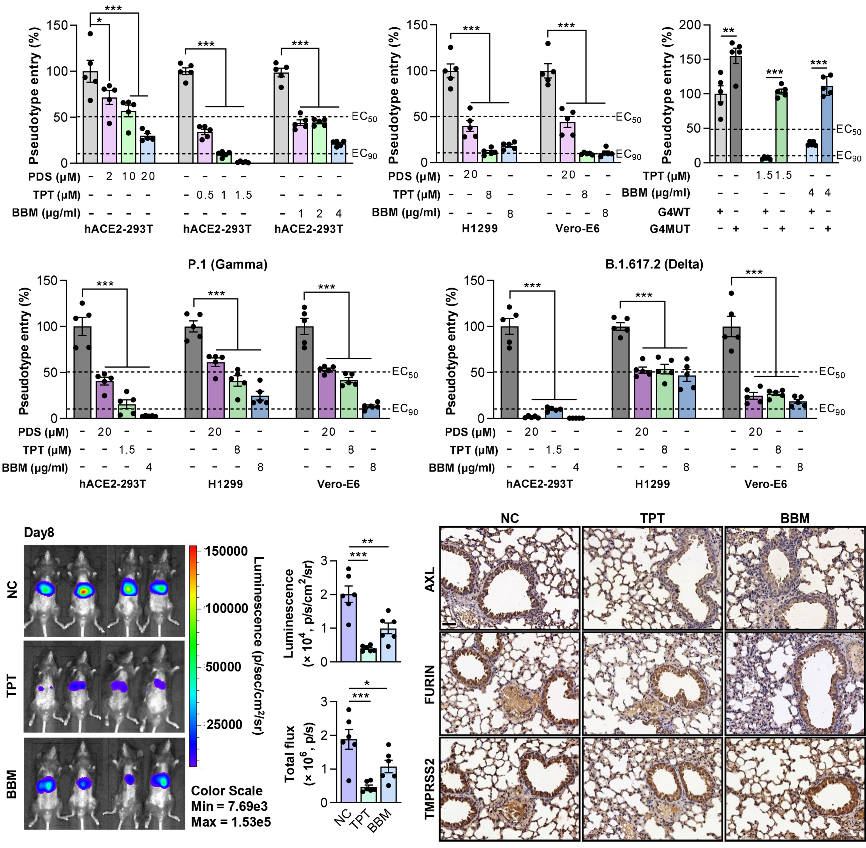 图4. TPT、BBM抑制SARS-CoV-2感染(图源:Qiyu Tong,et al.,PLoS Pathog, 2023) 图4. TPT、BBM抑制SARS-CoV-2感染(图源:Qiyu Tong,et al.,PLoS Pathog, 2023)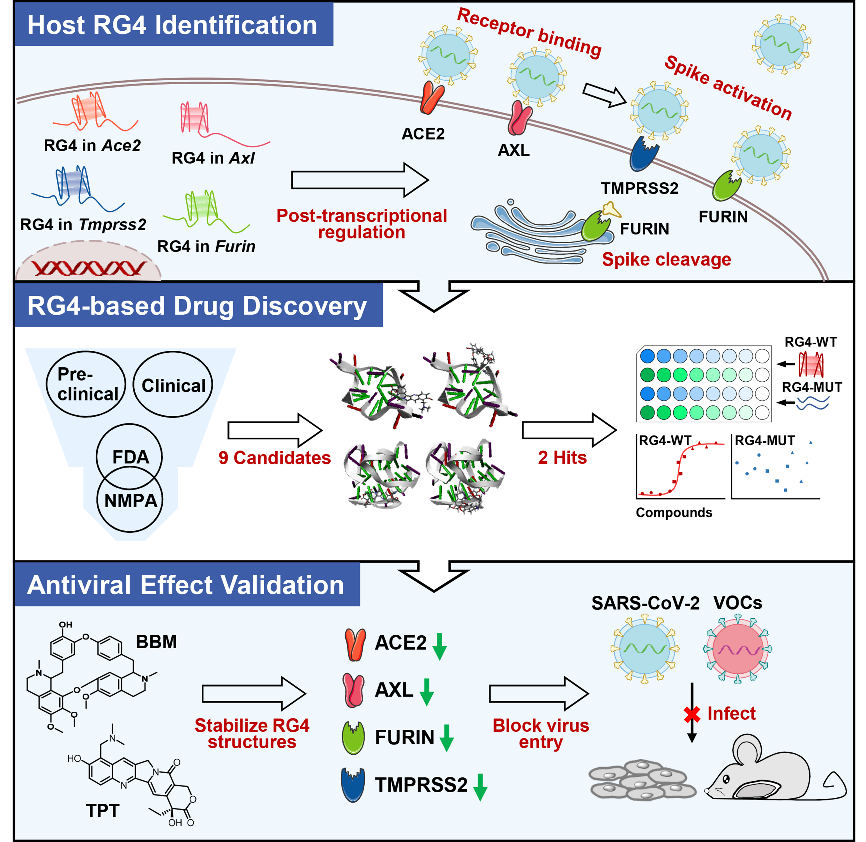 图5. 工作总结图:TPT和BBM通过靶向SARS-CoV-2宿主因子RG4抑制病毒感染(图源:Qiyu Tong,et al.,PLoS Pathog, 2023) 图5. 工作总结图:TPT和BBM通过靶向SARS-CoV-2宿主因子RG4抑制病毒感染(图源:Qiyu Tong,et al.,PLoS Pathog, 2023)文章结论与讨论,启发与展望 综上所述,该研究发现RG4在SARS-CoV-2感染关键宿主因子中广泛分布,并以RG4为靶点进行抗新冠小分子药物的筛选和鉴定,获得两个能够有效抑制SARS-CoV-2感染的临床药物拓扑替康和小檗胺(图5)。此研究揭示了RG4广泛参与SARS-CoV-2感染调控的重要机制,为新冠防治提供了更加广谱的药物靶向策略。该研究采用的假病毒系统只能模拟病毒进入的过程,因此拓扑替康和小檗胺的防治作用需要在真病毒模型中确认,并通过进一步的临床实验,才能最终指导其防治新冠。 原文链接:https://journals.plos.org/plospathogens/article?id=10.1371/journal.ppat.1011131  通讯作者:傅湘辉教授(左1),田艳副研究员(左2);第一作者:童麒羽(右2)、刘更(右1)(照片提供自:四川大学傅湘辉团队) 通讯作者:傅湘辉教授(左1),田艳副研究员(左2);第一作者:童麒羽(右2)、刘更(右1)(照片提供自:四川大学傅湘辉团队)研究团队简介(上下滑动阅读) 四川大学华西医院傅湘辉教授和田艳副研究员为论文通讯作者,硕士研究生童麒羽和博士后刘更为第一作者。该研究得到国家自然科学基金重大研究计划、面上和青年科学基金项目等项目资助,得到华西医院呼吸与危重症医学科程伟教授和刘丹教授,以及四川大学生物治疗国家重点实验室戚世乾教授的大力支持。傅湘辉教授负责的“代谢与疾病”研究室以代谢科学为中心,主要探究肿瘤和糖尿病、脂肪肝等重大疾病的发病机制,重点发现疾病共性靶点,并开展相关转化应用研究,相关成果以通讯作者发表在J Clin Invest、J Hepatol、Hepatology、Mol Cancer、Mol Ther、Nat Commun、PLoS Biol、PLoS Pathog、Signal Transduct Target Ther、Theranostics、Trends系列期刊等。欢迎有志于课题组相关研究领域的博士后加入(联系邮箱:[email protected])。 往期文章精选 【1】Deve Cell︱白晓春/邹志鹏团队揭示RanGAP1表达缺失是染色体不稳定和骨肉瘤快速发生的元凶 【2】Cell Metab︱质肽生物团队揭示治疗肥胖的新型双靶点长效融合蛋白 【3】Research︱电能细胞生物膜全周期调控:天津大学宋浩团队首次提出导电生物膜全周期调控和构建策略 【4】Cell Rep Med︱聂秀/孟斌/全雪萍团队使用自注意力增强的卷积神经网络预测结直肠癌微卫星不稳定性 【5】PloS Pathog︱王锡锋团队揭示植物病毒操纵介体昆虫自噬促进持久传播的机制 【6】PLoS Genet︱郑道琼/Thomas D. Petes团队合作阐释转座子序列驱动酵母基因组变异规律 【7】EMBO Reports︱吴缅/谷皓/邵凤民团队发现血小板型磷酸果糖激酶PFKP作为蛋白激酶调控mESC胚系分化 【8】Immunity︱杨庆凯团队揭示机体利用DNA间距离(凝聚程度)识别危险或非我DNA的机制 【9】Nat Commun︱曹彦光团队揭示结直肠癌肿瘤响应与复发以及转移病灶所在器官之间的差异性 【10】APS︱上海交通大学朱建伟团队开发评价SARS-CoV-2中和抗体广谱性的方法 优质科研学习课程推荐 【1】肿瘤免疫与新型细胞死亡课题设计及生信分析研讨会( 2023年2月25-26日,腾讯在线会议) 【2】全国循证医学Meta分析与网状Meta研讨会(2023年3月4-5日,腾讯在线会议) 【3】多组学联合网络药理学及分子对接与实验验证研讨会(2023年2月25-26日,腾讯在线会议) 【4】高分SCI文章与标书作图(暨AI软件作图)研讨会(2023年2月25-26日,腾讯在线会议)(延期至:3月24-26日) 【5】宏基因组与代谢组/脂质组学R软件数据可视化研讨会(2023年2月18-19日,腾讯在线会议) 欢迎加入“岚翰生命科学” ”岚翰生命科学“ 诚聘副主编/编辑/运营岗位 (在线办公) 参考文献(上下滑动阅读) [1] Dumas L,Herviou P, Dassi E, Cammas A, Millevoi S. G-Quadruplexes in RNA Biology: RecentAdvances and Future Directions. Trends Biochem Sci. 2021;46(4):270-283. [2] Liu G, Du W, Sang X, et al. RNAG-quadruplex in TMPRSS2 reduces SARS-CoV-2 infection. Nat Commun.2022;13(1):1444. [3] Qin G, Zhao C, Liu Y, et al. RNAG-quadruplex formed in SARS-CoV-2 used for COVID-19 treatment in animal models.Cell Discov. 2022;8(1):86. 本文完 |
【本文地址】
今日新闻 |
推荐新闻 |