指南共识 |
您所在的位置:网站首页 › 最新的生物制剂叫什么名字 › 指南共识 |
指南共识
|
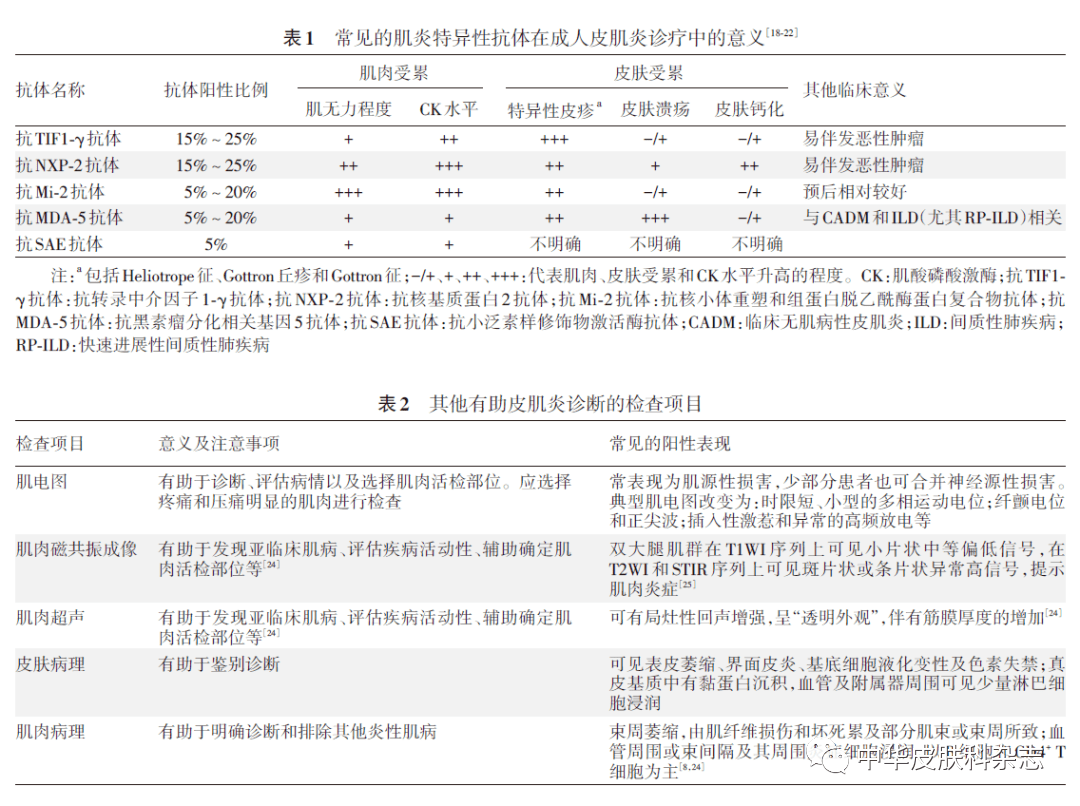
(一)实验室检查 一般实验室检查:可有轻度贫血、白细胞正常或减少。红细胞沉降率和C反应蛋白可升高或正常,与疾病活动程度不平行。血清肌红蛋白在急性期升高,其含量变化可估测疾病活动程度。血清铁蛋白升高是皮肌炎患者发生急性ILD的危险因素,并与皮肌炎合并急性ILD的预后相关。 肌酶谱检查:肌酸磷酸激酶(CK)、乳酸脱氢酶(LDH)、醛缩酶(ALD)、丙氨酸转氨酶(ALT)和天冬氨酸转氨酶(AST)在急性期升高,CK和ALD特异性较高。 肌炎特异性抗体(MSA)和肌炎相关性抗体(MAA):2018年欧洲神经肌肉中心(ENMC)国际研讨会首次根据不同的MSA定义了皮肌炎的临床亚型:①抗TIF1-γ抗体阳性的皮肌炎;②抗核基质蛋白2抗体 阳性的皮肌炎;③抗核小体重塑和组蛋白脱乙酰酶蛋白复合物抗体阳性的皮肌炎;④抗MDA-5抗体阳性的皮肌炎;⑤抗小泛素样修饰物激活酶抗体(阳性的皮肌炎;⑥自身抗体阴性的皮肌炎。每种MSA与独特的临床表型相关,在提示肌肉受累、皮肤受累、ILD和肿瘤发生情况等方面的差异见表1 [18-22] 。MSA有助于在缺少肌肉活检以及临床表现不典型的情况下进行辅助诊断,也有助于指导治疗和预后判断。除以上常见MSA外,抗氨基酰tRNA合成酶抗体也被认为是MSA,与抗合成酶综合征相关。 MAA常提示肌炎与其他结缔组织病重叠。 (二)其他有助诊断的检查项目 其他有助皮肌炎诊断的检查项目见表2,包括肌电图、肌肉磁共振成像(MRI)、肌肉超声、皮肤病理、肌肉病理检查等。
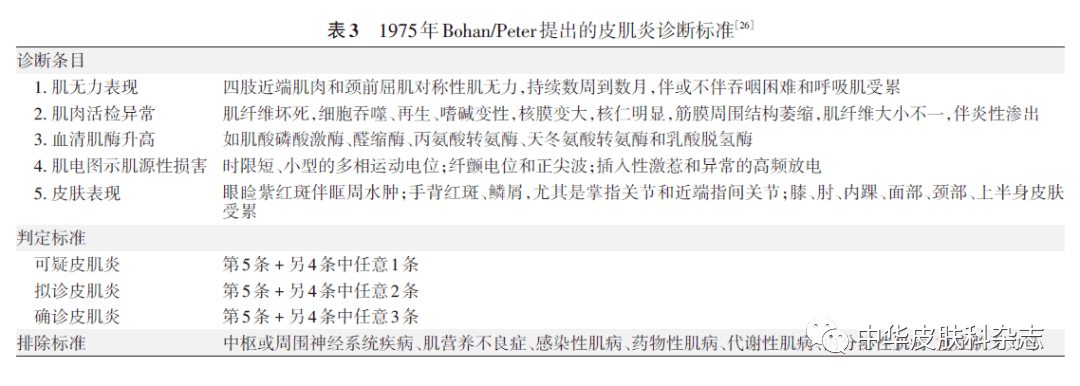
(三)肺、心脏受累的辅助检查 建议所有皮肌炎患者完善肺功能(含一氧化碳弥散功能)和肺部高分辨计算机断层扫描(HRCT)检查。若初次评估未见异常,需密切监测,在出现新的肺部症状或症状加重时需再次行HRCT。 (四)肿瘤筛查 应结合皮肌炎患者的年龄、症状、MSA等评估伴发恶性肿瘤的风险,筛查的方法包括体检、血尿便常规、肿瘤标志物、影像学检查、细胞学检查、鼻咽喉镜和胃肠镜等。 三、诊断 (一)皮肌炎的诊断 1. 目前国内最常用的皮肌炎诊断标准为1975年Bohan和Peter提出的标准(表3)。该标准简便易用,临床应用最广泛,不足之处在于未考虑MSA、影像学等指标,也不能用于诊断CADM。
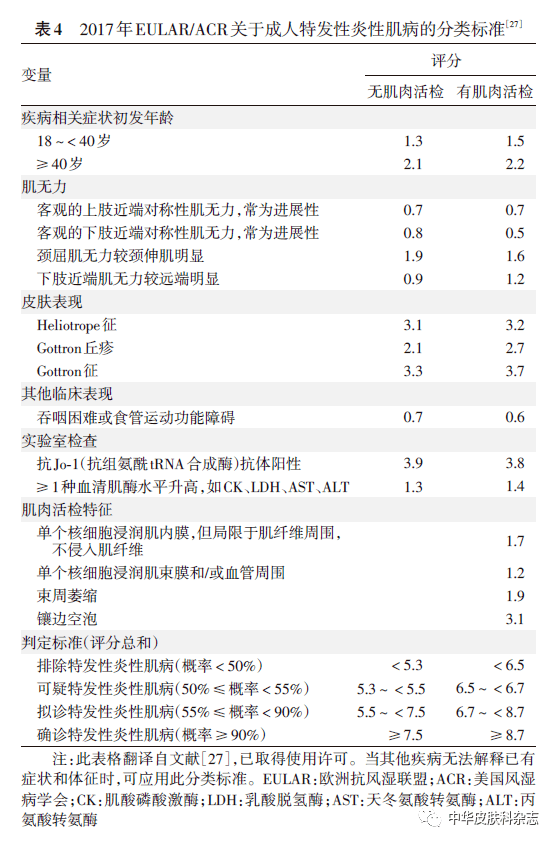
2. 最新的成人皮肌炎分类标准由欧洲抗风湿联盟(EULAR)和美国风湿病学会(ACR)于2017年提出。按照EULAR/ACR分类标准,患者积分概率 ≥ 55%视为拟诊IIM(表4),拟诊IIM患者满足下述①②③项即可诊断为成人皮肌炎:①首次出现IIM相关症状时年龄 ≥ 18岁;②有Heliotrope征或Gottron丘疹或Gottron征;③客观的上肢近端对称性肌无力(指经徒手肌力测定或者其他肌力检查方法证实的肌无力),常为进展性,或客观的下肢近端对称性肌无力,常为进展性,或颈屈肌无力较颈伸肌明显,或下肢近端肌无力较远端明显。若满足①、②,但不满足③,可诊断为无肌病性皮肌炎。与既往多数标准相比,此标准具有更高的敏感性和特异性。此标准中,临床表现典型(如具有典型皮疹)的患者无需进一步检查(如肌肉活检),然而部分不具备典型皮疹的患者可能漏诊。此外,该标准未纳入肌电图、肌肉MRI、除抗Jo-1抗体以外的MSA等指标,且主要基于高加索人群,在国内的应用有待进一步验证。
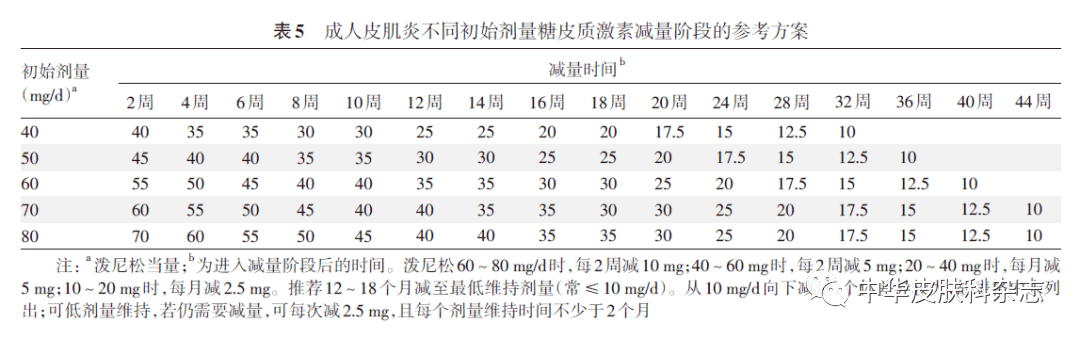
(二)CADM的诊断 部分患者可仅有皮肌炎的典型皮肤表现而没有肌无力表现,且皮损组织病理符合皮肌炎。如果这类患者病程长于6个月,在最初6个月内未进行连续2个月以上的免疫抑制治疗,且未使用能导致皮肌炎样皮损的药物如他汀类降脂药、羟基脲等,可诊断为CADM。CADM又可根据是否伴有血清肌酶升高、肌电图及肌活检等异常,分为无肌病性皮肌炎和低肌病性皮肌炎(又称微肌病性皮肌炎)。与经典型皮肌炎相比,CADM合并ILD的风险升高,且更易发生RP-ILD。CADM亦可伴发恶性肿瘤。对于CADM,推荐进行与经典型皮肌炎一样的胸部影像学检查和恶性肿瘤筛查。 四、治疗原则及方案 (一)经典型皮肌炎 1. 激素:系统应用激素是皮肌炎治疗的首选方案,其治疗可分为初始阶段、减量阶段、维持阶段。 初始阶段:激素剂量一般为泼尼松0.75~1 mg·kg-1 ·d-1 (最大不超过80 mg/d),或等效剂量的其他激素。 减量阶段:多数患者在用药4~6周后明显改善,主要表现为肌酶明显下降和肌力明显恢复,此时可进入减量阶段。该阶段激素减量应根据患者具体病情,如肌酶下降和肌力恢复情况综合考虑。日本、德国专家建议每周减5~10 mg,低于20 mg时每周减2.5~5 mg,然而,皮肌炎复发率超过50%,多发生于激素减量阶段。皮肌炎尚无标准的激素减量方案,结合文献及专家意见,本共识建议参考表5的减量方案。
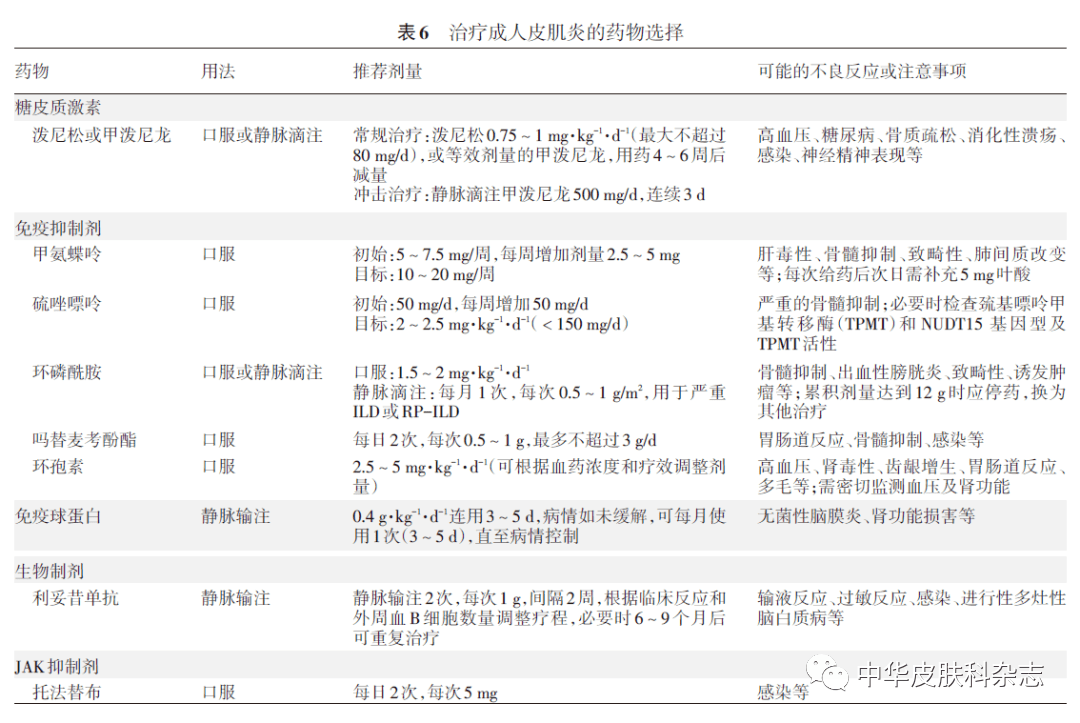
维持阶段:激素减至最低维持剂量后,通常维持2年或以上,以减少复发。 对应用上述推荐剂量激素联合免疫抑制剂治疗失败的肌肉严重受累的患者,可采用静脉滴注甲泼尼龙冲击治疗,500 mg/d连续3 d,然后恢复到冲击前的激素治疗剂量。 部分经典型皮肌炎皮损对激素不敏感,尤其是头面部皮损。皮损持续存在及皮损伴随的瘙痒持续不缓解,通常不影响激素减量。当患者对激素反应欠佳时,可能存在诊断有误、治疗欠妥、伴发肿瘤、激素诱导性肌病等情况。开始激素治疗或激素加量超过1个月后,若肌无力较前加重,且存在其他库欣综合征样特征,同时血清肌酶水平正常、不变或降低,提示激素诱导性肌病可能。 随访:定期评估疗效,建议初始阶段每周1次,减量阶段每2~4周1次,维持阶段每3个月1次。减量阶段应开始配合适量功能锻炼和康复理疗。应全程监测肌酶水平、肌力情况、皮肌炎其他系统表现等。用徒手肌力测定方法,评估颈部屈肌、三角肌、肱二头肌、腕部伸肌、臀大肌、臀中肌、股四头肌和踝背屈肌等肌肉。也可采用测定30 s内手臂上提1 kg重物的次数、双手交叠从座位上站起的次数等简易测试。 2. 免疫抑制剂:单用激素仅适用于部分轻症皮肌炎患者,多数患者需使用免疫抑制剂。通常在开始激素减量前后加用免疫抑制剂,以实现激素的早期减量,减少激素的累积用量,并降低复发率。当皮肌炎病情危重,如出现重症肌炎、吞咽困难、RP-ILD时,可将激素联用免疫抑制剂作为初始治疗。针对肌肉受累,皮肌炎患者中最常选用的免疫抑制剂为甲氨蝶呤(MTX)和硫唑嘌呤(AZA),前者起效更快 [18] 。必要时应进行巯基嘌呤甲基转移酶(TPMT)和NUDT15基因型检测及TPMT活性检测。MTX的初始剂量为5~7.5 mg/周,每周增加2.5~5 mg,目标剂量为10~20 mg/周。AZA的初始剂量为50 mg/d,每周增加50 mg/d,目标剂量为2~2.5 mg·kg -1 ·d -1 (<150 mg/d)。合并ILD的皮肌炎患者首选的免疫抑制剂为环磷酰胺(CTX)。 对于激素联合MTX或联合AZA治疗抵抗的患者,可考虑更换为其他免疫抑制剂,如吗替麦考酚酯(MMF)、环孢素(CsA)、CTX。对于应用激素顾虑较大的患者,或可不采用激素,仅采用免疫抑制剂的联合治疗,如MTX + AZA联合方案:起始剂量为MTX 7.5 mg/周,AZA 50 mg/d,逐步增加至最大剂量(MTX 25 mg/周,AZA 150 mg/d)。 3. 其他治疗:对激素联合MTX或联合AZA治疗抵抗的患者,也可加用静脉输注免疫球蛋白(IVIG)。治疗方案为0.4 g·kg -1 ·d -1 连用3~5 d,若病情不缓解,可每月使用1次(3~5 d),直至病情控制。 难治性皮肌炎可应用抗CD-20单抗(利妥昔单抗)和JAK抑制剂(托法替布、巴瑞替尼等)。其他报道过的生物制剂有抗白细胞介素6受体单抗(托珠单抗)、T细胞选择性共刺激免疫调节剂(阿巴西普)、肿瘤坏死因子α抑制剂(英夫利西单抗)、白细胞介素1受体拮抗剂(阿那白滞素)、抗CD-52单抗(阿仑单抗)等;其他报道过的口服小分子抑制剂有磷酸二酯酶4抑制剂(阿普斯特)等。难治性皮肌炎也可应用血液净化治疗,如血浆置换或血液灌流等。治疗皮肌炎的药物选择详见表6 。
(二)CADM 1. 防晒:应穿戴宽檐帽和防晒服,严格注意光防护,缩短日晒时间。外出时若日晒明显,应选择高防晒系数的广谱防晒剂。 2. 外用治疗:头皮、躯干、四肢等部位皮损常选择中效或强效激素,面部、腋窝、腹股沟等皮肤较薄部位皮损常选择弱效激素,建议每日2次。封包治疗可提高激素穿透力和效力,可能有助于手背等部位皮损的治疗。剂型方面,躯干、四肢等部位常用软膏、乳膏等,头皮等部位常用泡沫剂、洗剂、溶液等。如需长期治疗,可逐渐减少用药频率,降低激素效价,或采用间隔疗法(如治疗2周、停药2周),或联用钙调磷酸酶抑制剂,以减少局部和全身不良反应。 钙调磷酸酶抑制剂(常用0.03%或0.1%他克莫司软膏,也用1%吡美莫司乳膏)可用于外用激素治疗无效的患者,或用于易发生皮肤萎缩部位的长期维持治疗,建议每日2次,开始使用时可能会有皮肤烧灼、疼痛感,可逐步建立耐受,疗程常为1~2个月。此外,皮肤屏障修复剂和保湿剂或可减少水分丢失,缓解瘙痒。 3. 系统药物治疗:对于中度和重度皮损,推荐的一线药物是MMF或MTX,剂量最高分别可达3 g/d和20 mg/周,可单独使用;但当病情进展至出现肌肉病变时,需联合系统应用激素。若MMF无效,可换用MTX,反之亦然,若均无效,可选择使用利妥昔单抗、IVIG、CsA等。口服抗组胺药物,尤其是具有镇静作用的抗组胺药物,可用于瘙痒性皮疹。氨苯砜、沙利度胺也可改善皮肤症状。 推荐羟氯喹与免疫抑制剂等药物联用,并建议进行眼科基线检查及随访评估。单独系统应用激素对CADM疗效也欠佳,不推荐单独应用。 皮肤钙化可采用个案报道的地尔硫卓、小剂量华法林、丙磺舒、氢氧化铝和双磷酸盐等,也可考虑手术切除。 (三)皮肌炎合并系统受累 1. 皮肌炎合并ILD:ILD是皮肌炎患者预后不良的重要因素。抗MDA-5抗体阳性的皮肌炎患者合并ILD概率增加,需重视抗MDA-5抗体的筛查,对此类患者积极干预,从而改善预后。 (1)药物治疗主要是系统应用激素,若病情稳定,可予泼尼松0.75~1 mg·kg-1 ·d-1 口服,加用或联用一种免疫抑制剂。对于严重ILD或RP-ILD导致病情加重甚至呼吸衰竭时,可采用三联治疗:静脉滴注甲泼尼龙(参考剂量:80 mg/d),并联用钙调磷酸酶抑制剂(CsA或他克莫司,需根据血浆药物水平和药物有效性调整剂量)和静脉滴注CTX(每月1 次,每次0.5~1 g/m2 )。肾功能正常时,CsA谷浓度应维持在100~150 ng/ml,他克莫司谷浓度应维持在5~10 ng/ml。用药前应充分评估感染风险,必要时可使用抗生素预防性抗感染。病情改善后激素逐渐减量,免疫抑制剂可以更换为口服MMF。 (2)ILD患者一般不使用MTX,因为MTX可引起ILD,甚至RP-ILD。 (3)调整治疗前,需评估是否存在引起肺功能恶化的其他原因,如合并感染、药物性肺炎或呼吸肌无力等。 (4)若激素和免疫抑制剂疗效欠佳,可尝试更换或联用IVIG。 (5)抗MDA-5抗体阳性的ILD患者可考虑早期使用JAK抑制剂(如托法替布)。 2. 皮肌炎合并心脏受累:皮肌炎患者合并心脏受累时,采用的疗法与合并ILD类似,即系统应用激素,联用免疫抑制剂(如CsA、CTX、AZA等)或利妥昔单抗治疗。对于病情严重的患者,可采用激素冲击治疗。 3. 皮肌炎合并食管肌受累:皮肌炎患者合并食管肌受累应加强护理,并系统应用激素联合IVIG治疗,或联合免疫抑制剂(MTX、AZA等)治疗。对于病情严重的患者,可采用激素冲击治疗。 (四)皮肌炎合并恶性肿瘤 皮肌炎患者合并恶性肿瘤时,应同时治疗恶性肿瘤(手术切除、放疗、化疗等)和皮肌炎(激素和免疫抑制剂等)。激素和免疫抑制剂可能加重免疫抑制状态,延缓术后伤口愈合。需根据皮肌炎和肿瘤的病情严重程度选择主要的治疗目标。 (五)皮肌炎合并妊娠 皮肌炎合并妊娠较少见,治疗首选系统应用激素,根据疾病活动程度调整剂量。妊娠期妇女在使用较低剂量激素(泼尼松<15 mg/d)的情况下,胎儿的风险较低,但妊娠期妇女长期使用较高剂量激素,可对胎儿有毒性作用或致早产风险增加。有文献报告IVIG、羟氯喹和AZA治疗少量妊娠期IIM病例,可考虑作为二线药物。MTX和CTX由于潜在的致畸性、致突变性和胚胎毒性,禁用于妊娠期。 (六)慢性复发型皮肌炎 复发时应根据患者具体情况采用不同药物种类和剂量,若激素未停用,建议增加至泼尼松0.5~1 mg·kg-1·d-1。若激素疗效欠佳,应换用或加用免疫抑制剂,并联用IVIG,也可选择生物制剂或口服小分子抑制剂。一旦重新控制病情,建议更缓慢地减量激素。若患者已停用激素,应重新评估病情,确定治疗方案。需要注意的是,对于肌肉状态稳定、仅有皮损复发的情况,不推荐单独增加激素剂量。 五、成人皮肌炎治疗管理流程图 成人皮肌炎的治疗需结合患者的临床表现、病情严重程度、其他系统受累、伴发疾病等因素,选择合适的治疗方案。我们总结了成人皮肌炎患者治疗管理的简易流程图,见图1。
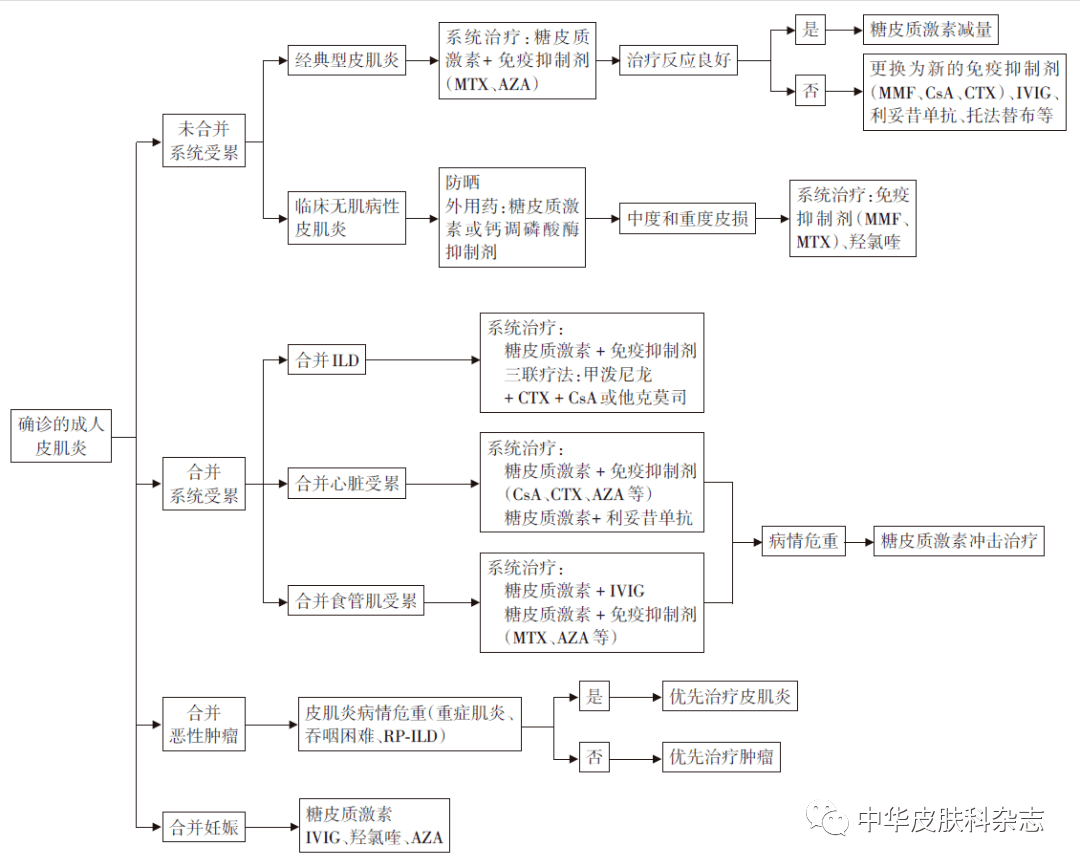
MTX:甲氨蝶呤;AZA:硫唑嘌呤;MMF:吗替麦考酚酯;CsA:环孢素;CTX:环磷酰胺;IVIG:静脉输注免疫球蛋白;ILD:间质性肺疾病;RP⁃ILD:快速进展性间质性肺疾病 图1 成人皮肌炎患者治疗管理流程图(防晒和外用治疗适用于所有类型的皮肌炎) 以上内容引自:成人皮肌炎诊疗中国专家共识(2022年)[J].中华皮肤科杂志,2022, 55(11):939-948. 来源:皮科学术研究院返回搜狐,查看更多 |
【本文地址】
今日新闻 |
推荐新闻 |