硫酸铜的提纯实验报告(八篇) |
您所在的位置:网站首页 › 无机化学的实验报告 › 硫酸铜的提纯实验报告(八篇) |
硫酸铜的提纯实验报告(八篇)
|
五水硫酸铜结晶水含量的测定 一、实验目的要求: 1.了解制备五水硫酸铜晶体的方法。 2.测定硫酸铜的结晶水含量。 二、实验内容: 1.五水硫酸铜的提纯。 2.五水硫酸铜晶体自由水的脱去。 3.测定硫酸铜晶体里的结晶水含量。 三、主要仪器设备及药品: 仪器设备:电子天平,称量瓶,不锈钢锅(薄壁,内装食盐用于盐浴),温度计(量程在350℃,测量盐浴温度),烘箱(烘干自由水),电炉,滤纸,皮筋。 药品:五水硫酸铜,3公斤食盐左右(用于盐浴加热),无水乙醇。 四、实验原理 五水硫酸铜结构:
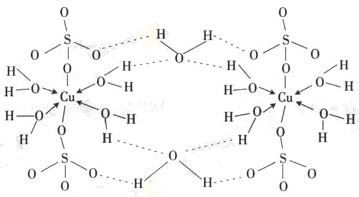
图1 CuSO4·5H2O的晶体结构 一般性质 硫酸铜CuSO4(硫酸铜晶体:CuSO4·5H2O)分子量249.68。深蓝色大颗粒状结晶体或蓝色颗粒状结晶粉末,略透明。有毒,无臭,带有金属涩味。密度2.2844g/cm-3。干燥空气中会缓慢风化。易溶于水,水溶液呈弱酸性。不溶于乙醇,缓缓溶于甘油。150℃以上将失去全部水结晶成为白色粉末状无水硫酸铜。五水硫酸铜有极强的吸水性,把它投入95%乙醇成含水有机物(即吸收水分)而恢复为蓝色结晶体。 失水过程
五水硫酸铜晶体失水分三步。上图中两个仅以配位键与铜离子结合的水分子最先失去,大致温度为102摄氏度。两个与铜离子以配位键结合,并且与外部的一个水分子以氢键结合的水分子随温度升高而失去,大致温度为113摄氏度。最外层水分子最难失去,因为它的氢原子与周围的硫酸根离子中的氧原子之间形成氢键,它的氧原子又和与铜离子配位的水分子的氢原子之间形成氢键,总体上构成一种稳定的环状结构,因此破坏这个结构需要较高能量。失去最外层水分子所需温度大致为258摄氏度。 五、实验步骤: 1、在常温下将适量的CuSO4溶解于少量的水中,配置成过饱和溶液,倒掉上层溶液,取未溶解的五水硫酸铜加少量水洗涤三次,再用无水乙醇洗涤三次,将所得试剂尽量滴干(为节约实验时间,可用滤纸将大部分自由水吸干)。 …… …… 余下全文 |
【本文地址】
今日新闻 |
推荐新闻 |