专家共识丨冠状动脉CT血流储备分数应用临床路径中国专家共识 |
您所在的位置:网站首页 › 无创ffr检测 › 专家共识丨冠状动脉CT血流储备分数应用临床路径中国专家共识 |
专家共识丨冠状动脉CT血流储备分数应用临床路径中国专家共识
|
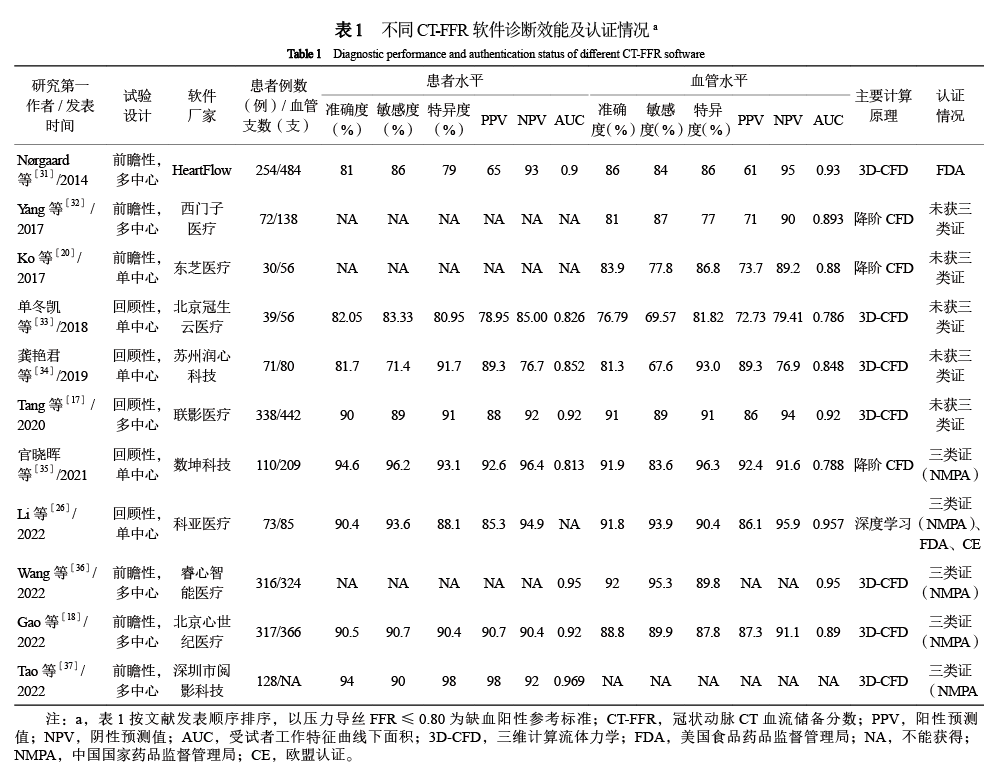
为帮助我国广大临床工作者合理、规范地应用CT-FFR,中国医师协会心血管内科医师分会超声心动图和影像学组联合《中国介入心脏病学杂志》编辑委员会牵头组织相关专家,基于国内外最新临床研究成果,参考相关指南和共识,结合我国国情和临床实践,撰写了该共识。专家组希望本临床路径共识的制订与发布能够对未来CT-FFR技术进一步参与患者诊疗起到积极的推动作用。 1 CT-FFR基本原理及诊断效能 1. 1 CT-FFR基本原理 CT-FFR是一项无创的图像后处理技术,基于常规CCTA所获得的冠状动脉三维图像,辅以计算机专用软件,即可根据冠状动脉解剖模型,联合冠状动脉生理学的数学模型、流体动力学的物理定律,模拟冠状动脉血流情况,计算冠状动脉流速和压力,提供模拟FFR结果。CT-FFR将冠状动脉狭窄的解剖严重程度与其生理效应耦合起来,提供了狭窄病变的生理学信息,使临床医师能更全面地了解冠状动脉的供血情况。 经典的CT-FFR计算大致可分为3个要素。(1)从CCTA图像提取出解剖模型,设定计算模拟的区域。以往需要人工分割血管边界生成模型。随着机器学习人工智能技术的应用,大部分工作可由计算机自动完成。(2)选择合适的数学模型和数值方法。描述流体运动的纳维-斯托克斯(Navier-Stokes)方程也适用于大动脉和冠状动脉的血液流动。复杂区域的纳维-斯托克斯方程需要使用数值方法在计算机上求解。例如有限元法,由于适合处理具有复杂边界的问题,被最先应用到CT-FFR的计算。(3)确定边界条件。除了选定微分方程,求解还需要边界信息,例如入口的流量、下游血管的流阻等。边界条件需要符合患者的生理特征,这些信息可通过临床数据和数学模型估算。根据FFR计算所采用的方法,目前可用的CT-FFR软件主要有以下3类:基于三维计算流体力学(3D-computational flow dynamics,3D-CFD)的CT-FFR、基于降阶CFD的CT-FFR、基于深度学习的CT-FFR。 1. 1. 1 基于3D-CFD的CT-FFR 基于3D-CFD的CT-FFR软件以血管的三维模型为基础,采用了计算流体力学的数值方法,辅以心血管力学模型计算出三维模型中压力速度场,进而估计出CT-FFR。基于3D-CFD的CT-FFR对血流的还原程度较高、具有较高的精准度,但其计算量较大,早期每例的处理时间较长(一般为1~4 h),需要专业人员在核心实验室的超级计算机上进行离线并行计算和处理,限制了其在临床的广泛应用。近年来随着技术和算法的进步,基于3D-CFD的CT-FFR在精准度和计算时间上都有明显提高,这使得基于3D-CFD的CT-FFR实现了现场实时分析。基于3D-CFD的计算方法在原理上适用于各种冠状动脉解剖结构和复杂病变,但对于血管边界的重建要求较高,跟其他CT-FFR方法一样受图像质量影响。 1. 1. 2 基于降阶CFD的CT-FFR 基于降阶CFD的CT-FFR软件便于现场部署及计算,通过一维降阶模型进行流体模拟,沿着冠状动脉树进行压力、流量的测定,最后,将CT-FFR值的空间分布以彩色编码地图的方式投影至三维冠状动脉树模型上。基于降阶CFD的计算时间显著低于3D-CFD,计算时间2~5 min,图像分割及人工修改时间另计,目前已经能实现一站式自动化CT-FFR分析。基于降阶CFD的计算方法,丢失了部分三维信息,因此在某些复杂解剖结构上精准度可能会受到限制。 1. 1. 3 基于深度学习的CT-FFR 基于机器学习算法的CT-FFR使用深度学习框架,采用多层神经网络结构和一维降阶模型,对大数据集的冠状动脉树解剖结构与其相应计算血流动力学之间的复杂关系进行离线训练、学习,模拟一个符合CFD计算结果的模型。完成训练后基于深度学习相比基于3D-CFD可以更快地计算CT-FFR,更加适合现场部署计算。基于深度学习的计算方法,由于训练集中存在的压力导丝FFR测量的真实CCTA数据很有限,因此对于训练集中不存在或代表性不够的冠状动脉解剖结构和复杂病变,计算结果可能存在一定的不确定性。 1. 2 CT-FFR的诊断效能 最早由HeartFlow公司资助的3项前瞻性、多中心、核心实验室采用盲法分析的对照试验,以压力导丝FFR(0.80为界值)作为参考标准,证明了与CCTA相比,CT-FFR与压力导丝FFR有更高的一致性,在诊断效能上具有优势。此后国内外多家公司也开展了CT-FFR分析软件的开发和应用,不同算法的CT-FFR也相继应用于冠心病的精准诊治。表1罗列了部分相关诊断效能的临床研究结果,随着算法的优化,CT-FFR对于心肌缺血的诊断效能逐渐提高。
由于受到CT空间分辨力和冠状动脉钙化所致的线束硬化伪影的限制,CCTA经常高估狭窄程度,进一步限制了特异性。一项基于深度学习的CT-FFR研究显示,在轻度至中度钙化病变中,CT-FFR比CCTA表现出更好的鉴别缺血能力,在中度或严重钙化的患者和血管中诊断的准确度和特异度均高于CCTA。另一项研究也发现在严重钙化的冠心病患者中(钙化评分>400),CT-FFR的准确度和特异度均显著高于CCTA(75%比44%,69%比23%),而敏感度的差异无统计学意义(88%比94%)。FACC研究前瞻性入选了260例钙化积分>399分(中位数为895分,43%的患者>1 000分)的稳定胸痛患者,78%的患者CT-FFR值≤0.80,以压力导丝FFR(共112例患者182支血管)为对照时,血管水平CT-FFR诊断的准确度为78%,敏感度为82%,特异度为75%,受试者工作特征曲线下面积为0.81。 2 CT-FFR的图像质控、工作流程及测量位置选择 2. 1 图像质控 CT-FFR是基于冠状动脉模型进行仿真计算的,而冠状动脉模型的精准度严重依赖于CCTA图像质量。目前CT扫描的最小空间分辨率约为0.5 mm,只能检测到0.5 mm以上厚度的斑块。目前,CT-FFR对于直径2.5 mm以上冠状动脉的计算是可靠的(图像质量优越的可适当放宽至2.0 mm),然而冠状动脉钙化和图像伪影也是制约CT-FFR计算的重要因素。ADVANCE研究在注册队列和临床队列中分别有2.9%和8.4%的患者因为CCTA图像质量问题未能完成CT-FFR计算。要想获得准确的CT-FFR值,需要优化CCTA影像采集从而获取高质量图像。高时间分辨率、高管电压、薄层厚、低心率能获得较高的图像质量。所以CCTA要在至少64排探测器的CT设备上完成,并严格执行心血管CT指南的扫描计划;在无禁忌证的情况下使用 β受体阻滞剂将心率降至70次/分以下(最好降至65次/分以下);在无禁忌证的情况下扫描前3~ 5 min舌下含服硝酸甘油(片)或者喷服硝酸甘油(气雾剂)。获取CCTA图像后如有明显的运动伪影或者断层伪影,不建议进行CT-FFR测量。由于总钙化积分>1 000分的患者进行CT-FFR计算的准确度不确定,也建议进行排除。 推荐意见:用于CT-FFR测量的CCTA图像要用至少64排探测器的CT,遵守心血管CT指南扫描规范。不建议对有严重伪影和严重钙化(总钙化积分>1 000分)的图像进行CT-FFR测量。 2.2 CT-FFR工作流程 临床医师提出进行CT-FFR测量的需求,在CCTA图像质控合格满足CT-FFR测量条件下,将CCTA图像导入CT-FFR相关软件工作站。软件进行血管分割及斑块检出(不同软件具体操作会稍有不同),虽然现在很多软件的血管分割和斑块检出准确度较高,但还是建议由测量员进行人工复核,必要时进行手动调整,所有测量员要经过规范专业的培训并通过测量一致性评价后方可对患者的临床数据进行正式测量。人工复核完毕后由软件进行相应的建模计算,获得冠状动脉树任意一点的CT-FFR值。最后结果需要上级医师进行审核确认。简要流程见图1。
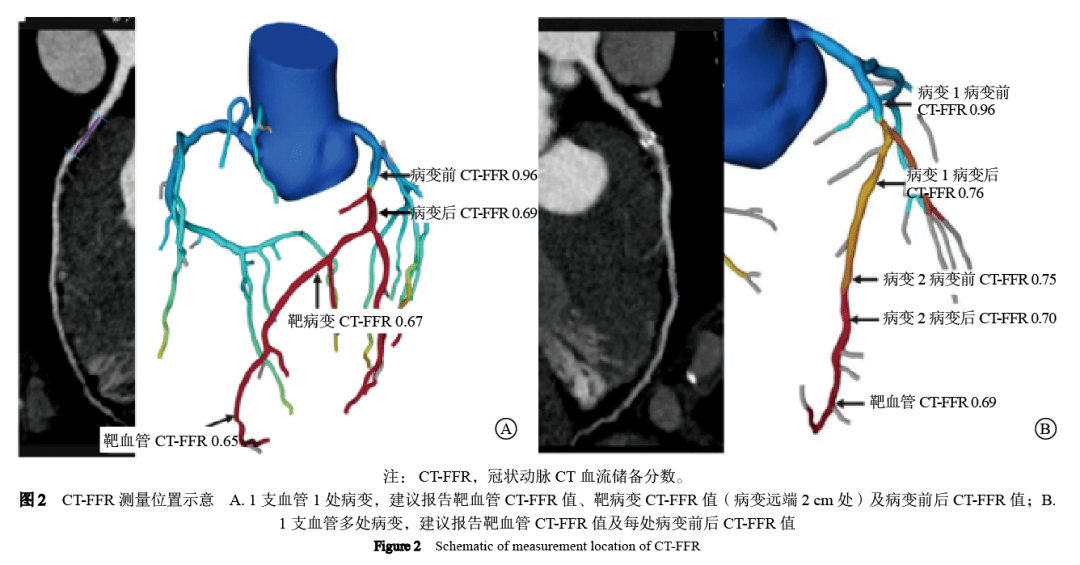
2.3 测量位置选择 CT-FFR能提供整个冠状动脉树任意位置的CT-FFR值,应该根据临床医师关注的靶血管和靶病变确定测量位置。如无特殊,首先报告靶血管水平的CT-FFR值,一般将测量位置定为血管远端直径等于2 mm处;还要报告靶病变水平的CT-FFR值,推荐测量位置选择病变远端2 cm处;对于1条靶血管多处病变的情况,还要报告每个病变的跨病变△CT-FFR值,即病变近端与远端CT-FFR的差值(图2)。临床医师和影像科医师应当共同合作,在CT-FFR计算前对CT图像及测量位置进行必要的确认。
推荐意见:建议同时提供靶血管、靶病变及跨病变△CT-FFR值。 3 CT-FFR的临床证据 3.1 CT-FFR减少ICA的使用,提高血运重建占比 在CCTA诊断为严重狭窄的病变中,只有49%在压力导丝FFR评估时显示血流动力学有意义。PLATFORM研究显示在计划进行ICA的临床稳定的患者中,61%的患者在接受CCTA/CT-FFR检查后取消ICA。NXT研究中,CT-FFR将68%的CCTA假阳性患者和67%的CCTA假阳性血管正确地重新分类为真正的阴性结果,降低了临床误诊率,提高了ICA的效率。CT-FFR RIPCORD研究将NXT研究中的患者信息交由3名临床医师进行回顾性、假设性的临床决策。研究者发现通过CT-FFR检查后,44%患者的治疗方式被改变,18%的患者改变了需要血运重建的靶血管。在真实世界的ADVANCE注册研究中,与最开始的基于CCTA的治疗计划相比,CT-FFR改变了66.9%患者的临床诊疗计划。FORECAST研究是一项多中心随机对照研究,1 400例患者随机分为常规临床诊疗组和CCTA/CT-FFR指导诊疗组,结果显示CCTA/CT-FFR组ICA的比例显著低于常规诊疗组(19%比25%, P =0.01),而CCTA/CT-FFR组血运重建占比高于常规诊疗组(75%比55%),提 示CT-FFR有助于提高ICA的效率。CT-FFR在复杂冠心病中也证明了其可行性和准确性。SYNTAX Ⅲ REVOLUTION研究是一项多中心随机对照研究,比较左主干或三支血管病变患者分别行CCTA、ICA后的临床决策。结果显示CT-FFR纠正了CCTA对SYNTAX评分的过高估计,与ICA相比,在相似程度上改变患者的临床决策(6.3%比9.0%)。 3. 2 CT-FFR对冠心病患者的预后价值 PLATFORM研究在90 d随访中,使用CT-FFR后取消ICA的患者没有发生主要不良心血管事件(major adverse cardiovascular events,MACE)。同时在1年随访时计划ICA队列中直接ICA组和CCTA/CT-FFR指导组患者的临床事件和生活质量差异均无统计学意义,但CT-FFR组的医疗支出减少。ADVANCE注册研究观察到,在CT-FFR>0.80的患者中,90 d内无死亡/心肌梗死发生,而在CT-FFR≤0.80的患者中,MACE发生率( HR 19.75,95% CI 1.19~326, P =0.008)和死亡/心肌梗死发生率( HR 14.68,95% CI 0.88~246, P =0.039)均显著升高,表明CT-FFR>0.80与良好的短期预后相关。在ADVANCE注册研究1年的随访中,CT-FFR值与之后ICA、血运重建和MACE发生率呈负相关,由于总体事件率仅1.16%,与CT-FFR>0.80相比,CT-FFR≤0.80的患者MACE风险增加差异无统计学意义( RR 1.81, P =0.06),但心血管死亡或心肌梗死的风险显著增加( RR 4.22,95% CI 1.28~13.95, P =0.01);而在CT-FFR>0.90的患者中无任何临床事件发生。Nørgaard等进行的一项单中心研究发现CT-FFR>0.80的患者可以安全地推迟ICA,其在2年随访的不良心血管事件发生率(全因死亡、心肌梗死、因不稳定型心绞痛住院或非计划血运重建术)与CCTA狭窄<30%的患者相似( P =0.58)。NXT试验的5年随访研究表明,CT-FFR≤0.80患者的全因死亡、心肌梗死、血运重建的复合终点显著升高;此外,与PLATFORM研究结果相似的是,CT-FFR>0.80的患者没有发生心肌梗死或死亡,表明了CT-FFR>0.80的长期安全性。近年来,基于功能性的SYNTAX积分也有新的成果,CT-FFR SYNTAX积分(FSS CTA )将CCTA解剖学上的狭窄数据与CT-FFR评估的功能数据相结合,与CCTA SYNTAX积分(SS CTA )和ICA SYNTAX积分(SS ICA )相比,FSS CTA 对MACE的预测准确率更高。以上研究均基于临床情况稳定的患者,一项研究回顾性分析CT-FFR在急诊室急性胸痛患者中的使用。该研究入选的急性胸痛患者排除了心电图明显变化或者心肌标记物阳性,即排除了明确诊断为急性冠状动脉综合征(acute coronary syndrome,ACS)的患者,结果发现CT-FFR>0.80患者90 d随访未发生死亡或者非致死性心肌梗死。综上,CT-FFR对冠心病患者的预后有一定的预测价值。 4 CT-FFR应用临床路径 本共识设定的临床情境是患者已经进行了CCTA检查,且CCTA图像也适合进行CT-FFR测量。 患者的临床疾病状态是千差万别的,在临床实践中,面对复杂的患病个体,需要结合患者的症状、合并症、其他检查结果合理应用CT-FFR,在冠状动脉疾病的诊断、风险评估、个体化治疗方案的制订以及疗效评价方面充分发挥和利用CT-FFR的临床价值。本共识将对哪些临床情况推荐使用CT-FFR及如何解读CT-FFR值进行介绍。 4. 1 CT-FFR应用的一般临床情境 4. 1. 1 无症状人群 国内一些体检机构会对部分冠心病验前概率较高的无症状人群进行CCTA检查,但目前尚无该人群CT-FFR的相关研究。参照稳定冠心病的相关研究,建议狭窄程度>90%的患者由临床医师根据病变部位和其他检查进行个体化评估,判断是否进行ICA检查,狭窄程度30%~90%的患者进行CT-FFR测量。 4. 1. 2 无冠心病史症状稳定或症状不典型患者 这是目前大部分CT-FFR研究入选的患者人群,是循证证据最充分的人群。这些研究大部分入选标准为CCTA狭窄程度为30%~90%的患者(也有研究入选狭窄程度下限定为40%),对CT-FFR>0.80的患者进行药物治疗而不进行ICA,短期及长期的预后均良好。最新的一项多中心随机对照临床研究显示,基于现场部署的CT-FFR诊疗流程将显著减少90 d内ICA发现非阻塞性冠状动脉疾病或不需要干预的患者比例,相较常规诊疗组的降幅达39%;此外,CT-FFR策略增加了入选人群的90 d内血运重建比例,总体上有节省医疗成本的趋势,尽管该策略尚未被发现显著改善症状或生活质量,但也未影响心血管临床终点。本共识建议狭窄程度>90%的患者直接进行ICA检查,狭窄程度30%~90%的血管进行CT-FFR测量。 4. 1. 3 ACS患者 当患者诊断为ACS时,如为ST段抬高的ACS,建议紧急行ICA;如为非ST段抬高ACS,先进行危险分层,当危险分层为低危时,可先进行无创评估,而当危险分层为非低危患者时,建议紧急或择期行ICA。既往CT-FFR研究基本排除了ACS患者。但由于CCTA在低危ACS患者的应用得到临床指南的推荐,所以本共识推荐对于该人群CT-FFR的应用参照上一部分症状稳定患者。近年有不少FFR在ACS患者ICA中应用的相关研究,主要是ICA后发现存在多支血管病变时,FFR可以协助判断靶血管以及指导非靶血管的血运重建。由于目前研发的CT-FFR软件的测量值与FFR一致性良好,本共识推荐CT-FFR可用于协助指导ACS患者ICA后非靶血管是否进行血运重建。CT-FFR在ACS患者中应用时,对CT-FFR测量软件有更高要求,包括部署现场工作站,且图像处理要能在靶血管结束血运重建前完成。 4. 1. 4 有冠心病病史患者 既往有冠心病病史患者,因本共识设定的临床情境是患者已经进行了CCTA检查,可以推荐直接CCTA+CT-FFR临床策略,这样可以减少CCTA检查后评估CT-FFR的等待时间。既往CT-FFR研究基本排除了血运重建的患者,这方面的证据比较缺乏,所以目前不推荐CT-FFR用于血运重建术后血管的常规评估。由于近年来药物球囊使用的增加,对于单纯药物球囊扩张的血管,冠状动脉内无置入物,本共识推荐可以按无血运重建的路径进行。 推荐意见:CT-FFR的临床使用要根据不同场景进行选择,推荐路径见图3。但最终的临床决策需要临床医师结合患者临床表现、病变部位、病变特点来综合决定。
4. 2 CT-FFR界值及解读 FFR的推荐界值是0.80,建议0.80以上病变进行药物治疗;FFR<0.75的病变可诱发心肌缺血,推荐行血运重建;FFR 0.75~0.80为“灰区”,可综合患者的其他情况进行判断。目前大部分临床研究中CT-FFR的界值是0.80。一项荟萃研究发现CT-FFR对FFR值有轻微的低估,当CT-FFR在0.70~0.80时发生诊断错误的可能性最大。为了进一步减少不必要的ICA,本共识专家组推荐CT-FFR的灰区设定在0.70~0.80,由临床医师根据患者的其他信息来决定是否进一步进行ICA。 推荐意见:目标CT-FFR>0.80,认为该血管可能不存在缺血;0.70~0.80为灰区,应综合其他临床信息和检查结果,可充分调整药物治疗后再进行判断;<0.70认为该血管可能存在缺血,建议进行ICA。 4. 3 CT-FFR应用的特殊临床情境 4. 3. 1 经导管主动脉瓣置换术(transcatheter aortic valve replacement,TAVR)前冠状动脉评估 TAVR近几年在国内发展迅速,TAVR术前常规要进行冠状动脉的评估。目前有些中心常规均行ICA检查;有些中心考虑到CCTA的高阴性预测价值,如果CCTA完全阴性就不再进行ICA检查,但如果CCTA阳性或不能确定阴性则会进行ICA检查。有研究提示,TAVR术前的CT-FFR值与术后随访期间的MACE发生率增加相关;而以ICA为参考标准,CT-FFR较单纯CCTA提高了拟行TAVR患者冠状动脉是否存在有意义狭窄的判断准确性,准确度增加3.9%~10.7%,能更大程度地避免不必要的ICA。主动脉瓣重度狭窄影响冠状动脉血流,而TAVR术后的冠状动脉血流会相应增加,目前的CT-FFR产品尚未专门考虑这类人群,准确性还需验证。一项纳入189例行TAVR的患者的研究发现,21.7%的患者TAVR术前和术后的CT-FFR分类发生变化,即术前>0.80的术后变为≤0.80或者反之。 推荐意见:虽然CT-FFR较单纯CCTA能在一定程度上提高主动脉瓣狭窄患者冠状动脉狭窄判断的准确性,但由于TAVR术前术后冠状动脉血流的变化会影响CT-FFR值,故本共识推荐CT-FFR可用于TAVR术前冠状动脉评估,但在解读CT-FFR值时要慎重,可适当增大灰区范围。 4. 3. 2 非心脏手术患者的术前冠状动脉评估 目前国内在非心脏外科术前评估的临床实践中,进行CCTA检查的患者不在少数,PANDA Study验证了CCTA作为非心脏外科手术术前心脏评估的有效性。而相关的术前评估指南对部分患者建议进行运动或者药物负荷试验评估冠状动脉缺血情况。CT-FFR尚未得到术前评估指南的推荐,但由于CT-FFR诊断心肌缺血(以压力导丝FFR为金标准)的准确度接近90%,CT-FFR可以部分取代负荷试验。 推荐意见:CT-FFR可用于非心脏手术患者的术前冠状动脉评估。 5 CT-FFR的局限性 虽然CT-FFR在冠心病诊断、治疗决策方面得到了一定验证,但目前CT-FFR还有一些局限性。(1)CT-FFR获得的临床证据来源于不同的软件,将某一软件的研究结果外推至其他软件产品需慎重。(2)CT-FFR对CCTA的图像质量要求较高,仍有不少比例的CCTA图像无法进行CT-FFR计算。(3)CT-FFR对严重钙化病变的诊断效能不确定。(4)CT-FFR 在经皮冠状动脉介入治疗术后或冠状动脉旁路移植术后的应用还缺乏临床证据。 需要指出的是,CT-FFR只是心脏CT评估技术的一个方面,CT斑块定量分析、CT斑块流体力学分析和CT影像组学分析等,都是近年来涌现的心脏CT评估方法。实际应用中,临床医师需要熟悉并了解相关技术的适应证,丰富各类冠心病状态的临床诊治路径,对患者进行更加精准的个体化诊疗。 目前国内自主研发的CT-FFR软件大部分仅进行了诊断效能方面的研究,其用于临床决策及预后的数据还非常缺乏。需要共同努力进行相关的高质量前瞻性临床研究,为CT-FFR在临床的广泛应用提供更多的证据支持。 写 作 组 成 员 龚艳君(北京大学第一医院),刘学波(同济大学附属同济医院),杨俊杰(中国人民解放军总医院), 张龙江(中国人民解放军东部战区总医院) 专 家 组 成 员 (按照姓名汉语拼音排序):陈端端(北京理工大学生命学院生物医学工程系),陈纪言(广东省人民医院),陈良龙(福建医科大学附属协和医院),陈韵岱(中国人民解放军总医院),程流泉(中国人民解放军总医院),傅国胜(浙江大学医学院附属邵逸夫医院),高传玉(河南省人民医院),葛均波(复旦大学附属中山医院),龚艳君(北京大学第一医院),郭军(中国人民解放军总医院),贺勇(四川大学华西医院),侯阳(中国医科大学附属盛京医院),霍勇(北京大学第一医院),季福绥(卫生部北京医院),金征宇(北京协和医院),孔祥清(江苏省人民医院),兰宏志(深圳睿心智能医疗科技有限公司),李保(山西省心血管病医院/山西二院),李东(天津医科大学总医院),李刚(四川省人民医院),李建平(北京大学第一医院),李浪(广西医科大学第一附属医院),李小虎(安徽医科大学第一附属医院),刘斌(吉林大学第二医院),刘巨(南方科技大学力学与航空航天工程系),刘学波(同济大学附属同济医院),卢光明(中国人民解放军东部战区总医院),吕滨(中国医学科学院阜外医院),马根山(东南大学附属中大医院),马礼坤(安徽省立医院),彭建军(北京世纪坛医院),钱杰(中国医学科学院阜外医院),钱菊英(复旦大学附属中山医院),秦勤(天津胸科医院),邱春光(郑州大学第一附属医院),邱建星(北京大学第一医院),王怡宁(北京协和医院),夏黎明(华中科技大学附属同济医院),徐磊(首都医科大学附属北京安贞医院),严福华(上海交通大学医学院附属瑞金医院),阳炜光(斯坦福大学心血管生物力学计算实验室),杨俊杰(中国人民解放军总医院),杨丽霞(中国人民解放军联勤保障部队九二〇医院),杨敏福(首都医科大学附属北京朝阳医院),于波(哈尔滨医科大学第二附属医院),袁祖贻(西安交通大学医学院第一附属医院),苑海涛(山东省立医院),张佳胤(上海市第一人民医院),张龙江(中国人民解放军东部战区总医院),张亚琴(中山大学附属第五医院),张兆琪(首都医科大学附属北京安贞医院),郑敏文(中国人民解放军空军军医大学第一附属医院) 参考文献:略 END 版权声明(预发表) 为提升传播效率,《中国介入心脏病学杂志》通过预出版策略发表该专栏文章。这些预出版文章均已经过同行评议,以优先出版方式在线发表,可作为有效引用内容。由于优先发表的内容尚未完成规范的编校流程,不保证其内容与印刷版完全一致。 杂志邮箱: 投稿网址: http://zjxb.cbpt.cnki.net 编辑部电话: 《中国介入心脏病学杂志》编辑部返回搜狐,查看更多 |
【本文地址】
今日新闻 |
推荐新闻 |