2020年执业药师药事管理与法规考试真题答案及解析(配伍选择题) |
您所在的位置:网站首页 › 执业药师药事管理与法规题型 › 2020年执业药师药事管理与法规考试真题答案及解析(配伍选择题) |
2020年执业药师药事管理与法规考试真题答案及解析(配伍选择题)
|
摘要:2020年执业药师考试药事管理与法规真题答案及解析已更新,本文为2020年执业药师考试药事管理与法规配伍选择题真题答案及解析,2020年执业药师考试药事管理与法规完整真题及答案可在执业药师频道首页真题专题中查看。 2020年执业药师药事管理与法规配伍选择题真题答案及解析如下: 配伍选择题(共60题,每题1分。题干分为若干组,每组题目对应同一组备选项,备选项可重复选用,也可不选用,每题只有一个选项最符合题意) 【41~42】 A. 国药准字S + 4位年号 + 4位顺序号 B. 国药准字H + 4位年号 + 4位顺序号 C. J + 4位年号 + 4位顺序号 D. 国药准字HJ + 4位年号+ 4位顺序号 41、境内生产的生物制品的批准文号格式是( ) 42、境外生产的化学药品的批准文号格式是( ) 【43~44】 A. 药品生产企业 B. 药品经营企业 C. 临床试验机构伦理委员会 D. 药物安全性评价中心 43、应当设立或指定负责药品不良反应报告和监测的机构并配备专(兼)职人员的是( ) 44、应当设立专门负责药品不良反应报告和监测的机构并配备专职人员的是( ) 【45~47】 A. 阿托品 B. 咖啡因 C. 布桂嗪 D. 氯胺酮 根据《麻醉药品和精神药品管理条例》 45、邮寄时需要预先办理准予邮寄证明,托运时需要预先办理运输证明的麻醉药品是( ) 46、邮寄时需要预先办理准予邮寄证明,托运时需要预先办理运输证明的精神药品是( ) 47、邮寄时需要预先办理准予邮寄证明,托运时无需预先办理运输证明的精神药品是( ) 【48~50】 A. 慎重经验用药 B. 参照药敏试验结果选用 C. 及时将预警信息通报本机构医务人员 D. 暂停对此目标细菌的临床应用 根据《抗菌药物临床应用管理办法》 48、对主要目标细菌耐药率超过50%的抗菌药物,医疗机构应采取的细菌耐药预警机制和措施是( ) 49、对主要目标细菌耐药率超过40%的抗菌药物,医疗机构应采取的细菌耐药预警机制和措施是( ) 50、对主要目标细菌耐药率超过30%的抗菌药物,医疗机构应采取的细菌耐药预警机制和措施是( ) 【51~53】 A. 单味罂粟壳 B. 复方磷酸可待因溶液 C. 按非处方药管理的含麻黄碱类复方制剂 D. 复方甘草片 51、药品零售企业应当查验购买者身份证并对姓名和身份证号予以登记的是( ) 52、不属于麻醉药品和精神药品,但按处方药管理,药品零售企业必须凭处方调剂的是( ) 53、按第二类精神药品管理,必须凭精神药品专用处方才能调剂的是( ) 【54~55】 A. 医疗用毒性药品 B. 含麻黄碱类复方制剂 C. 免疫规划疫苗 D. 含兴奋剂药品 54、加强A型肉毒毒素的监督管理,将其列入的管理类别是( ) 55、在药品包装和标签上,无需印制特定字样或专有标识的是( ) 【56~58】 A. 混淆行为 B. 侵犯商业秘密行为 C. 虚假宣传和虚假交易行为 D. 诋毁商誉行为 根据《反不正当竞争法》 56、某药品零售连锁企业安排“网络水军”为其销售的商品生成不真实的网络销量数据和“用户好评”,该“刷单炒信”的行为属于( ) 57、某药品生产企业听说有医疗机构通过不良反应监测系统报送了其争对手生产的药品的不良反应信息,未经证实即通过公众媒体发布信息,声称其竞争对手生产的药品不符合药品标准,该行为属于( ) 58、某药品生产企业研制部门负责人未经企业同意,将企业在研药物的临床研究数据披露给开展相同品种研制的其他药品生产企业,该行为属于( ) 【59~60】 A. 具有执业药师资格和3年以上药品经营质量管理工作经历 B. 具有大学本科以上学历,执业药师资格和3年以上药品经营质量管理工作经历 C. 具有中药学中级以上专业技术职称 D. 具有中药学初级以上专业枝术职称 59、中药饮片批发企业质量管理部门负责人的资质要求是( ) 60、中药饮片批发企业中药材验收人员的资质要求是( ) 【61~62】 A. 【警示语】 B. 【禁忌】 C. 【规格】 D. 【药品名称】 根据《药品说明书和标签管理规定》 61、列出药品不能应用的各种情形,包括禁止应用该药的人群、疾病等的药品说明书项目是( ) 62、含有化学药品的中药复方制剂,其处方药说明书中应注明“本品含×××(化学药品通用名称)”的药品说明书项目是( ) 【63~65】 A. 3个月 B. 1年 C. 5年 D. 3年 63、《药品类易制毒化学品购用证明》的有效期是( ) 64、《麻醉药品、第一类精神药品运输证明》的有效期是( ) 65、《药品经营许可证》的有效期是( ) 【66~68】 A. 法律 B. 行政法规 C. 规范性文件 D. 部门规章 66、《药品经营质量管理规范》的法律层级属于 ( ) 67、《药品生产监督管理办法》的法律层级属于 ( ) 68、《医疗用毒性药品管理办法》的法律层级属于 ( ) 【69~71】 A. 道地药材 B. 鲜用药材 C. 野生或半野生药用动植物 D. 自采自种自用中草药 69、产自特定区域,比其他地区的同种中药材品质和疗效更好的是( ) 70、不得加工成中药制剂的是( ) 71、采集应坚持“最大持续产量”原则的是( ) 【72~73】 A. 通用名称 B. 商品名称 C. 驰名商标 D. 注册商标 根据《药品、医疗器械、保健、特殊医学用途配方食品广告审查管理暂行办法》 72、药品广告中严禁出现的文字是( ) 73、药品广告中必须标明的内容是( ) 【74~75】 A. 不予核发药品生产许可证 B. 注销药品生产许可证 C. 补发药品生产许可证 D. 不予再注册 74、对药品生产许可证有效期届满未重新发证的,应当( ) 75、对在药品再注册申请时,经上市后评价,属于疗效不确切、不良反应大或者因其他原因危害人体健康的药品,应当( ) 【76~78】 A. 制剂及其成分的研究充分,结果明确,安全性良好 B. 用药对象明确,适应症或功能主治明确 C. 作为处方药使用时的安全性 D. 涉及运动员、儿童等人群用药,应有明确的安全性指示 76、非处方药的有效性具有的特点包括( ) 77、非处方药的安全性评价包括( ) 78、申请处方药转换为非处方药的基本要求包括( ) 【79~80】 A. 所有抗菌药物 B. 所有中药注射剂 C. 所有终止妊娠药品 D. 所有生物制品 79、药品零售企业必须凭处方销售的是( ) 80、药品零售企业严格禁止销售的是( ) 【81~83】 A. 行政许可 B. 行政处罚 C. 行政复议 D. 行政强制 81、药品监督管理部门查封生产假药的场所和设施,属于( ) 82、行政相对人对药品监督管理部门作出的没收违法所得决定不服时,可以提出( ) 83、药品监督管理部门颁发《药品生产许可证》,属于( ) 【84~85】 A. 责令改正,给予警告 B. 责令停业整顿 C. 处十万元以上五十万元以下的罚款 D. 责令暂停销售 根据《药品管理法》 84、未按照规定开展药品上市后研究或上市后评价的行为,经警告,逾期不改正的,应承担的行政法律责任为( ) 85、药品经营企业零售药品未正确说明用法、用量等事项时,应承担的行政法律责任为( ) 【86~88】 A. 有效期后2年 B. 3年 C. 一直 D. 不少于5年 86、从事医疗器械网络销售的企业,对无有效期的非植入类医疗器械销售记录的保存期限是( ) 87、从事医疗器械网络销售的企业,对有有效期的非植入类医疗器械销售记录的保存时限是( ) 88、从事医疗器械网络销售的企业,对植入类医疗器械销售记录的保存时限是( ) 【89~90】 A. 药品监督管理局药品注册司 B. 药品监督管理局药品审评中心 C. 药品监督管理局行政事项受理服务和投诉举报中心 D. 省级药品监督管理部门 89、负责境外生产药品再注册审评工作的部门是( ) 90、负责境内生产药品再注册申请的受理、审查和审批的部门是( ) 答案及解析: 【41~42】A、D 【试题解析】本题考查药品审评审批。 药品批准文件
H代表化学药品,Z代表中药,S代表生物制品。 境内生产的生物制品的批准文号格式:国药准字S+4位年号+4位顺序号。 境外生产的化学药品的批准文号格式:国药准字HJ+4位年号+4位顺序号。 B选项为境内生产的化学药的批准文号格式。C选项为干扰项。故本题选A、D。 【43~44】B、A 【试题解析】本题考查药品不良反应报告和处置。 药品经营企业应当设立或指定负责药品不良反应报告和监测的机构并配备专(兼)职人员。 药品生产企业应当设立专门负责药品不良反应报告和监测的机构并配备专职人员。 CD选项为干扰项。故本题选B、A。 【希赛点拨】 药品不良反应报告主体、报告范围
【45~47】C、D、B 【试题解析】本题考查麻醉药品和精神药品目录。 麻醉药品和精神药品目录
麻醉药品和精神药品邮寄时需要预先办理准予邮寄证明,麻醉药品和第一类精神药品托运时需要预先办理运输证明,第二类精神药品托运时无需预先办理运输证明。 阿托品属于医疗用毒性药品,咖啡因属于第二类精神药品,布桂嗪属于麻醉药品,氯胺酮属于第一类精神药品。 托运时需要预先办理运输证明的麻醉药品是布桂嗪;托运时需要预先办理运输证明的精神药品是氯胺酮;托运时无需预先办理运输证明的精神药品是咖啡因。故本题选C、D、B。 【48~50】B、A、C 【试题解析】本题考查抗菌药物应用管理。
对主要目标细菌耐药率超过50%的抗菌药物,医疗机构应参照药敏试验结果选用。 对主要目标细菌耐药率超过40%的抗菌药物,医疗机构应慎重经验用药。 对主要目标细菌耐药率超过30%的抗菌药物,医疗机构应预警信息通报本医疗机构医务人员。 故本题选B、A、C。 【51~53】C、D、B 【试题解析】本题考查含特殊药品复方制剂的管理。 含特殊药品复方制剂的管理
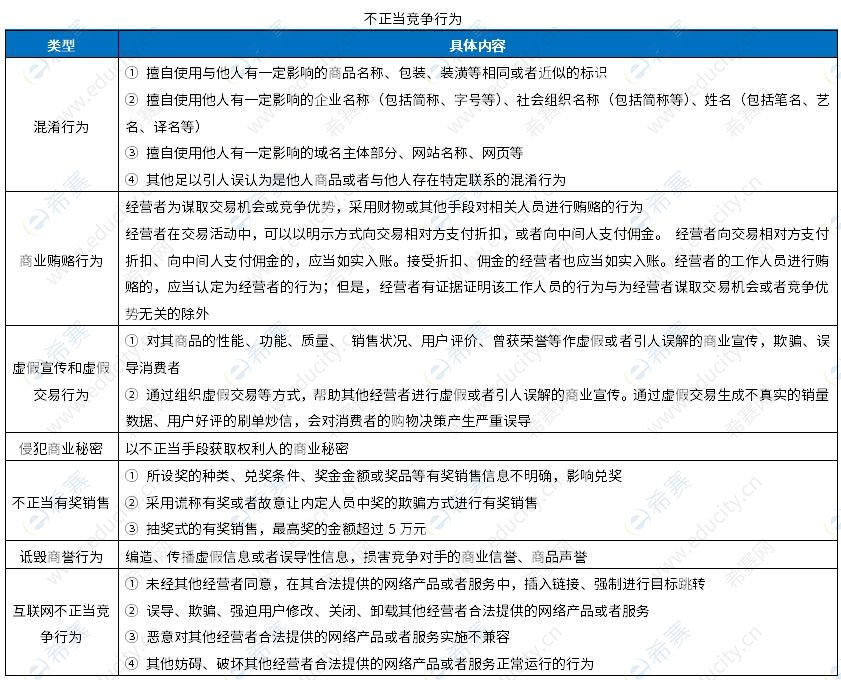
药品零售企业销售含麻黄碱类复方制剂,应查验购买者身份证,并对其姓名和身份证号码予以登记。 复方甘草片不属于麻醉药品和精神药品,但按处方药管理。 含可待因复方口服液体制剂管理:列入第二类精神药品管理,凭医疗机构开具的精神药品专用处方销售。 A选项罂粟壳为麻醉药品。故本题选C、D、B。 【54~55】A、B 【试题解析】本题考查医疗用毒性药品管理、含特殊药品复方制剂的管理。 A型肉毒毒素列入医疗用毒性药品的管理。 含麻黄碱类复方制剂无需印制特定字样或专有标识。 C选项有专有标识,D选项药品中含有兴奋剂目录所列禁用物质的,在包装标识或者产品说明书上注明“运动员慎用”字样。 故本题选A、B。 【希赛点拨】专有标识  【56~58】C、D、B 【试题解析】本题考查不正当竞争行为。
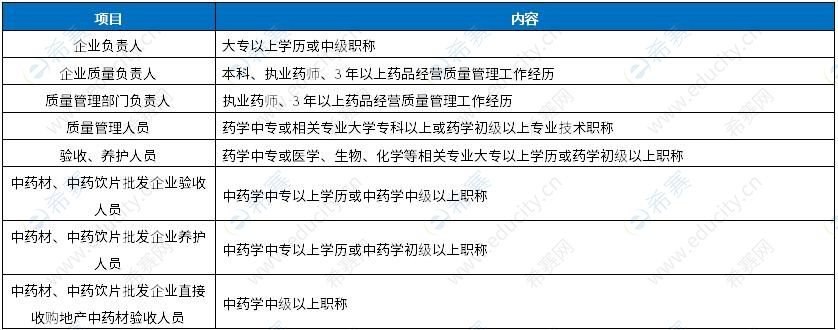
通过组织虚假交易等方式,帮助其他经营者进行虚假或者引人误解的商业宣传。通过虚假交易生成不真实的销量数据、用户好评的刷单炒信,会对消费者的购物决策产生严重误导属于虚假宣传和虚假交易行为。 编造、传播虚假信息或者误导性信息,损害竞争对手的商业信誉、商品声誉属于诋毁商誉行为。 以不正当手段获取权利人的商业秘密属于侵犯商业秘密行为。 故本题选C、D、B。 【59~60】A、C 【试题解析】本题考查药品经营质量管理规范。 药品经营质量管理规范的批发企业人员资质
中药饮片批发企业质量管理部门负责人的资质要求是具有执业药师资格和3年以上药品经营质量管理工作经历。B选项易混淆,B选项为企业质量负责人的资质要求。 中药饮片批发企业中药材验收人员的资质要求是具有中药学中级以上专业技术职称。D选项为干扰项。 故本题选A、C。 【61~62】B、A 【试题解析】本题考查药品说明书管理规定。 【禁忌】项下列出药品不能应用的各种情形,包括禁止应用该药的人群、疾病等。 【警示语】下列出含有化学药品的中药复方制剂,其处方药说明书中应注明“本品含×××( 化学药品通用名称 )”。 故本题选B、A。 【希赛点拨】 药品说明书要点
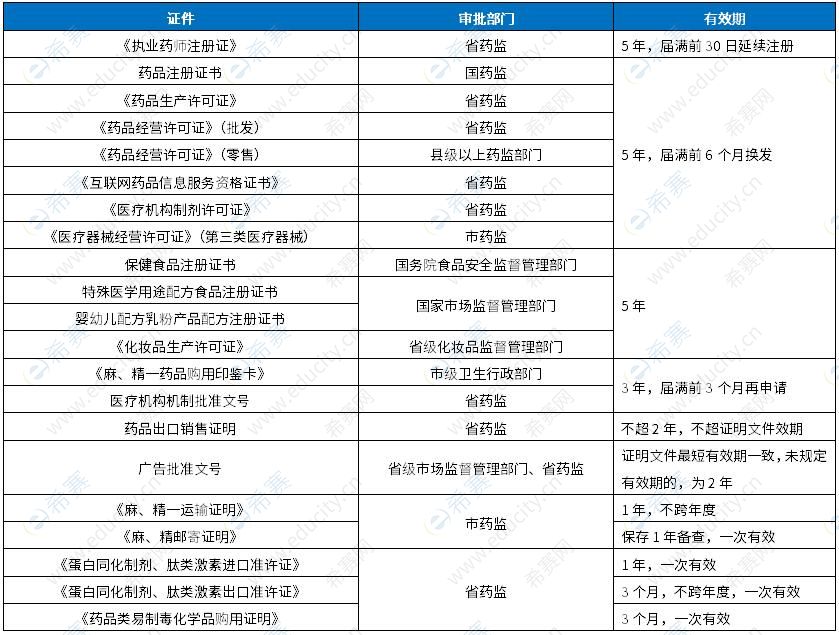
【63~65】A、B、C 【试题解析】本题考查麻醉药品和精神药品管理、药品类易制毒化学品的管理。 《药品类易制毒化学品购用证明》的有效期是3个月。 《麻醉药品、第一类精神药品运输证明》的有效期是1年。 《药品经营许可证》的有效期是5年。 故本题选A、B、C。 【希赛点拨】相关证件的审批部门及有效期总结
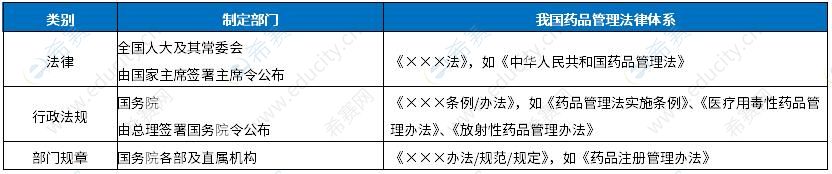
【66~68】D、D、B 【试题解析】本题考查我国药品管理法律体系和法律关系。 法律渊源
《药品经营质量管理规范》的法律层级属于部门规章。 《药品生产监督管理办法》的法律层级属于部分规章。 《医疗用毒性药品管理办法》的法律层级属于行政法规。 注意除了《医疗用毒性药品管理办法》、《放射性药品管理办法》,一般行政法规为《×××条例》。 故本题选D、D、B。 【69~71】A、D、C 【试题解析】本题考查中药材的生产、经营和使用管理。 道地中药材是指经过中医临床长期应用优选出来的,产地特定地域,与其他地区所产同种中药材相比,品质和疗效更好,且质量稳定,具有较高知名度的中药材。 乡村中医药技术人员自种自采自种的中草药,只限于其所在的村医疗机构内使用,不得上市流通,不得加工成中药制剂。 野生或半野生药用动植物的采集应坚持“最大持续产量”原则,“最大持续产量”即不危害生态环境,可持续生产(采收)的最大产量。 B选项为干扰项。故本题选A、D、C。 【希赛点拨】 中药材自种、自采、自用的管理 ① 定义:乡村中医药技术人员自己种植、采收、使用,不需特殊加工炮制的植物中草药。 ② 条件:熟悉中草药知识和栽培、具有中草药辨识能力;熟练掌握中医基本理论、技能和自种自采中草药的性味功用、临床疗效、用法用量、配伍禁忌、毒副作用等。 ③ 不得自种自采自用情形:规定需特殊管理的医疗用毒性中草药、麻醉药品原植物、濒稀野生植物药材。 ④ 其他:只限于其所在的村医疗机构内使用;不得上市流通,不得加工成中药制剂。 【72~73】C、A 【试题解析】本题考查药品广告的审查和发布。 药品标签
药品广告中严禁出现驰名商标。药品广告中必须标明通用名称。BD选项为干扰项。故本题选C、A。 【74~75】B、D 【试题解析】本题考查药品生产许可。 药品生产许可证管理
对药品生产许可证有效期届满未重新发证的,应当注销药品生产许可证。 对在药品再注册申请时,经上市后评价,属于疗效不确切、不良反应大或者因其他原因危害人体健康的药品,应当不予再注册。AC选项为干扰项。故本题选B、D。 【76~78】B、A、C 【试题解析】本题考查非处方药注册和转换制度。 处方药转换为非处方药安全性及有效性评价
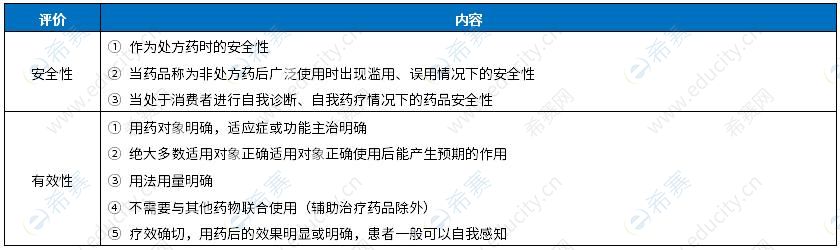
非处方药的有效性具有的特点包括用药对象明确,适应症或功能主治明确。 非处方药的安全性评价包括制剂及其成分的研究充分,结果明确,安全性良好。 申请处方药转换为非处方药的基本要求包括作为处方药使用时的安全性。 D选项为干扰项。故本题选B、A、C。 【79~80】A、C 【试题解析】本题考查处方药与非处方药的经营管理。
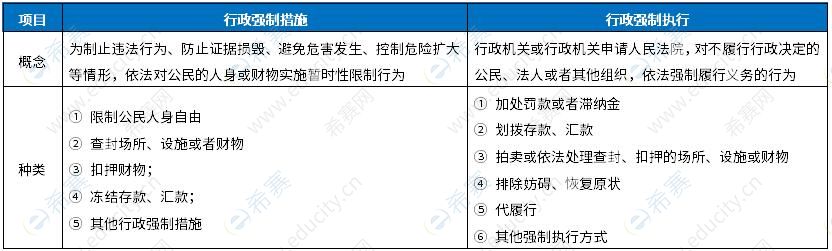
所有注射剂药品零售企业必须凭处方销售。 所有终止妊娠药品药品零售企业严格禁止销售。 BD选项为干扰项。故本题选A、C。 【81~83】D、C、A 【试题解析】本题考查药品监督管理行政法律制度。 药品监督管理部门查封生产假药的场所和设施,属于行政强制。 行政相对人对药品监督管理部门作出的没收违法所得决定不服时,可以提出行政复议。 药品监督管理部门颁发《药品生产许可证》,属于行政许可。 B选项行政处罚包括:警告、罚款、没收非法财物、没收违法所得、责令停产停业、暂扣或吊销有关许可证等。 故本题选D、C、A。 【希赛点拨】 行政强制措施与行政强制执行
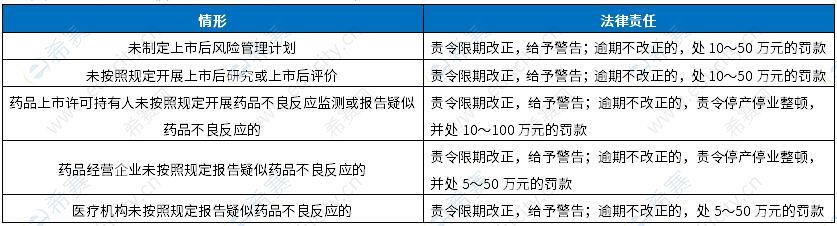
【84~85】C、A 【试题解析】本题考查违反药品上市后管理规定的法律责任。
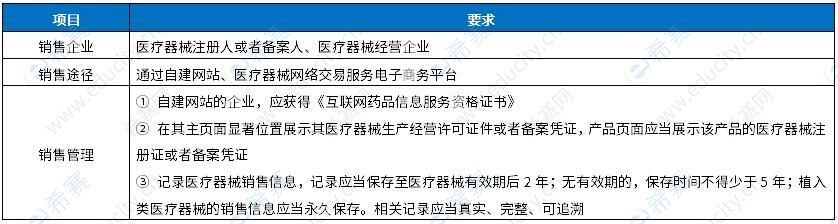
未按照规定开展药品上市后研究或上市后评价的,责令限期改正,给予警告;逾期不改正的,处10~50万元的罚款。 经营企业购销药品未按照规定记录,零售企业未正确说明用法、用量等事项,或者未按照规定调配处方的,责令改正,给予警告;情节严重的,吊销药品经营许可证。 BD为干扰项。故本题选C、A。 【86~88】D、A、C 【试题解析】本题考查医疗器械经营与使用管理。 医疗器械网络销售监督管理要求
从事医疗器械网络销售的企业记录医疗器械销售信息,记录应当保存至医疗器械有效期后2年;无有效期的,保存时间不得少于5年;植入类医疗器械的销售信息应当一直保存。故本题选D、A、C。 【89~90】B、D 【试题解析】本题考查药品审评审批。 药品注册证书有效期5年;持有人应当在药品注册证书有效期届满前6个月申请再注册。境内生产药品再注册申请由持有人向其所在地省级药监部门提出。境外生产药品再注册申请由持有人向药品审评中心提出。AC选项为干扰项。故本题选B、D。 【希赛点拨】 不予再注册的情形: ① 有效期届满前未提出再注册申请的; ② 药品注册证书有效期内持有人不能履行持续考察药品质量、疗效和不良反应责任的; ③ 未在规定时限内完成药品批准证明文件和药品监督管理部门要求的研究工作且无合理理由的; ④ 经上市后评价,属于疗效不确切、不良反应大或者因其他原因危害人体健康的; ⑤ 法律、行政法规规定的其他不予再注册情形。 相关推荐: 执业药师职业资格考试介绍 执业中药师视频课程 执业西药师视频课程 |
【本文地址】
今日新闻 |
推荐新闻 |