丽珠集团深度:主业多元稳健发展,创新性微球及生物制剂打开第二增长【东吴医药朱国广/周新明团队】 |
您所在的位置:网站首页 › 奥曲肽微球是化疗药吗 › 丽珠集团深度:主业多元稳健发展,创新性微球及生物制剂打开第二增长【东吴医药朱国广/周新明团队】 |
丽珠集团深度:主业多元稳健发展,创新性微球及生物制剂打开第二增长【东吴医药朱国广/周新明团队】
|
盈利预测与投资评级:我们预计,2023-2025年,公司归母净利润为 21.6/24.4/27.9亿元,对应当前市值的PE为 15/13/11倍。考虑公司创新属性新品落地将带来较快业绩增速+复杂制剂及独家专利产品壁垒较高、主营业务增长稳健,且公司当前估值较低,首次覆盖给予“买入”评级。 风险提示:产品降价、新药研发、原材料供应和价格波动、医药政策不确定性风险。
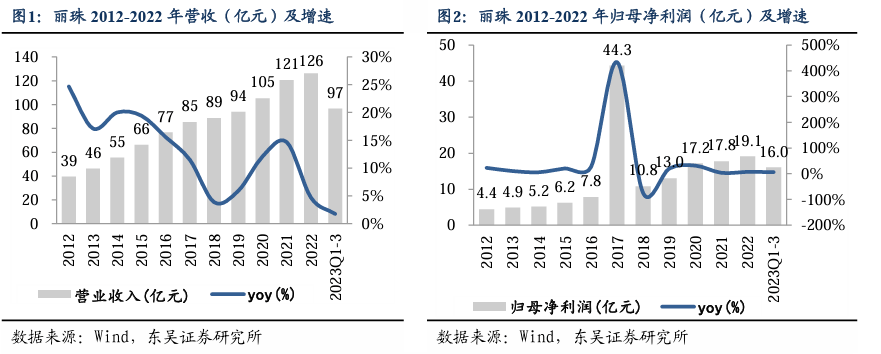
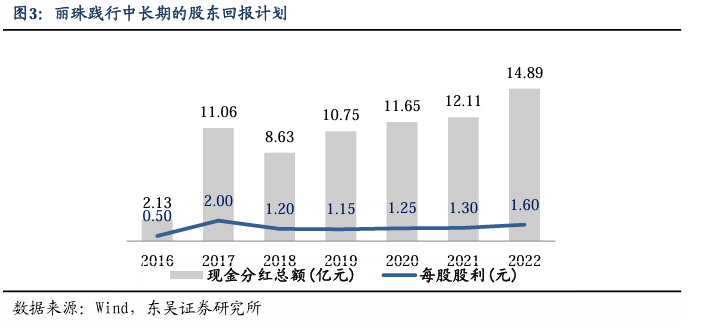
1. 投资逻辑:高分红+低估值,主营稳健发展+创新加速兑现 一、集团企业稳健发展,多维度盈利数据持续发力,员工激励更添信心。1)营收、利润双增长。2020-2023Q3即使受到疫情+政策波动,分别实现收入105.2/120.6/126.3/96.6亿元,同增12.1/14.7/4.7/1.8%,6年CAGR为8.71%;归母净利润17.2/17.8/19.1/11.7亿元,同增31.6/3.5/7.5/5.1%,6年CAGR为15.99%。业绩稳健放量,主要是受益于微球等高壁垒产品的研发能力及竞争优势,质量、成本、营销体系多方面的精细化管理,多元化的产品结构和业务布局等因素。2)合伙人计划+股票期权激励+股份回购增添投资者信心。(A)2020年,公司发布中长期事业合伙人持股计划,以2018年扣非归母净利润9.47亿元为基数,考核2019-2028年的净利润复合增长率,实行超额累进计提各期激励基金,具体计提比例见下表。2021、2022年分别实施了第一期、第二期持股计划。(B)2022年,公司发布股票期权激励计划,拟向1,026名激励对象授予1,797万份股票期权,占总股本比例1.92%,激励对象主要为中高级管理人员及核心骨干;以2021年扣非归母净利润为基础,考核2022-2024年的净利润复合增长率不低于15%。(C)截至2023年,公司通过集中竞价回购了A股股份1.16千万股,占总股本的1.24%,使用资金4.02亿元,全部回购股份予以注销并相应减少注册资本。公司与股东及核心员工利益深度绑定,组织架构稳定性强,注重股东利益,增强投资者信心。3)卓越管理:中国首家MSCI ESG3A级药企,构建可持续发展的全球使命。2023年MSCI ESG评级由2A级上调至全球最高等级3A级,成为中国制药行业中首家获得最高3A评级的企业;截至2023年8月评级更新日,全球制药行业中仅有4家企业获得MSCI ESG的最高评级3A级。
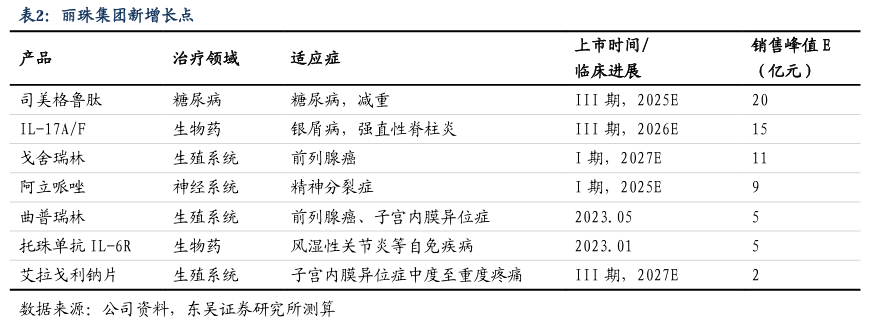
二、高股息、低估值。公司治理良好,践行中长期的股东回报计划,十年累计分红75亿元,近5年股息高达2.27-4.57%。
三、微球制剂及生物制品收获期,驱动业绩新增量。由传统化药企业向高壁垒复杂制剂及创新生物药转型,2023-2025管线布局加速兑现。1)司美格鲁肽糖尿病适应症正在进行III期临床试验,预计24Q2报产,且减重适应症23年12月递交IND,不仅临床进展领先,而且具备其原料药自主生产的能力,我们预计有望成为20亿元大品种。2)IL-17A/F单抗的III期临床有序推进,其适应症银屑病和强直性脊柱炎分别对应我国患病人数570万和560万人,市场辽阔,双靶抑制剂疗效突出,目前全球IL-17A/F双效抑制剂仅有一款上市,丽珠有望成为国内首款获批,成为15亿品种。3)戈舍瑞林缓释植入剂正在开展中试向生产的桥接试验,曾是阿斯利康独家超35亿市场的大品种,上市后将协同完善丽珠的促性激素市场管线矩阵,有望抢占30%的市场,达到销售峰值11亿元。4)阿立哌唑长效剂型已经完成I期临床试验,2023Q3上市许可申请获得受理,预计2025年上市;该产品机理独特,顺应性强,临床需求明确;国内抗精神病药市场规模约35亿元,相比竞争较激烈的口服制剂,注射剂涉足药企仅3家,我们预计2028年达到销售峰值8.5亿元。5)丽珠曲普瑞林微球为国内首批,2023年5月获批前列腺癌适应症,率先进入市场;市场规模约15亿元,国产制剂尚无竞争,有望快速实现进口替代,成为5亿品种。6)IL-6R托珠单抗于2023年迅速获批用于新冠抗疫,预期后续持续用于类风湿关节炎等自免疾病,成为5亿品种。
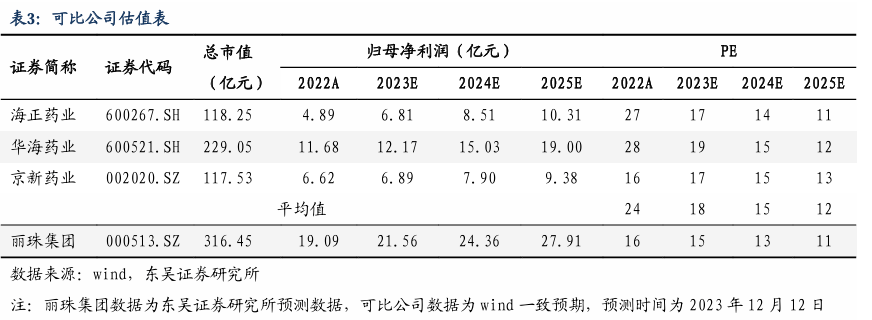
我们预计2023-2025年,公司营业收入分别为132.2/143.1/159.3亿元,归母净利润为21.6/24.4/27.9亿元,对应当前市值的PE为15/13/11倍。选择与公司业务相近的海正药业、华海药业、京新药业作为可比公司,考虑到公司创新属性新品落地带来业绩增速快+复杂制剂及独家专利产品壁垒较高、主营业务增长稳健,且公司当前估值较低、创新属性尚未完全体现,首次覆盖,给予“买入”评级。
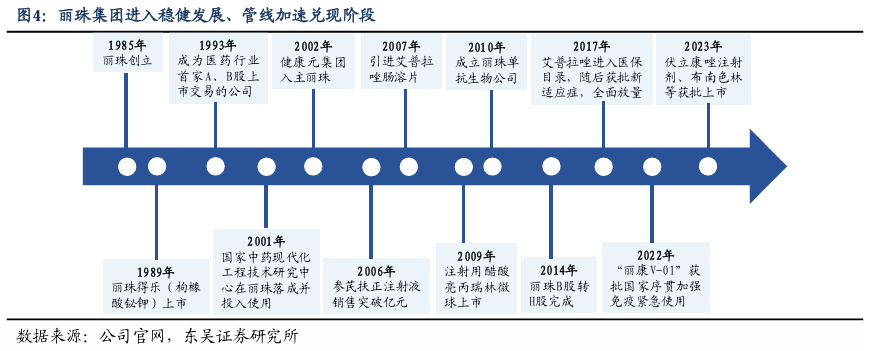
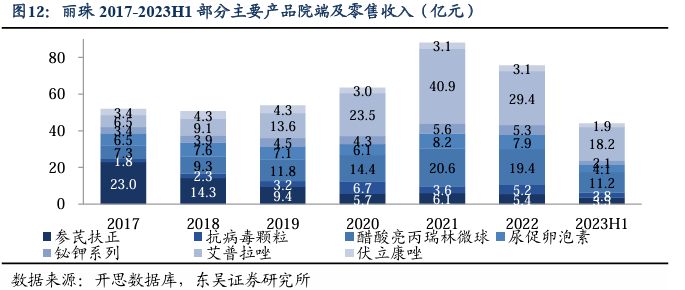
2. 丽珠集团:转型创新药及高壁垒复杂制剂的综合医药集团 2.1. 公司概况:成立近四十年,是高壁垒微球制剂及促性激素领域龙头 丽珠医药集团股份有限公司是集医药研发、生产、销售为一体的综合性企业集团,全国医药行业首家A、B股上市的公司。集团架构方面,丽珠集团创建于1985年1月,1993年在A、B股先后上市,2002年由健康元(原太太药业)收购,2014年丽珠B股转H股完成。产品方面,早期主要依赖于胃酸相关治疗(得乐、维三联等)及参芪扶正注射液等产品;第二阶段,进入高壁垒复杂制剂大品种放量阶段,2007年引进艾普拉唑并于2017年进入医保目录后全面放量,2009年亮丙瑞林上市并在2019年成为销量冠军;2020年进入抗疫阶段,新冠试剂盒陆续上市,抗病毒颗粒增长迅猛,艾普、亮丙均破10亿并成为公司高速增长的引擎;未来,将持续向高端制剂及生物创新药转型,强化辅助生殖、消化系统疾病,进军精神疾病等蓝海领域,配合股权激励注入活力,目标在充满变革及机遇的医药行业后疫情时代稳健发展。
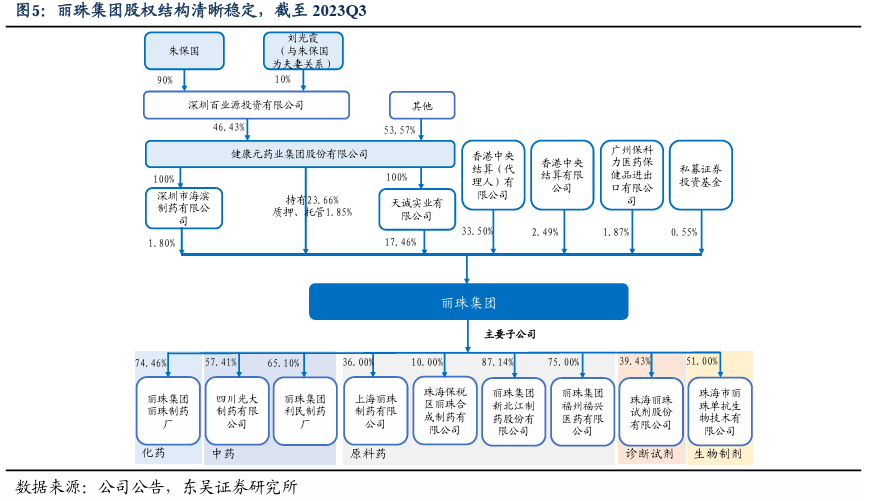
股权结构清晰稳定。截至2023Q3,健康元直接及间接持有丽珠集团44.77%股本权益,为丽珠的控股股东;朱保国担任健康元及丽珠集团的董事长,总计直接及间接持有丽珠33.07%股份,为公司实际控制人。副董事长陶德胜、董事徐国祥、执行董事及总裁唐阳刚分别直接持有公司股份0.10%、0.10%、0.05%。丽珠集团拥有25家全资子公司,26家控股子公司,业务范围涵盖医药研发、生产、销售等领域。其中,丽珠集团直接持有丽珠生物51.00%股权,丽珠生物直接持有丽珠单抗100%股权。
管理层经验丰富。公司管理层均有十年以上医药行业从事经验,对行业有深刻的理解认知。高级管理人员多数具有化学、管理学等相关学位及医药行业相关背景,行业熟悉度高,管理专业性强。
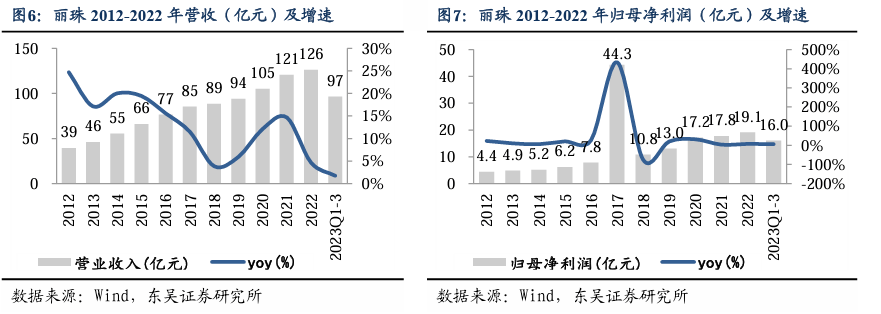
营收增长稳健,净利润增长较快。2016-2022年,公司营收由76.5亿元增至126.3亿元,6年CAGR为8.71%;归母净利润由2016年的7.8亿元增至2022年的19.1亿元,6年CAGR为15.99%。2017年,净利润大幅增长是由于处置珠海维星实业子公司股权的投资收益。2018年,营收及归母净利润增速下降,主要系医保控费、招标降价等政策调整影响。2021年,营收同比增长达14.7%,之后随着国内行业监管与准入政策趋严的大环境,增速有所放缓;但整体规模效应依旧显著,保持稳健增长。
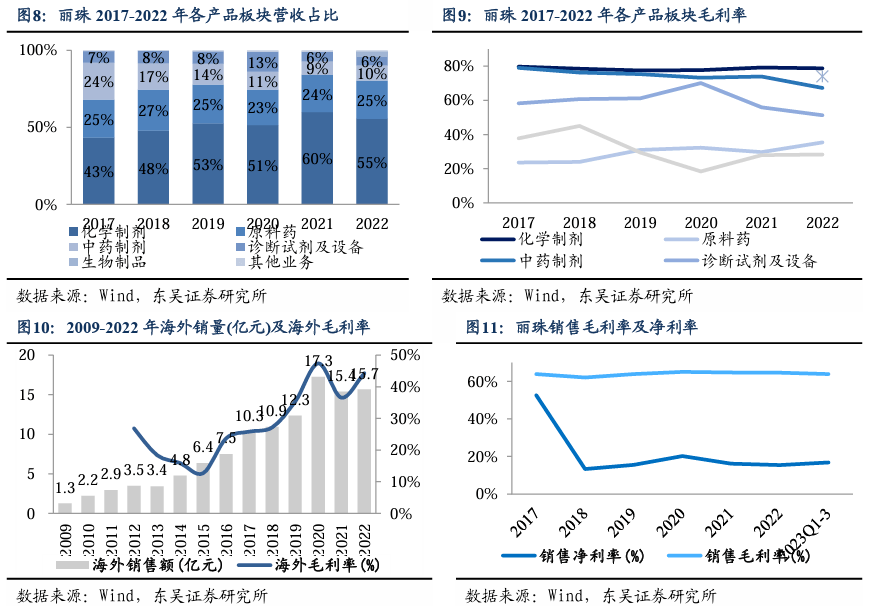
高端化学制剂及原料药境内外销售带动利润增长。2023Q3,按主要业务领域或药品划分为三大块,以化学制剂类产品为主(占营收比55%),其中创新药及高壁垒复杂制剂占比35%,以及原料药板块(占营收比25%)和中药板块(占营收比10%)。化学制剂板块包括传统仿制化药及高壁垒复杂制剂,近年来毛利率维持在80%左右;随着化学制剂的营收占比从约40%稳定至55%左右,公司利润结构优化。原料药板块的高端抗生素及高端宠物药产品销售占比及盈利也稳步提升,2017-2022年毛利率由23.6%增至35.4%,带动海外销量由2012年的3.47亿元增长至2022年的15.65亿元,十年CAGR为16.3%。2022年,公司境外主营业务收入占比12.9%;境外业务增收更增利,目前毛利率稳定在40%左右。近5年来,公司整体毛利率维持约65%,净利率近20%。
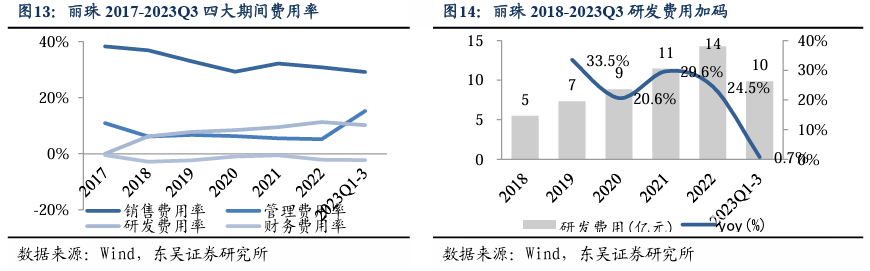
销售及管理费用降低,研发投入增加。2017-2023Q3,公司销售、管理费用呈现波动下降趋势。2022年,四项费用同比+1.39%,主要系研发费用加码(+24.51%),用于新冠疫苗的研发和大规模临床试验;财务费用率下降主要是利息收入增加以及因汇率变动带来汇兑收益所致。商业化实力强劲。公司营销网络覆盖全国各省份及海外超80个国家或地区,产品覆盖国内二级以上6000余家、二级以下基层医疗终端10万余家、40多万家药店。BD团队不断加快自有项目的出海步伐:自2021的PD-1实现了公司首次创新产品海外商业化授权之后,持续推进创新类产品及管线的国际合作、申报注册、技术转移及对外许可授权等工作。
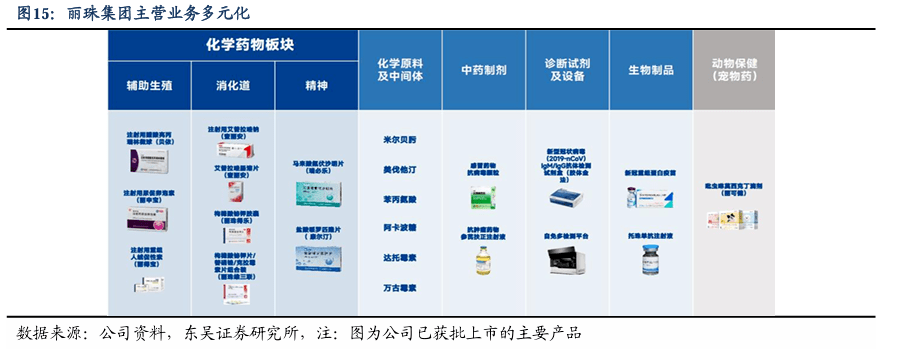
2.2. 产品概况:集中于辅助生殖、消化道、精神类疾病的多元化业务布局 丽珠集团主营业务多元化。产品涵盖化学药、生物药、中药制剂、原料药及中间体、诊断试剂及设备等多个医药细分领域,治疗领域方面集中于辅助生殖(亮丙瑞林、尿促卵泡素、尿促性素等)、消化道(艾普拉唑、铋钾系列、雷贝拉唑等)、精神类疾病(氟伏沙明等)。丽珠具备较多产品储备,拥有439项制剂批文,187项产品进入医保,155项在研产品,以及677项专利及专利申请;同时不断获得国际性药品获批注册和国内临床批准,及一致性评价项目顺利完成,新老药物进展顺利。现阶段聚焦发展创新药及高壁垒复杂制剂,并以独特的原料药优势,加强原料制剂一体化。
由传统化药企业向高壁垒复杂制剂及创新生物药企转型,2023-2025管线布局加速兑现。重点产品包括近两年获批上市的:曲普瑞林微球、注射用醋酸西曲瑞克、重组人绒促性素、IL-6R托珠单抗注射液、丽康V-01新冠疫苗、新冠二价苗、布南色林片、注射用伏立康唑、以及注射用丹曲林钠。5项准备或正在申请报产受理:阿立哌唑微球、黄体酮注射液、盐酸鲁拉西酮片、盐酸哌罗匹隆片、和PD-1抑制剂。正在推进6项III期/BE临床试验:司美格鲁肽、IL-17A/F单抗、亮丙瑞林微球(3M剂型)、奥曲肽微球、重组人促卵泡激素、和艾拉戈利钠片;5项I期临床试验:曲普瑞林微球(3M)、丙氨瑞林微球、干扰素a-2bFc、艾普拉唑微丸肠溶片、和阿塞那平贴剂。预期2024-2025年,多项催化事件有望落地,包括亮丙瑞林微球(3M)、曲普瑞林微球(1M)子宫内膜异位适应症、阿立哌唑微球、PD-1单抗、司美格鲁肽注射液、以及艾普拉唑微丸肠溶片的获批上市。
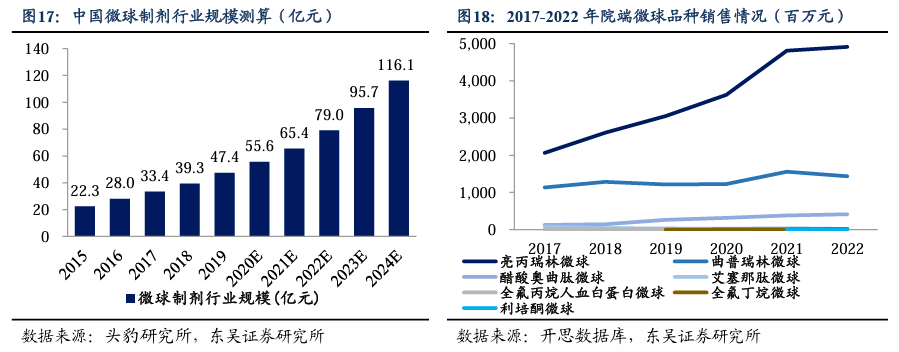
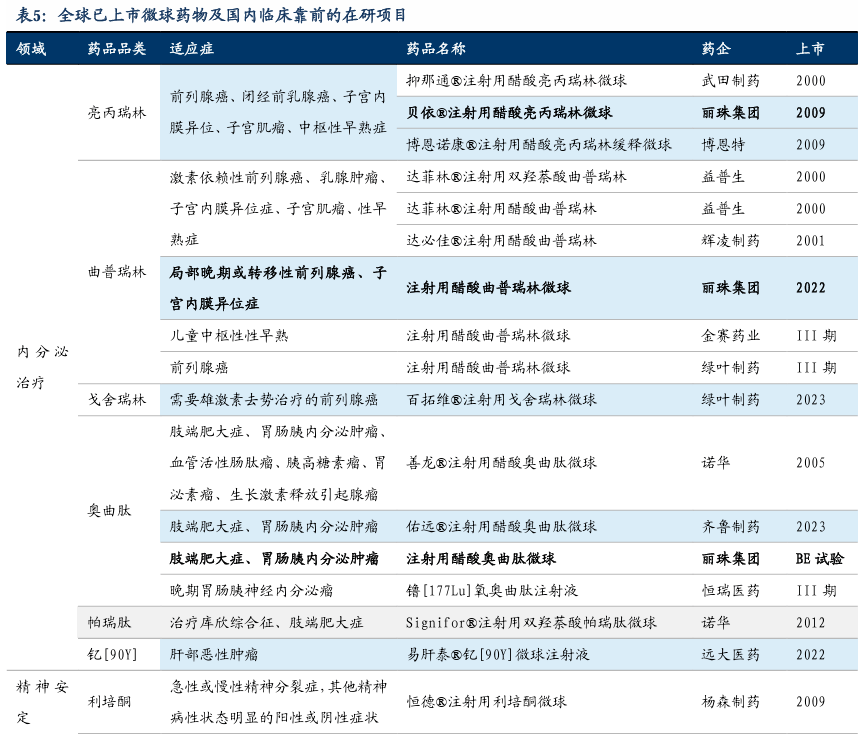
3. 长效微球高壁垒制剂领跑者,辅助生殖龙头进军精神疾病 3.1. 微球行业:抢占微球高壁垒复杂制剂的先发优势 微球作为长效注射剂的成熟品类,药物缓释特点优势显著。长效注射剂是起到缓释、长效作用的注射制剂;相比于口服制剂,血药浓度稳定、药物的有效作用时间长达数周乃至数月,可降低给药频次,从而带来患者便利性、依从性、及巨大的社会效应。长效注射给药系统可通过载体控制药物缓释速度,主要采取了微囊/微球、聚合物胶束、或纳米粒等技术。其中,微球技术的临床应用最为成熟,全球最早上市时间为1986年;截至2023Q3,全球已有18款微球产品上市,其中7款国产。微球(microspheres)将药物包埋或吸附在聚合物分子的表面,形成微小球状实体,其粒径一般在1-250微米。通过皮下或肌肉注射进入体内后载体表面快速释放、药物扩散、聚合物溶蚀降解等方式,实现药物的半衰期延迟。微球生产技术壁垒较高,全球获批上市的药企较少,因为1)药物处方工艺复杂,微球的包封率、粒径均匀性等质量参数难以控制,重复性和稳定性均有难度,产业化生产难度大;2)技术壁垒、专利、和设备等制约因素,比如全程无菌化操作,对生产过程与定制化设备的要求严格;3)研发周期较长,存在进入及资金壁垒。 微球制剂规模近120亿元,复合增速约20%,空间广阔。根据头豹研究所数据,2015-2019年中国微球制剂行业市场规模由22.3亿元增长到47.4亿元,期间CAGR为20.8%。未来,随着多个原研药专利过期,本土企业加紧布局微球制剂领域,将促进微球制剂技术水平提升,及国产微球制剂产品加速上市,中国微球制剂市场规模将呈现快速增长趋势。据头豹研究所,2024年中国微球剂行业市场规模将增长至116.1亿元,2019-2024年CAGR为19.7%。已上市的主要微球品种为亮丙瑞林、曲普瑞林和奥曲肽。目前我国微球制剂医院市场销售规模的第一梯队是亮丙瑞林微球,2022年样本医院销售额49.1亿元,销量仍处于增长阶段,是带动微球制剂发展的主要品种。在医院市场第二梯队产品中,曲普瑞林和奥曲肽的销售额总体上保持较高的增长势头,2022年样本医院销售额分别为7.32亿和1.94亿元。其余微球制剂销售额尚未过千万。
微球制剂生产的工业控制壁垒高,竞争格局好。由于微球制剂的技术壁垒,微球关键制备技术掌握在欧美日发达国家如美国强生、瑞士诺华、法国益普生、日本武田、德国辉凌等制药巨头手中;目前国内竞争环境相对温和,主要参与药企较为集中,包括丽珠集团、绿叶制药、齐鲁制药、金赛药业、和圣兆药物。截至2023Q3,按药物有效成分计,全球共12个微球产品品类上市;我国进口微球产品5个(亮丙瑞林、曲普瑞林、奥曲肽、利培酮、艾塞那肽),国产微球有5个(亮丙瑞林、曲普瑞林、利培酮、戈舍瑞林、奥曲肽以及钇[90Y])。我国研发申报的微球产品集中在内分泌治疗的GnRH类药物、精神疾病、糖尿病和肿瘤等治疗领域。根据药物临床试验登记与信息公示平台的数据显示,我国共有65款微球制剂项目在研;从产品类别来看,研发亮丙瑞林、曲普瑞林、戈舍瑞林的微球制剂项目分别有9个、7个、6个。 丽珠集团率先实现微球产业化,布局微球研发平台,占据先发优势。丽珠2013年引进微球项目平台,成立研究院化药研究所微球室;2015年获国家级研发平台“长效微球技术国家地方联合工程研究中心”称号;2017年成立丽珠微球科技,是国内最早研发、也是最为领先的微球产品企业之一。微球项目主要分布在肿瘤、辅助生殖、精神等领域。截至2023Q3,丽珠微球及缓释植入剂的在研项目共6项:1)阿立哌唑微球(1M)已于2023年9月受理报产;2)醋酸亮丙瑞林微球(3M)正在开展BE试验;3)醋酸奥曲肽微球(1M)正在开展BE试验;4)醋酸丙氨瑞林微球(1M)正在进行I期临床;5)醋酸戈舍瑞林缓释植入剂(1M)开展了中试向生产的桥接试验;6)双羟萘酸曲普瑞林微球(3M)用于晚期前列腺癌,正在筹备开展I期临床。
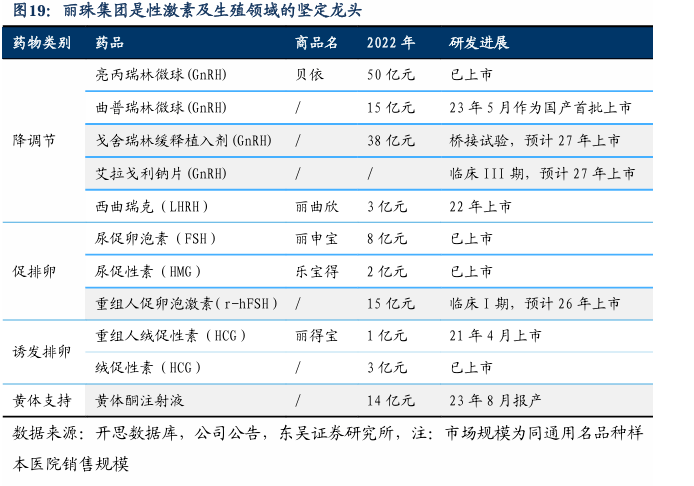
3.2. 促性领域:曲普瑞林获批上市,协同贝依®亮丙瑞林渠道放量 丽珠集团为性激素及生殖领域的坚定龙头。丽珠在促性激素领域有多款产品,主要用于辅助生殖和妇科疾病领域,除去瑞林类微球高端制剂,还有醋酸西曲瑞克、尿促卵泡素、尿促性素、和绒促性素在售。据米内网数据,2021年,性激素及生殖系统调节剂的主要销售终端的70%在中国公立医疗机构;其中,TOP5药企占据超60%的市场,其中4家为全球性跨国药企,丽珠作为5家中唯一一家中国药企,市占份额坚守TOP3,稳定保持在10%以上。
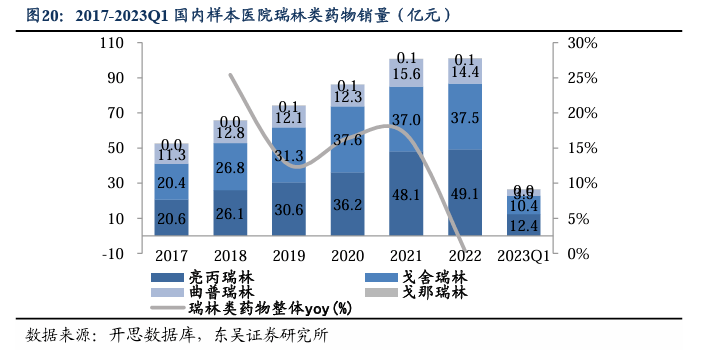
瑞林类GnRHa市场过百亿且持续扩张,近5年CAGR为14%。瑞林类药物,是以促性激素释放激素(GnRH)结构为基础的一类人工合成的多肽类药物。GnRH是下丘脑-垂体-性腺轴的重要信息分子,紧密联系神经、免疫、内分泌三大调节系统,对生殖调控具有重要意义。GnRH激动剂(GnRHa)用于治疗多种对性激素依赖疾病,包括子宫平滑肌瘤、子宫内膜异位症、乳腺癌、前列腺癌、中枢性性早熟等疾病;小剂量可用于促排卵治疗(详见附录)。瑞林类药物只能注射给药,较长的治疗周期,催化其微球长效制剂的发展。作为多肽类激素一般无法口服用药,而是采取静脉给药等注射方式,这是由于这类激素在经过人体胃肠道时,容易被肠肽酶或蛋白酶分解代谢,营销药物疗效。又因其半衰期短、治疗周期长,需要反复注射,因此市场上常用微球制剂,以延长其半衰期,降低注射频率。根据开思数据库,2017-2022年,瑞林类药物的样本医院市场空间由52.4亿元提升至101.1亿元,5年复合增速14.0%。国内常用的GnRH激动剂(GnRHa)有三种瑞林类代表药物,分别是亮丙瑞林、戈舍瑞林、和曲普瑞林,它们都有着巨大的市场,针对这三款瑞林药物丽珠集团均有布局。
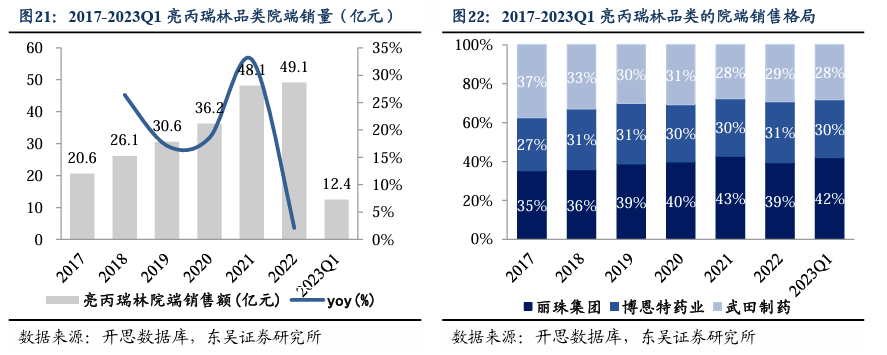
亮丙瑞林:国内销售格局三足鼎立,近年来丽珠集团博得头筹、市占率达40%。亮丙瑞林是当前GnRH品类中份额最大的品种。通过对垂体-性腺系统的抑制作用,对性激素依赖性疾病发挥作用,主要用于子宫内膜异位、前列腺癌及停经前乳癌、中枢性性早熟症等疾病治疗。丽珠的亮丙瑞林(1M)是我国最早上市的微球制剂之一,属于医保乙类,1M注射用无菌粉末(3.75mg)为1295元/支,于2009年获批上市,主要治疗子宫内膜异位、子宫肌瘤等。市场:亮丙瑞林普通制剂于1985年上市,微球制剂于1989年在美国上市,并于2000年进入我国市场。2009年,上海丽珠制药和北京博恩特药业的亮丙瑞林微球制剂产品(1M)在我国获批上市,国产微球制剂迎来历史性突破。微球剂型的上市,也推动了促性腺激素释放激素类似物的市场扩张。根据开思数据库,2017-2022年,国产亮丙瑞林入局较早,放量较快,5年复合增速18.9%,市场空间约50亿元。格局:截至2022年,国内亮丙瑞林微球制剂呈现三足鼎立的局面,主要由3家企业生产:日本武田制药、上海丽珠制药和北京博恩特药业,3家企业所占份额大致相当,丽珠占约40%的市场份额。在以亮丙瑞林为首的GnRH市场,丽珠集团不断突破,近年来市占率逐步提升,目前抢占市场头筹。丽珠优势:1)丽珠的亮丙瑞林作为国产独家,较早上市并纳入医保。2)国产品种具备价格优势。2021-2022年中标价:武田1M(3.75mg)规格的中标平均价为1595元/支,3M(11.25mg)为3925元/支;国产丽珠1M注射用无菌粉末(3.75mg)为1295元/支,博恩特1M粉针剂(3.75mg)为1273元/支。3)有望获批首款国产亮丙瑞林(3M)制剂,自2022年,正在开展生物等效性试验(CTR20222654)。亮丙瑞林3M剂型,目前我国只有武田制药成功上市销售,尚未有国产厂家实现上市。基于该产品销量基数较大+医保限价,因此,我们预计亮丙瑞林销量在未来3年将维持较为稳定的水平。
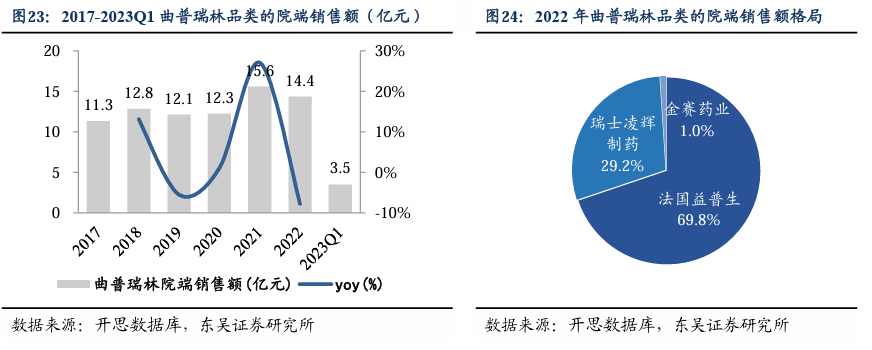
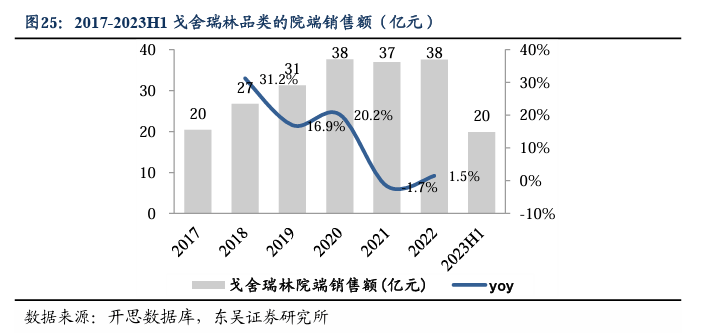
曲普瑞林:国内首批,抢占先发优势,有望快速实现进口替代。曲普瑞林获批适应症包括子宫内膜异位症、子宫肌瘤、绝经前乳腺癌、前列腺癌、性早熟。市场:全球首个微球制剂(达菲林®曲普瑞林)最早由法国益普生公司研制并于1986在法国上市,该产品1989年进入美国市场,目前在80多个国家上市;达菲林2022年全球销售额30亿法郎。根据开思数据库,国内曲普瑞林相关制剂的院内市场约15亿元。格局及优势:1)丽珠的曲普瑞林有望实现进口替代:目前法国益普生、瑞士辉凌制药市场优势较大,进口产品占据99%的市场。2)丽珠的曲普瑞林微球为国内首批,率先进入市场:国内其余获批均为曲普瑞林注射剂,微球制剂尚无其他国产产品。丽珠的注射用醋酸曲普瑞林微球,于2015年首次提交IND并获得受理,2020年启动III期(CTR20200200)并于2021年结束试验;2023年5月,以2.2类新药获批,适应症应为局部晚期或转移性前列腺癌;这是丽珠集团第2个上市的微球制剂,也是国内首个曲普瑞林微球制剂。除了丽珠的曲普瑞林微球获批,金赛药业和绿叶制药正在进行III期临床研究。其中,金赛药业已完成适应症为中枢性性早熟的临床III期试验(CTR20211679),或将成为国内、继丽珠之后的第2款曲普瑞林微球制剂。3)丽珠持续拓展适应症,子宫内膜异位症的Ⅲ期临床试验完成入组,随访也接近尾声(CTR20212632)。未来:瑞林类药物仍较有潜力,主要源于,一方面,近年来子宫肌瘤和内膜异位症等疾病有年轻化及发病率上升趋势,可能与医生及患者对该病的认识提高、女性对妇科疾病筛查的普及、腔镜手术的广泛开展有关;另一方面,未来随着人们对辅助生殖技术的认知加深、人均可支配收入提高、鼓励生育的政策放开等,中国辅助生殖渗透率的提升空间广阔。我们预计,丽珠曲普瑞林为国内首批,有望快速实现进口替代,快速抢占30%市场份额,成为5亿品种。
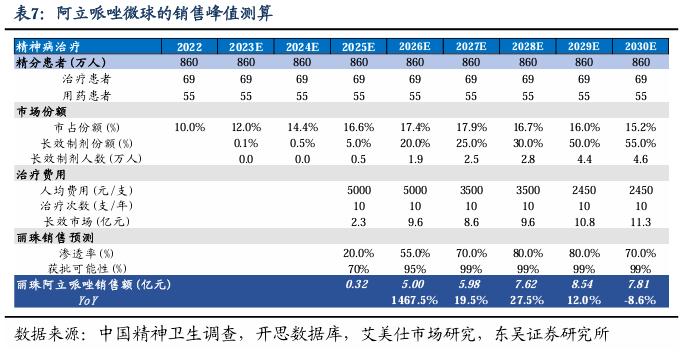
戈舍瑞林:曾是阿斯利康的独家品种,丽珠促性激素市场矩阵的协同补充。戈舍瑞林属于我国医保乙类产品,获批适应症有:晚期前列腺癌的姑息治疗,以及绝经前及围绝经期晚期乳腺癌、子宫内膜异位和子宫纤维瘤的治疗。市场:经阿斯利康市场培育,国内戈舍瑞林市场超35亿元,2022年样本医院的销售额达37.5亿元,5年CAGR为13.0%。1987年由瑞典阿斯利康开发的长效醋酸戈舍瑞林缓释植入剂(Zoladex)在英国上市,用于治疗前列腺癌;1996年3.6mg规格在中国获批上市,2012年10.8mg规格也获批进入中国,借助阿斯利康的销售及推广能力打通戈舍瑞林入院渠道。据全球畅销药数据,Zoladex销售额由2005年的10.0亿美元增长到2011年峰值的11.9亿美元,一度成为阿斯利康最畅销的肿瘤药;据IMS数据和阿斯利康财报,2022年戈舍瑞林全球销售收入超过9亿美元。格局:目前仅有两家药企上市。除了阿斯利康,2023年7月,百拓维®注射用戈舍瑞林微球获批上市,是绿叶制药自主研发的化药2.2类新药,并由绿叶制药和百济神州共同开展商业化战略合作。未来潜力:丽珠的醋酸戈舍瑞林缓释植入剂(1M)正在开展中试向生产的桥接试验,也是国产戈舍瑞林长效制剂临床进度最快之一,上市后有望跻身超35亿大市场品种,快速实现进口替代,完善丽珠的促性激素产品矩阵。我们预计,丽珠的戈舍瑞林缓释剂将于2027年上市,上市后将快速抢占30%市场份额,达成11亿元的销售峰值。
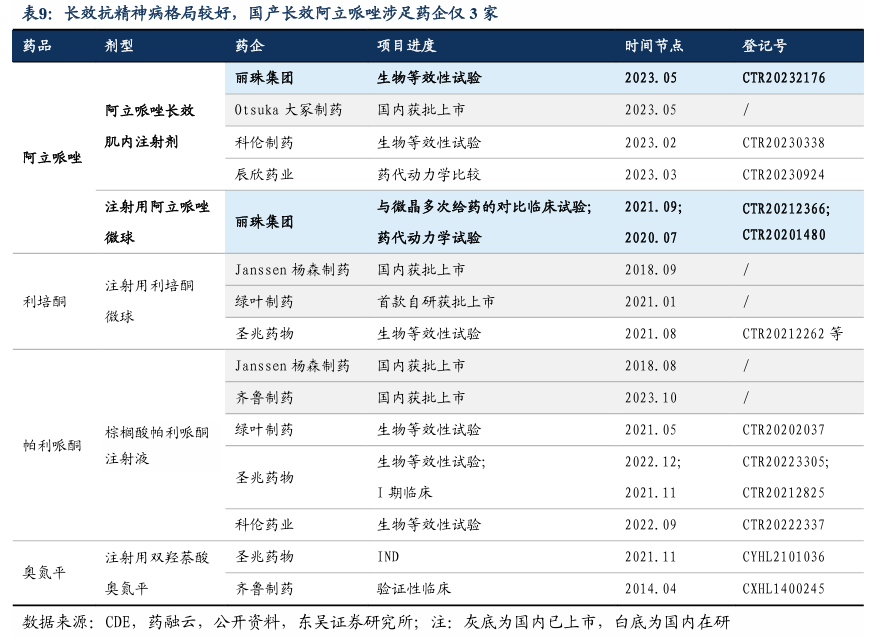
艾拉戈利钠片:产品优势:是公司自主研发的仿制药。其原研药艾拉戈克钠(Elagolix,Orilissa®)是首款也是目前上市的唯一一款口服GnRH拮抗剂,用于治疗子宫内膜异位症中度至重度疼痛。与注射剂相比,使用更为方便,患者依从性也更好;与GnRHa激动剂相比,无“点火效应”,可长时间服药,可应用于月经周期的任何阶段,停药后垂体功能可迅速恢复等优势。市场:Orilissa®于2018年获FDA批准上市;根据药融云数据,在随后2019-2021年的全球销售额为分别0.93/1.25/1.45亿美元。格局:Orilissa®于2022年收到CDE国内上市申请的受理,除此以外,目前国内尚无专用于该适应症的GnRH拮抗剂获批;相关仿制药研发还有华海药业、正大天晴、齐鲁制药等正在进行生物等效性研究。未来潜力:丽珠的艾拉戈利钠片已于2023年10月进入III期临床,预期2027年上市,除去适应症子宫内膜异位疼痛,更有望被广泛用于缓解痛经。 3.3. 精神领域:阿立哌唑微球机理+时效双重优势 价值评估:产品机理独特,长效剂型需求强,阿立哌唑微球销售峰值有望于2029年达8.5亿元。我国精神分裂症患者超过860万人,其中仅有8%的精神障碍患者会寻求治疗,用药率约80%,那么治疗患者约55万人。丽珠的阿立哌唑微球(1M)适应症为精神分裂,完成I期多次给药临床试验出组,及所有受试者随访,并完成临床数据分析。基于1)阿立哌唑是唯一的多巴胺D2受体的部分激动剂,机理独特、副作用小。2)丽珠精神疾病领域已有渠道基础(氟伏沙明、哌罗匹隆等)。3)海内海外的同类产品放量皆较快,海外阿立哌唑长效注射剂近2017-2022年CAGR为18.5%;国内棕榈酸帕利哌酮注射液5年CAGR为41.9%。4)竞争格局较好,国内获批的抗精神病药长效制剂仅有3个品种,阿立哌唑注射剂(大冢制药于2023年上市),利培酮微球(杨森制药、绿叶制药),和帕利哌酮注射剂(杨森制药、齐鲁制药);而涉足阿立哌唑长效制剂的药企也仅有3家(丽珠集团、科伦制药、辰欣药业)。我们预计,假设阿立哌唑微球将于2025年上市,并于2029年达到销售峰值8.5亿元,对应用药人数4.4万人,考虑依从性问题假设年均治疗次数为10支,用药量44万支,丽珠作为国产独家长效阿立哌唑针剂渗透率达80%。我们预计2025-2027年销售分别为32、500、598百万元。
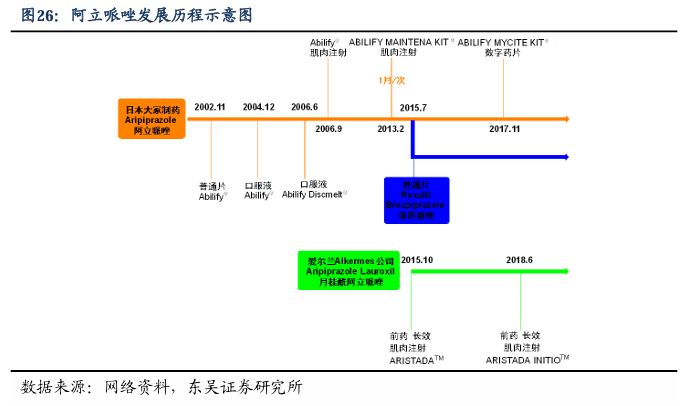
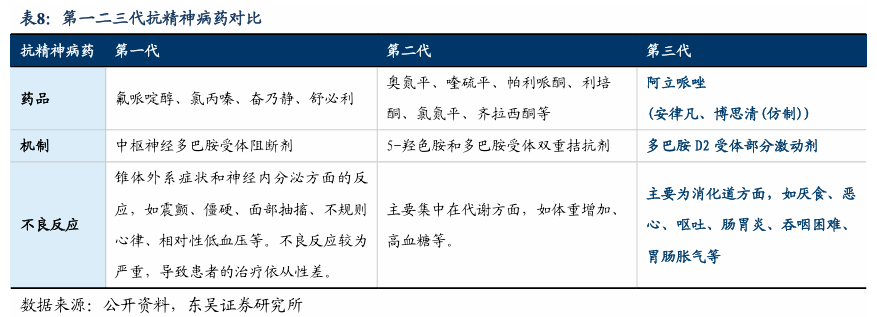
我国精神分裂症患者超过860万人。精神分裂症是一组慢性且经常使人衰弱的、严重的精神疾病,会影响到患者的思考、感受和行为方式,出现阳性症状(幻觉和妄想)、阴性症状(难以享受生活和远离他人)、情感症状、认知缺陷以及冲动攻击行为。根据中国精神卫生调查横跨157个疾病监测点的数据,我国精神分裂症及其他精神病性障碍的加权终生患病率为7.46‰,30天患病率为6.13‰;根据人口推算,我国精神分裂症患者超过860万人。然而由于相关医疗及咨询服务的资源缺乏、社会经济局限性及认知普及度等问题,仅有8%的精神障碍患者曾经寻求专业帮助。 长效剂型疗效突出,顺应性强,临床市场需求明确。精神分裂症病期多漫长,一般不能治愈,需终身治疗;大量患者存在服药不依从或部分依从的现象。尽管抗精神病药用药率高达约80%,规律服药率只有约40%。而从疾病早期开始定期进行药物治疗,可能是保持神经认知能力、防止大脑结构变化和阻碍慢性功能恶化进展的关键因素。因此,将抗精神疾病的药物开发成长效制剂,能有效规避患者漏服、藏药和拒绝服药问题,拥有巨大的临床价值和社会益处。阿立哌唑由百时美施贵宝和日本大冢制药联合研发,其原研药于2002年获得美国FDA批准上市,2004年获批进入中国(安律凡®阿立哌唑片剂),并属于2020年《医保》甲类、2018年《基药》品种。日本大冢制药又陆续研发出阿立哌唑口服液、口腔崩解片、普通肌内注射剂等剂型,但一方面,它们仍需要频繁给药,易引起患者情绪狂躁和攻击性行为,患者依从性仍是问题;另一方面,普通常释制剂还存在血药浓度起伏大、有峰谷现象等问题。因此,长效注射剂的开发,成为了必然的选择。一项美国临床精神药理学会年会(ASCP)的报告表明,口服抗精神病药的患者的总入院率为27.1%;相比之下,患者接受阿立哌唑1月长效注射剂治疗后,入院率骤降至2.7%,可见阿立哌唑长效制剂的优异临床效果。
阿立哌唑机理独特,副作用小。根据《精神分裂症防治指南(第二版)》,精神分裂症的主要一线前五大用药为奥氮平、喹硫平、利培酮、阿立哌唑、帕利哌酮等。由于阿立哌唑独特的药物机理,与其他二代抗精神病药并不构成完全竞争。美国《专家用药指南》推荐阿立哌唑为,与利培酮相并列的、治疗首发或复发性精神分裂症的首选药物。1)安全性方面,阿立哌唑和利培酮明显优于奥氮平和氟哌啶醇。在治疗谵妄的临床研究显示,利培酮治疗组的不良反应为4.8%,阿立哌唑9.5%,氟哌啶醇19%,奥氮平42.9%。其中,氟哌啶醇与利培酮易引起锥体外系副反应,发生率分别为19%、4.8%,长期服药应注意发生迟发性运动障碍;奥氮平则会引起过度镇静(28.6%),因此白天可以避免大剂量服用奥氮平和喹硫平等药物,以减轻白天的过度镇静。2)阿立哌唑对体重和糖脂代谢的影响不明显。发表在《中国药房》的研究显示,体重增加副作用方面,阿立哌唑显著优于利培酮,两者又优于奥氨平和氯氮平;而体重增加是精神分裂症康复期的常见副作用,逐渐受到临床关注。同时,阿立哌唑对空腹血糖的增加及2型糖尿病和脂代谢异常的发病风险也低于利培酮和奥氮平。3)疗效相当。疗效方面,主流的二三代非典型抗精神病药具有统计学上同等的疗效:累积反应率(PANSS总分下降30%)方面,阿立哌唑、奥氨平和利培酮之间没有差异(分别为70.1%、73.5%和74.8%;p=0.707)。4)机理独特,阿立哌唑是目前唯一用于临床的多巴胺D2受体的部分激动剂,其他二代抗精神病药并不构成完全竞争。它作为首个多巴胺系统稳定剂,具有独特的D2和5-羟色胺1A受体部分激动作用以及5-羟色胺2A受体拮抗作用,对于精神分裂症特定亚型获基因型或有突出疗效。5)潜在空间广阔,阿立哌唑对认知障碍、情感障碍、抑郁、焦虑等症状亦有改善作用;除治疗精神分裂症的症状外,在临床上还能用于双相障碍、重度抑郁症、自闭症和儿童孤独症,治疗场景丰富。总体来说,阿立哌唑作为非典型抗精神病药物,副作用小、服用简单、服药依从性较强,使得病情治疗更加稳定。
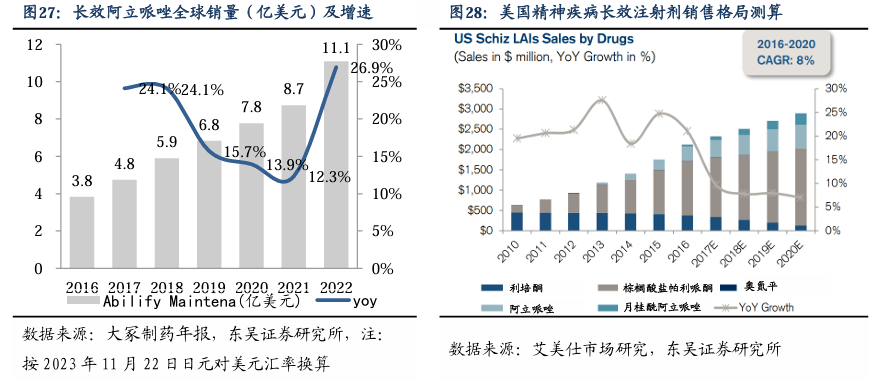
全球市场,2022年长效阿立哌唑销量11.1亿美元,5年CAGR为18.5%,在精神疾病长效注射剂的市占率约15%。阿立哌唑口服剂基于其疗效、安全性、副作用更易接受的优势,并且伴随长效剂型的获批上市,成为了最畅销的精神疾病用药,全球峰值销售额超过80亿美元,多年位居全球药品销售额前十之列,累计销售额超过635亿美元。阿立哌唑1月长效注射剂(Abilify Maintena)是由大冢和灵北制药合作开发,2013年被FDA批准上市。根据大冢制药年报,该品2022年销售收入11.1亿美元,2017-2022年CAGR为18.5%,增速较快,在全球精神疾病的长效注射剂领域中的市占率约15%。
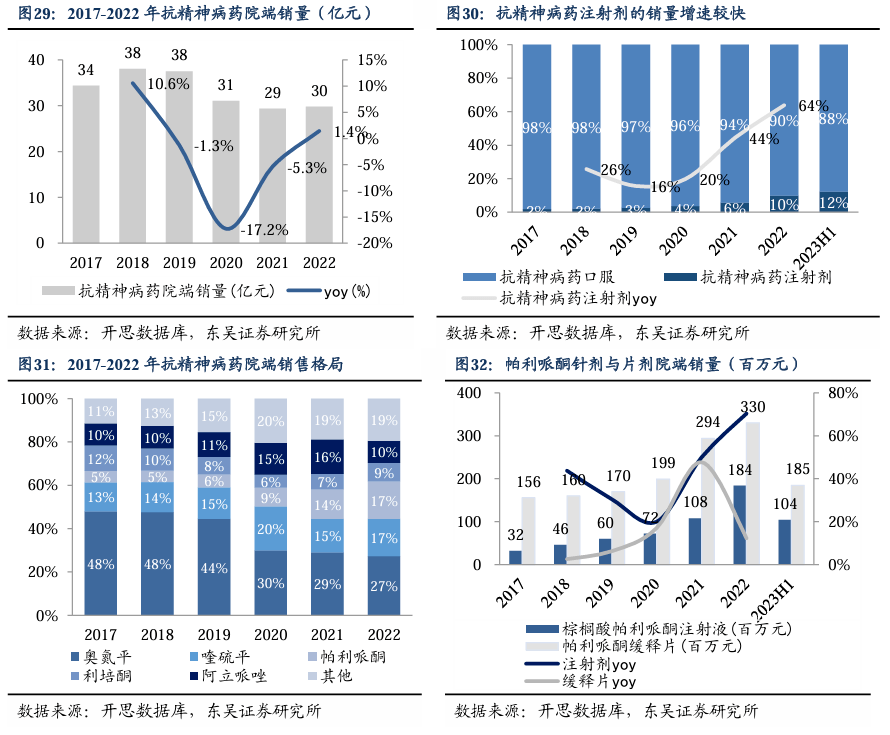
国内市场,阿立哌唑口服剂型已经竞争较强;长效制剂才是未来市场,5年CAGR为33%。截至2023H1,阿立哌唑国内已获批的剂型包括片剂、口崩片、口服液、胶囊剂、口溶膜、及进口注射剂。除了原研药企大冢制药外,国内共有近20家企业布局阿立哌唑,包括康弘药业、上药集团、恩华药业、齐鲁制药等。出于各种实际原因,口服抗精神病药通常作为一线处方,但长效注射抗精神病药才是解决依从性以及有效治疗和预防复发的方法。根据开思数据库,抗精神病药整体市场规模较为稳定,去除疫情影响,近五年国内市场规模年均约35亿元。近年来随着国内长效剂型的研发上市,注射剂型快速抢占口服剂型市场。根据开思数据库,2022年注射剂型的样本医院销售额约3亿元,占抗精神病药整体市场的10%,5年CAGR为32.7%。对比同细分领域药品的杨森制药的棕榈酸帕利哌酮注射液,与丽珠在研的阿立哌唑微球同为1M长效注射剂,其样本医院销量从2018年的0.46亿元增至2022年额1.84亿元,5年CAGR为41.9%,长效制剂的增速高于其片剂,佐证长效制剂将逐步替代口服剂型。
格局方面,抗精神病药长效注射剂竞争较少,国产长效阿立哌唑涉足药企仅3家。目前临床可用的长效针剂不多,主要系药物分子结构对剂型的限制,长效针剂研制技术的复杂程度和专利保护的限制,以及精神疾病机理尚不明确、新药开发较困难的原因。经查CDE网站,国内获批的抗精神病药长效制剂仅有3个品种,阿立哌唑注射剂(大冢制药于2023年上市)、利培酮微球(杨森制药、绿叶制药)、和帕利哌酮注射剂(杨森制药、齐鲁制药),竞争较好。国内参与开发阿立哌唑长效制剂的药企也尚不多,仅有2家国内企业:科伦药业于2017年首个获得长效制剂的临床批件后,仍在临床推进中;辰欣药业正在进行人体药代动力学比较临床试验。丽珠集团的阿立哌唑微球是按照2.2类新药注册申报,目前已经完成I期多次给药临床试验,并于23年10月获得报产受理。我们预计,丽珠的阿立哌唑微球将于2025年上市,较早进入国内抗精神病长效市场 + 制剂壁垒,有望在未来的十年里持续畅销,于2029年达到销售峰值8.5亿元。
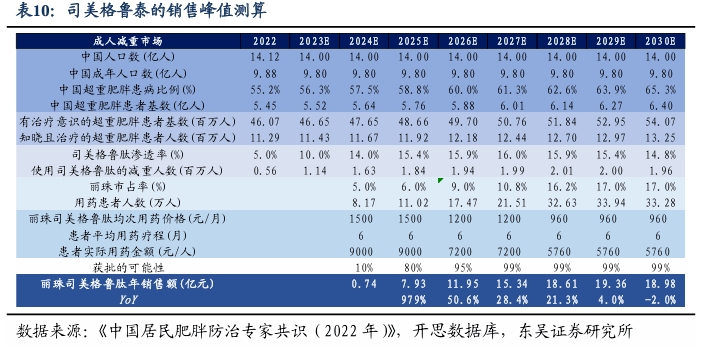
4. 生物药:聚焦辅助生殖主业+自身免疫创新领域 生物药品方面,截至2023Q4,有4项重点在研项目,包括1项正在进行BLA上市申报(PD-1),3项 III期临床(司美格鲁肽、IL-17A/F和重组人促卵泡素)。新冠疫苗、新冠二价苗和托珠单抗注射液的上市,使丽珠集团在生物药领域实现了跨越式的突破 除推进临床期的项目之外,丽珠生物还在双特异性抗体、NKT细胞治疗等领域进行研发探索。随着丽珠生物的产品陆续获批上市,丽珠生物充实了药物警戒、生产质量、产销衔接等相关团队,GMP体系以及产业化能力逐步提升,完善了整体运营能力。 4.1. 司美格鲁肽:国产临床进展领先,减重+降糖双市场空间超千亿 价值评估:司美格鲁肽除去减重降糖效果优异,拥有可降低重大不良心血管事件风险且伴随较少低血糖风险的优势。其潜在市场空间巨大,基于中国超重肥胖人数近8亿人,以及糖尿病患者约1.7亿人,市场空间有望达到500亿元;且市场培育良好,诺和诺德的GLP-1市占率达65%,司美格鲁肽上市后有望与其他多款GLP-1单、双靶点药物共享辽阔市场空间。格局方面,司美格鲁肽专利2026年到期,目前有7家公司的产品在临床3期,生物类似物或改良新药竞争力较强的企业有:丽珠、齐鲁、石药、华东。丽珠的临床进展为国内领先之一,2023年5月,糖尿病适应症完成III期临床试验入组,预计2024Q2报产,2025年获批,其减重适应症也将于2023年底申请IND;此外,丽珠具有原药及制剂生产优势,其司美格鲁肽注射液的原料药为自主生产,并享有长期积累的发酵原料药技术优势,包括前期研发生产过阿卡波糖、利拉鲁肽等复杂原料,因此在司美格鲁肽的原药及制剂方面均已具备稳定的生产工艺水平及能力。我们预计,丽珠司美格鲁肽仿制药有望在2029年成为20亿元大品种。
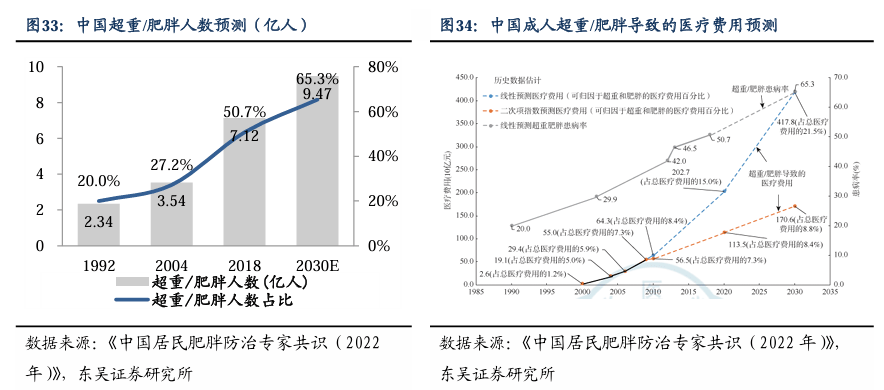
适应症一:除去审美更是疾病,国内超重肥胖成人患者占比超50%,预测2030年相关医疗费用超4100亿元。近年来,心血管疾病、糖尿病、部分癌症等慢性非传染性疾病(“慢性病”)导致的死亡人数占中国居民总死亡人数的近90%,而超重和肥胖是慢性病的主要危险因素。根据《中国居民肥胖防治专家共识(2022年)》指出的研究,我国成年居民肥胖(BMI≥28kg/㎡)和超重(BMI≥24kg/㎡)合并人数比例已超过50%。预计至2030年,我国成人、学龄儿童青少年和学龄前儿童的超重肥胖率可能分别达到65.3%、31.8%和15.6%,而超重肥胖的人数可能分别达到79.0千万、5.9千万和1.8千万。超重及肥胖已经成为中国乃至全球性的重大公共卫生问题,由超重肥胖导致的医疗费用或将达到4178亿元,占总医疗费用的21.5%。未来,随着肥胖人群的增加、居民体重管理和健康意识的增强,减肥需求市场将持续增加。
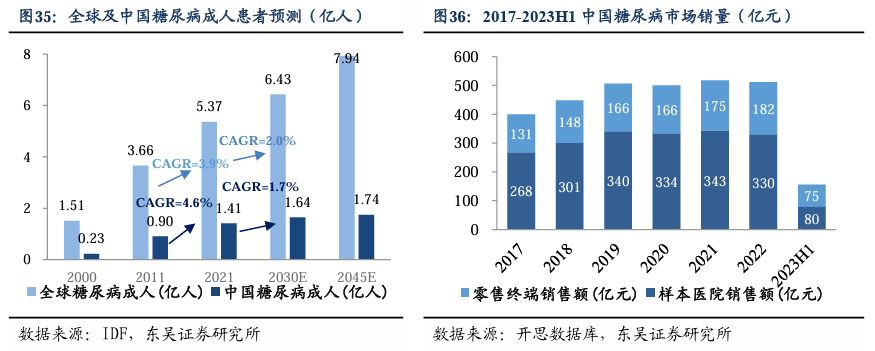
适应症二:糖尿病药物销量超500亿元,预测2030年国内患者超1.7亿人。糖尿病是以高血糖为特征的一类代谢性疾病,其中1型缺乏胰岛素分泌能力,在糖尿病中约占比 5%;2型主要是由于肥胖和缺乏锻炼,使身体无法有效地利用胰岛素,2型糖尿病(T2DM)往往在发病几年后才被诊断出来,且已出现并发症。我国糖尿病以2型为主,占总体糖尿病人群的90%以上;该病无法治愈,大多需要持续关注血糖水平并终身服药。国际糖尿病联合会(IDF)发布的《世界糖尿病地图(第10版)》显示,中国是世界糖尿病第一大国,全世界每4名糖尿病患者中就有1名来自中国。2011-2021年,我国糖尿病患者人数由9000万增加至1.4亿,CAGR达4.6%;预计到2030年中国的糖尿病患者(20-79岁)将达到1.7亿人。
GLP-1RA用药优势:兼顾心血管等疾病且无低血糖风险,新入选指南推荐的T2DM合并症一线用药。肾、心疾病为T2DM致死和致残的主要原因,也是GLP-1RA作为糖尿病用药的主要优势。1)中国成人T2DM患者合并心血管疾病的患病率为33.9%。基于已经有三种GLP-1RA被证明可显著降低重大不良心血管事件风险,美国糖尿病学会最新版指南《ADA糖尿病医学诊疗标准(2022版)》,首次将GLP-1RA推荐为T2DM合并心血管疾病患者的起始治疗,对于二甲双胍用药可以选择是否联用。2)国内27.1%的T2DM患者合并慢性肾脏疾病,而三种GLP-1RA均显示了良好的肾脏保护作用。对于T2DM合并慢性肾脏疾病高风险/已确诊的患者,优先推荐SGLT2抑制剂以延缓肾病进展;若存在SGLT2抑制剂使用禁忌或不能耐受时,推荐给予有心血管获益的GLP‑1R激动剂。3)对于超重肥胖人群的糖尿病前期控制手段,GLP-1RA也是推荐用药。4)低血糖症(血糖BG |
【本文地址】
今日新闻 |
推荐新闻 |