【临床注册】医疗器械临床试验 |
您所在的位置:网站首页 › 地板砖什么尺寸好看 › 【临床注册】医疗器械临床试验 |
【临床注册】医疗器械临床试验
|
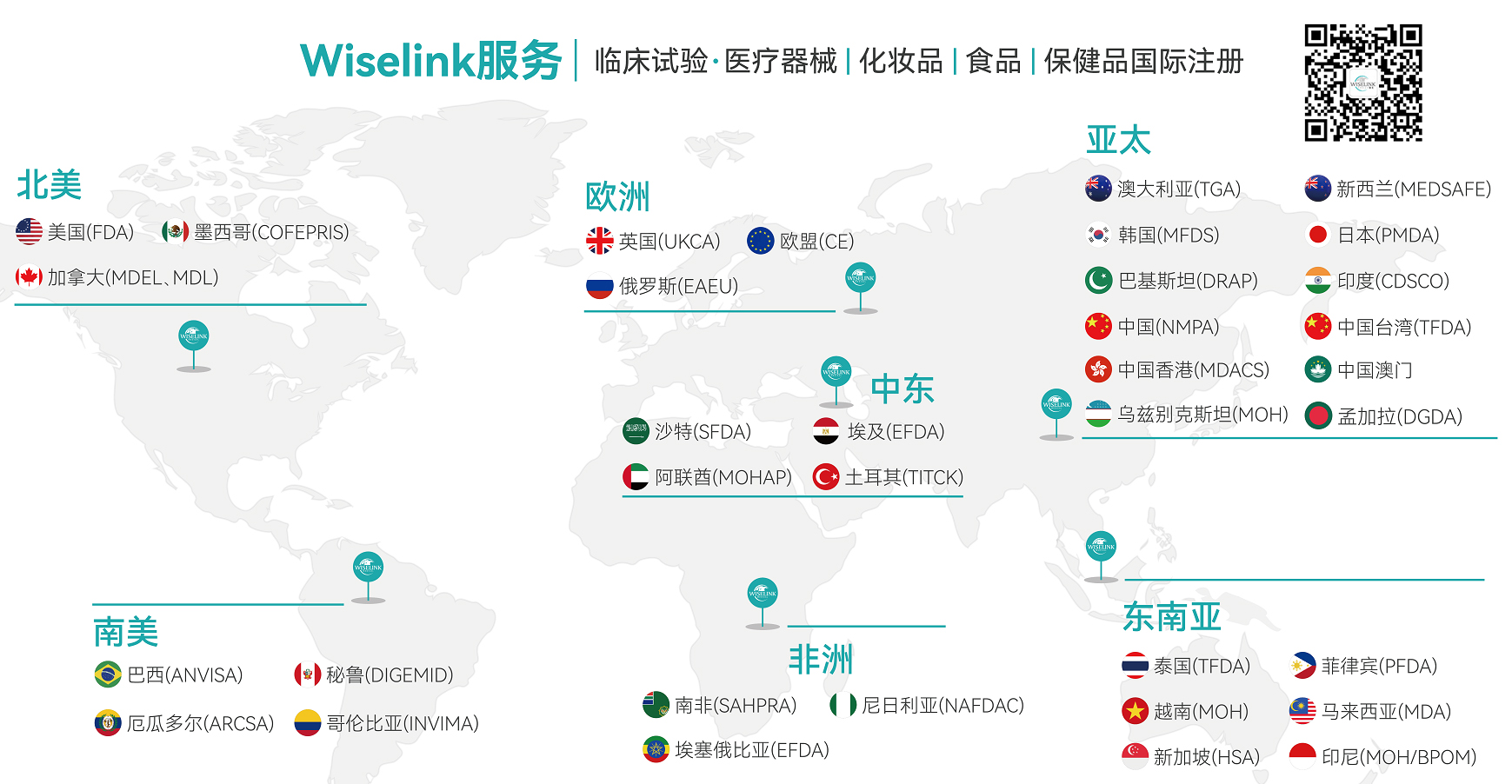
一、定义及临床试验目的 临床试验的定义:任何涉及⼀个或多个⼈类受试者的系统调查,以评估设备的安全性或性能。 • 医疗器械临床调查通常出于监管要求进⾏ • 进⾏临床调查的目的应在规划过程开始时商定,因为它将对研究的设计和需要⽣成的临床数据产⽣直接影响。 二、临床试验和医疗产品生命周期的关系 • 设计 - 验证 - 确认 - ⽣产 - 销售 - 售后 • 根据质量管理体系 ISO13485 • 设计验证应针对代表性产品进⾏ • 代表性产品包括初始⽣产单元、批次或同等产品 • 作为设计和开发验证的⼀部分,组织应根据适⽤的法规要求对医疗器械进⾏临床评估或性能评估 • ⽤于临床评估或性能评估的医疗器械不被视为发布给客户使⽤ 临床试验可分三个阶段:策划 — 执行 — 结束 三、临床试验策划 1、策划考虑因素 • 医疗器械法规 • 体外诊断医疗器械法规 (EU) 2017/746 (EU IVDR) • 医疗器械法规 (EU) 2017/745 (EU MDR) 2、质量管理体系要求 • 法规要求(国际 - MDSAP、区域 - MDR、国家 - 美国 FDA、加拿⼤- HC 等) 3、指导⽂件 • ISO 14155-2020 ⼈类受试者医疗器械的临床研究—良好的临床试验规范 • MEDDEV 2.7/4 关于临床研究的必要性和⼀般原则 • MEDDEV 2.7/2 Rev 2 关于临床调查验证和主管当局评估 • MDCG 2021-20 为 MDR 临床研究⽣成 CIV-ID 的说明 • MDCG 2021-08 临床研究申请/通知⽂件 • ISO 20916:2019 - 体外诊断医疗器械 - 使用⼈体样本的临床性能研究 - 良好的研究实践 • MDCG 2021-2 - COVID-19 快速抗体检测最新技术指南 4、人员配备 5、编写临床调查档案 6、选址 7、建立试验终止程序 四、临床试验执行 1、临床试验作业程序标准 2、相关部门审批 3、监测 Wiselink-全球布局
知汇供应链服务(深圳)有限公司 WiselinkSupply Chain Services (Shenzhen) Ltd,简称Wiselink CN隶属于澳大利亚Wiselink集团,是深圳大兴集团的官方合作企业,拥有包括原澳大利亚药品监督管理局局长Dr.Derrick Beech为首席顾问的国际专业团队,秉承源于澳洲、扎根中国、服务世界的精神,信守专业、客观、真诚的核心价值观,致力于为体外诊断(IVD)、医疗器械(MD)、保健品和化妆品制造商提供海外临床试验和全球合规认证服务。 集团总部 Wiselink Group Level 25 100 Mount Street, North Sydney, NSW Australia2060 欧洲分公司 Wiselink Medical (lreland) Limited Unit 1/4/7Block 1 Northwood Court, Northwood Crescent,Dublin 9. D09 E438, lreland 美国分公司 Wiselink Medical Inc 666 Old Country Rd, Suite 201, Garden City, NY 11530 泰国分公司 Wiselink Medical (Thailand) Company Limited No. 1 Vasu Building 1, Room No. P01, 1st Floor, Soi Sukhumvit 25, Sukhumvit Road, Klongtoey Nuea Subdistrict, Wattana District Bangkok 10110, Thailand 日本分公司 株式会社Wiselink Japan 地址:東京都千代田区神田須田町一丁目2番地7淡路町駅前ビル3階 新加坡分公司 Wiselink Medical (Singapore) Pte.Ltd. (SG) 08-07,175A, Bulington Square,Bencoolen Street 189650 Singapore 中国分公司 知汇供应链服务(深圳)有限公司 地址:深圳市宝安区新安街道稻兴环球科创中心A座1812室 官网:Http://www.wiselinkchina.com |
【本文地址】