讲座 |
您所在的位置:网站首页 › 医院手术pacu什么 › 讲座 |
讲座
|
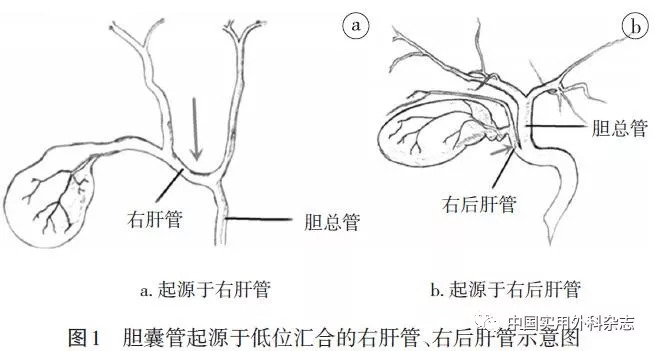
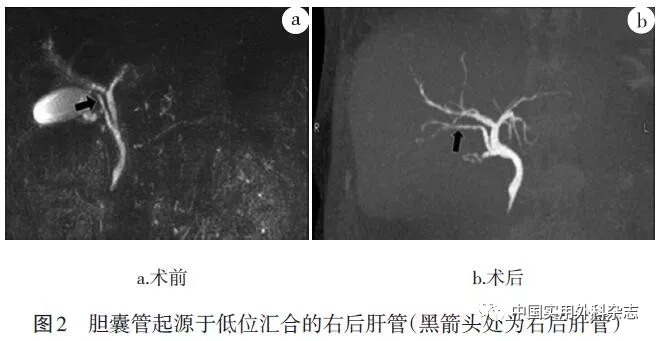
异位胆囊和重复胆囊常伴有胆囊管、胆囊动脉的变异,须仔细辨认两者的解剖关系后结扎、切断。肝内异位胆囊难以剥离者,可行部分胆囊切除。面对重复胆囊的病例,王捷等[4]建议对于非结石病人可切除病变胆囊、保留正常胆囊;对于结石病人则建议切除胆囊,以免残余胆囊结石复发。 1.1.1.2 胆囊管变异 其变异包括胆囊管的长度、数量、缺如、起源异常和汇入肝总管的形式异常等[5-6],后两种变异在临床中较为常见。以下为几种常见的胆囊管的起源变异[6-8]:胆囊管起源于左右肝管汇合部;胆囊管起源于胆总管囊肿;胆囊管起源于左、右肝管;胆囊管起源于右后肝管。当胆囊管起源于左右肝管汇合部时,极易同时损伤左右肝管,导致中转行开放胆肠吻合术。当胆囊管起源于低位汇合的右肝管、右后肝管(图1)时,术者很可能误将后两者作为胆囊管而切断。图2为笔者亲历的胆囊管起源于右后肝管病例。
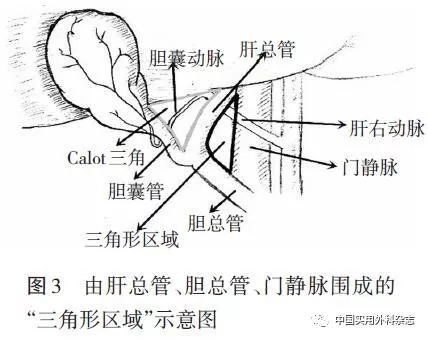
胆囊管汇入肝总管的形式也有诸多变异。Moosman等解剖了250具尸体,其中胆囊管从肝总管右侧壁汇入占79.6%,从肝总管左侧壁、前壁或后壁汇入占20.4%。屈士斌等[9]的研究中,63.3%的胆囊管和肝总管相遇后即成角汇合成胆总管,36.7%的胆囊管在纤维结缔组织中与肝总管伴行一段距离后再汇合形成胆总管。胆囊管在十二指肠前方走行,于十二指肠上部汇入肝总管则较为罕见。其中胆囊管与肝总管并行低位汇合最常发生IBDI,术中须细心寻找胆囊管的起源,以免误伤胆总管或残留胆囊管过长而形成残留结石[10]。 1.1.1.3 肝管变异 肝管的起源、数量、长度、直径及肝区引流路径均具有显著的个体差异,但85%的肝管变异发生在直径约3.0 cm的“Moosman区”即Calot三角内。异常肝管的开口越低、越接近胆囊管开口其损伤发生率就越高[4]。 黄志强强调,经典的左、右肝管汇合类型只约占半数,剩下半数右肝管呈分裂型,除非术前影像学检查证实有明确的左右肝管分支,否则头脑中一定视肝门部有三支肝管的结构[11]。常规地显露胆总管、肝总管均难以避免低位汇合的右后肝管损伤,且右后肝管损伤后症状又极具隐蔽性和欺骗性(如仅表现为迁延不愈的胆漏,内镜下逆行胰胆管造影检查有可能找不到漏点),术者容易误认为是迷走胆管的问题,造成经久不愈的胆漏和肝脏右后叶的萎缩。这类病人即使中转开放手术或再次手术都容易遗漏或修补失败。 此外,仍有5.5%的胆漏源自于Luschka胆管的损伤[12],导致术后可出现胆囊床胆漏、胆汁性腹膜炎、膈下或肝下脓肿等并发症[13]。由于Luschka胆管直径较小以及胆囊周围炎症的存在,术中不易被发现。精细解剖胆囊窝是避免Luschka胆管胆漏的惟一途径,术者须警惕胆囊窝的管状或条索状结构是Luschka胆管的可能。 1.1.1.4 胆囊动脉变异 胆囊动脉变异比胆道变异更加常见,主要体现在胆囊动脉的起源、走行、数量等方面。正常的胆囊动脉起源于肝右动脉,全程或部分走行于Calot三角内,术中易于显露。约20%的胆囊动脉起源于迷走肝右动脉、肝中动脉、肝左动脉、胰十二指肠动脉、肠系膜上动脉等,多走行于Calot三角外,术中探查时易损伤[14]。当胆囊动脉位于胆囊管或胆总管前方时,须先行离断动脉后方能清晰显露后面的胆道,钳夹动脉时易误伤后面的胆道[15]。此外,两支胆囊动脉的情况并不少见,3支及以上罕见,如术者满足于处理好一支胆囊动脉而忽略并切断其他分支,很容易导致出血[16]。 除上述解剖变异外,还有部分肝右动脉变异的存在。在IBDI的病例中,少数肝右动脉起源于肠系膜上动脉,经门静脉后方,伴胆总管右侧上行穿过Calot三角入肝[14],该动脉的损伤会给后续的修复和治疗带来更大的困难和障碍,病人最终不得不选择原位肝移植(orthotopic liver transplantation,OLT)[17]。 1.1.2 病理学因素 LC危险的病理学因素主要包括3方面:(1)急性炎症。急性胆囊炎(acute cholecystitis,AC) 的病人,其胆囊和Calot三角区炎性渗出、充血、水肿,三管(胆囊管、肝总管、胆总管)的解剖层次不清,手术极易造成IBDI。Törnqvist等[18]的研究显示,对AC病人行LC,其发生IBDI的风险是非AC病人的2倍。该研究根据2013版东京指南(Tokyo Guidelines 2013,TG13)对AC进行分级后显示:Ⅰ级AC行胆囊切除术不增加IBDI的风险,Ⅱ级AC的IBDI风险增加1倍以上,Ⅲ级AC的IBDI风险增加近8倍。为了避免IBDI的发生,2018版东京指南(Tokyo Guidelines 2018 ,TG18)[19-21]根据东京分级(Tokyo grade)、查尔森合并症指数(Charlson comorbidity index,CCI)、美国麻醉医师协会身体情况评分(American Society of Anesthesiologists physical status classification,ASA-PS)对AC的病人进行系统评估后选择合理的治疗方案。推荐适宜手术的病人在局部炎症进展和纤维化形成之前由经验丰富的外科医生尽早行LC,而不适合手术的病人在给予药物治疗和胆囊引流后,择期行LC。(2)合并肝硬化、门静脉高压症。此类病人门静脉系统长期淤血扩张,胆囊周围静脉增多、压力增高,伴有很多侧支循环的开放。同时肝硬化导致肝脏萎缩变小,肝门移位,胆囊位置改变,造成操作难度增加,易误伤曲张的静脉导致出血,如胆囊壁与肝床间粗短静脉的破裂出血、Calot三角和肝十二指肠韧带曲张静脉出血等。又由于肝硬化病人多存在凝血功能障碍,出血后很难停止和控制,这大大增加了术中IBDI的发生率。对于此类病人,须选择合理的 trocar位置,获得清晰的视野,减少不必要的操作,避免损伤肝门周围曲张静脉,剥离胆囊时须遵循“宁伤胆,勿伤肝”的原则[22]。(3)胆囊肿瘤。对于胆囊癌病人,为达到肿瘤R0切除,有时须切除部分肝外或肝内胆管,也可能增加IBDI的发生率。 综合上述因素,笔者认为,IBDI最易发生于AC导致Calot三角显示不清和胆囊管消失的情况。当Calot三角显示不清、胆囊管过短、Hartmann袋的过度牵拉时,导致局部形成一个由肝总管、胆总管、门静脉围成的“三角形区域”(图3),该区域内常有肝右动脉走行[14]。术者若按常规采用顺行胆囊切除法时则容易将该三角形区域误认为是Calot三角进行游离解剖,极易造成IBDI联合血管损伤。当Calot三角结构显示不清时,笔者建议采用逆行胆囊切除法,紧贴胆囊壁游离,不能轻易切断任何一个管道结构,必要时采用顺逆结合法显露胆囊,以避免发生IBDI。张长和等[23]采用“经胆囊颈横断腹腔镜胆囊次全切除法”处理胆囊颈部出现“冰冻样”Calot三角等复杂情况,并取得良好的效果。
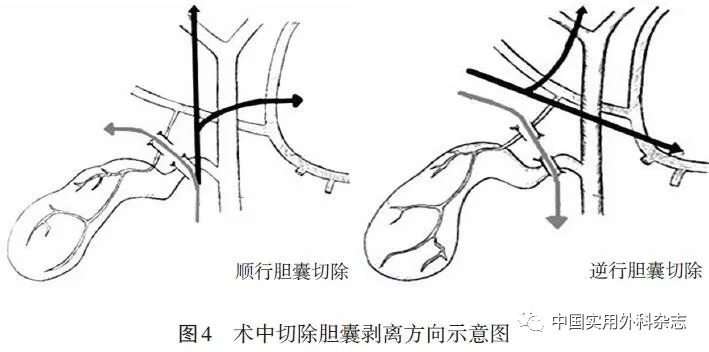
Mirizzi综合征常导致胆囊管消失,原则上要求开放手术。腹腔镜手术治疗Mirizzi综合征IBDI发生率为0~22%,因此,对Mirizzi综合征病人进行腹腔镜手术时需要有选择性[24]。对于大部分Ⅰ型Mirizzi综合征病例,有经验的外科团队可在腹腔镜下完成胆囊切除术或保留部分胆囊壶腹和胆囊管的次全胆囊切除术,而Ⅱ型及以上的Mirizzi综合征病例宜行开放手术。Mirizzi综合征可合并胆管炎,这类病人术前应尽早行胆道引流,待炎症和黄疸减轻后择期手术。Mirizzi综合征时,三管合流处有明显的炎症改变,顺行切除胆囊较为困难,且容易留下胆管缺损或加重IBDI。这种情况下应先从胆囊底部开始,逐渐向胆囊壶腹部游离。如果壶腹部易游离且可完全切除,行胆囊切除术。否则,采取胆囊内操作,取净胆囊内结石,行保留部分胆囊壶腹和胆囊管的次全胆囊切除术,避免IBDI。术中除了细致操作外,术者还应想到胆囊-胆管内瘘的存在,胆囊切除后宜选择合适的方式修补胆管缺损,并留置T管,避免术后胆管狭窄。 1.2 术者因素 由于LC学习曲线的客观存在[25],初学者在训练过程中都易发生IBDI。年轻的外科医生往往缺乏传统外科的手术经验,在遭遇IBDI时,对开放手术缺乏信心,不能及时中转,亦加重了IBDI的进展[26],这需要对初学者进行严格培训和监督。另外,外科医生对LC和IBDI的主观认识态度也至关重要。手术无大小、轻重之分,LC绝不能图一时之快,遭遇IBDI时应冷静面对、及时求助,避免情况恶化。 2 IBDI预防策略 2.1 详细的术前评估 超声能够准确判定胆囊病变的性质,了解病变的大小、数量和部位,可作为LC术前的常规检查。CT、磁共振胰胆管造影可以准确评估胆囊炎症的程度、周围炎症波及的范围及胆管的情况,从而判断LC的难易程度。此外,磁共振胰胆管造影还能够多角度准确评估肝内外胆管树的解剖关系,准确判断胆道是否存在变异、梗阻或狭窄,有助于减少IBDI的发生。对于AC病人,可参考TG18系统评估病人状态,从而合理地选择治疗方案;对于合并肝硬化的病人,须参考Child-Pugh分级积极调整肝功能到最好状态;对于怀疑胆囊肿瘤的病人,可利用超声造影、增强CT进行鉴别诊断和术前评估。术中荧光胆管造影和术中超声可能会减少IBDI,而目前尚无充分证据显示术中胆管造影的价值[21]。 2.2 精准的解剖辨认 肝Ⅳ段的下缘和Rouvière沟上缘应作为解剖标志[27],LC的任何操作应在这两个解剖区域内进行。Rouvière沟正对胆囊管和胆囊颈移行部,以此为定位点确定胆囊管的位置,可以指导术者维持正确的解剖平面。在基于Rouvière沟的定位技术之上游离Calot三角时,采用关键性安全视角(critical view of safety,CVS)原则[28]。Calot三角解剖完成时,安全视野内清晰看到有且仅有两个结构(胆囊管、胆囊动脉)进入胆囊,从而预防了IBDI的发生。 2.3 准确评估术中的危险程度 术中须明确何时应终止手术。LC方向感至关重要,顺行切除胆囊时,沿胆囊管向上剥离胆囊要尽早左转;逆行切除胆囊时,从胆囊底剥离胆囊近壶腹要及时右转,避免直行和左转,如果遇到障碍,及时终止和仔细辨识(图4)。AC导致胆囊壁渗出水肿,术者在分离胆囊床时可利用水肿的胆囊壁,结合电刀的锐性分离和吸引器的钝性分离,将胆囊壁的外层留在胆囊床上,从而安全地处理胆囊管和胆囊动脉。在分离过程中,一处分离层面不清晰时,须更换别处分离,有意识的靠近胆囊侧进行分离,避免切入肝脏内。当遇到解剖变异、Mirizzi综合征、AC等复杂情况以至于分离困难,达不到严格的安全视野时,可选择性应用术中胆道造影。亦参考TG18中的术中难度评分[21],及时改变手术策略,行次全、部分胆囊切除或开放胆囊切除术可能更佳。
2.4 精确控制术中的出血 术中出血容易导致IBDI的发生,因此预防出血比止血更为重要:术中在Calot三角内未发现胆囊动脉或发现异常粗大的胆囊动脉时须警惕是胆囊动脉或肝动脉变异的可能;术中轻柔地牵拉胆囊壁,以避免撕裂细小的胆囊动脉分支和较短的胆囊动脉及邻近的肝右动脉;尽量靠近胆囊壁结扎动脉,这样可获得较长的血管残端便于控制出血[16]。面对出血时,首先应压迫止血,然后镇静、思考是静脉出血还是动脉出血,避免盲目地大块组织钳夹止血和过度地使用电凝止血。胆囊壁或胆囊床的动脉性出血应采用Hemlock夹结扎止血;静脉出血可采用压迫、电凝或缝合止血;持续性大出血,应立即转为开放手术。 最后,确保顺利、安全地完成手术。面对困难LC要及时中转开放手术,若开放手术亦难以处理,可行胆囊造口引流暂时缓解,择期再行胆囊切除术。 3 IBDI的处理 发生IBDI时要冷静面对,及时终止错误操作,减少和终止出血,避免情况恶化;而对于术中不易察觉的IBDI,术者应在手术结束之前仔细冲洗,检查有无胆汁漏出,仔细检查标本是否“双管齐下”,怀疑损伤或损伤位置不明确时,应联合术中胆管造影、胆道镜探查等措施确认胆道的完整性[29]。IBDI的早期诊断至关重要,其最佳的修复时机就是在损伤术中,因为此时胆管局部的炎性水肿较轻。应由有经验的胆道外科医生实施一期修复[30]。对于基层医院医生,遭遇IBDI时,首先应充分引流,并尽早转至上级专科医院实施确定性修复手术。 (参考文献略) (2018-08-03收稿 2018-08-25修回) 版权声明 本文为《中国实用外科杂志》原创文章。其他媒体、网站、公众号等如需转载本文,请联系本刊编辑部获得授权,并在文题下醒目位置注明“原文刊发于《中国实用外科杂志》,卷(期):起止页码”。谢谢合作! 点击 阅读原文 返回搜狐,查看更多 |
【本文地址】
今日新闻 |
推荐新闻 |