高中化学:物质的检验、分离和提纯 |
您所在的位置:网站首页 › 分离提纯的操作 › 高中化学:物质的检验、分离和提纯 |
高中化学:物质的检验、分离和提纯
|
(2)化学方法 方法 适用条件 加热法 混合物中有热稳定性差的物质时,可直接加热,使热稳定性差的物质分解,如纯碱中混有小苏打 沉淀法 在混合物中加入某种试剂,使其中一种以沉淀的形式分离出去 转化法 不能通过一次反应达到分离的目的时,要先转化为其他物质分离,然后将转化后的物质恢复为原物质 酸碱法 被提纯物质不与酸碱反应,而杂质可与酸碱发生反应,如用NaOH溶液除去铁粉中的铝粉 氧化还原法 ①对混合物中混有的还原性杂质,可加入适当的氧化剂将其氧化为被提纯物质②对混合物中混有的氧化性杂质,可加入适当的还原剂将其还原为被提纯物质 调节pH法 通过加入试剂来调节溶液的pH,使溶液中杂质成分转化为沉淀而分离 电解法 利用电解原理来分离、提纯物质,如电解精炼铜 吸收法 常用于气体的净化和干燥,可根据被提纯气体中所含杂质气体的性质,选择适当的固体或溶液作吸收剂。常用装置是洗气瓶或干燥管(U形管) 4.依据物质的物理性质选择恰当分离(提纯)方法 (1)“固+固”混合物的分离(提纯)
(2)“固+液”混合物的分离(提纯)
(3)“液+液”混合物的分离(提纯)
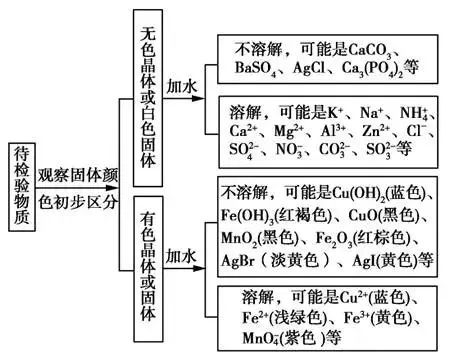
5.有机物分离提纯的常用方法 (1)分离和提纯有机物的一般原则 根据混合物中各成分的化学性质和物理性质的差异,通过化学或物理方法处理,以达到分离和提纯的目的。 (2)有机物分离和提纯的常用方法 常用方法 目的 主要仪器 实例 分液 分离、提纯互不相溶的液体混合物 分液漏斗 分离硝基苯与水 蒸馏 分离、提纯沸点相差较大的混合溶液 蒸馏烧瓶、冷凝管、接收器 分离乙醛与乙醇 洗气 分离、提纯气体混合物 洗气装置 除去甲烷中的乙烯 过滤 分离不溶性的固体和液体混合物 过滤器 分离硬脂酸与NaCl 渗析 除去胶体中的小分子、离子 半透膜、烧杯 除去淀粉中的NaCl、葡萄糖 ● 物质的检验与鉴别 ● 1.物质的检验 根据被检验物质的性质(主要是化学性质,也可以是特殊的物理性质)使被检验物质与加入的试剂产生作用,转变为某种已知物质,或产生某种特殊现象,从而确定被检验物质的成分。 2.物质检验的一般程序与思路 (1)固态物质的检验
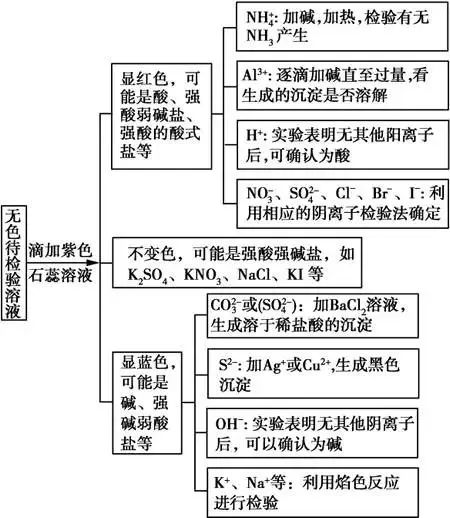
(2)无色溶液的检验
(3)气态物质的检验 由于气态物质贮存困难,使用时易扩散,故检验时要尽可能利用其物理性质;若利用化学性质,则尽可能多用试纸。一般按下列顺序进行检验:
3.鉴别的常用方法 鉴别方法 适用范围、原理 物理方法 观察法 观察被鉴别物质的状态、颜色等 嗅试法 判断气体或有挥发性物质的不同气味(有毒气体禁用) 水溶法 观察被鉴别物质在水中的溶解情况 加热法 主要用于易升华的物质 焰色反应法 常用于鉴别金属或金属离子 化学方法 加热法 常用于易分解的物质 显色法 主要用于某些在特定试剂中显示特殊颜色的离子 水溶法 常用于加水后有特殊现象的物质 点燃法 主要用于鉴别有助燃性或可燃性的物质 指定试剂法 主要根据待鉴别物质性质的差异来选择合适试剂 4.有机物鉴别与检验 有机物的种类繁多,含有不同的官能团,具有不同的化学性质,这决定了有机物鉴别的复杂性。对有机物的鉴别可以从以下几个方面进行总结。 (1)根据有机物的溶解性 通常是将有机物加入水中,观察其能否溶于水。用此方法可以鉴别乙酸和乙酸乙酯、乙醇和氯乙烷、甘油和油脂等。 (2)根据液态有机物的密度 观察不溶于水的有机物在水的上层还是下层,从而判断其密度比水的小还是大。用此方法可以鉴别硝基苯和苯、1-氯丁烷和四氯化碳等。 (3)根据有机物的燃烧情况 观察其是否可燃(大部分有机物都可燃,四氯化碳不可燃);燃烧时产生黑烟的多少(可区分乙烷、乙烯和乙炔,聚乙烯和聚苯乙烯等);燃烧时的气味(如识别聚氯乙烯、蛋白质等)。 (4)根据有机物官能团的性质 有机物分子中的官能团决定有机物的性质,有机物的性质反映了其分子中含有的官能团。检验有机物分子中官能团的常用试剂与方法如表所示: 物 质 试剂与方法 现象 不饱和烃 加入溴的四氯化碳溶液或酸性KMnO4溶液 溶液褪色 苯的同系物 加入酸性KMnO4溶液 溶液褪色 卤代烃 与NaOH水溶液混合加热,取水层,用稀硝酸酸化后,加入AgNO3溶液 有沉淀生成,根据沉淀的颜色,确定卤素的种类 醇 有气体放出;有果香味物质生成 醛基 2、加热煮沸 有银镜生成;有红色沉淀生成 羧酸 溶液显红色;有气体产生 酯 闻气味;与NaOH溶液混合、加热 果香味;油层消失 酚类 溶液显紫色;产生白色沉淀 淀粉 加入碘水 溶液显蓝色 蛋白质 加入浓硝酸微热(对于含苯基的蛋白质);灼烧 显黄色;有烧焦羽毛的气味 5.阳离子的检验 (1)阳离子检验思路 根据题目要求,若是检验阳离子则选择最为灵敏的试剂和方法,若是离子检验和推断相结合的题目,则可能会涉及多种检验方法。 (2)注意一些金属离子(Cu2+、Fe2+、Fe3+)在水溶液中的颜色。 (3)注意一些离子之间的相互干扰以及排除干扰因素的方法,如Fe2+的检验需首先加入KSCN溶液排除Fe3+的干扰等。 (4)常见阳离子的检验 离子 检验试剂 主要实验现象 Ba2+ 稀硫酸或可溶性硫酸盐溶液 先加稀盐酸,不产生沉淀,然后加稀硫酸或可溶性硫酸盐溶液生成白色沉淀 Mg2+ NaOH溶液 生成白色沉淀,NaOH过量时沉淀不溶解 Al3+ NaOH溶液或氨水 加氨水或适量NaOH溶液,有絮状白色沉淀生成,沉淀能溶于NaOH溶液,但不溶于氨水 Fe3+(黄色) NaOH溶液 生成红褐色沉淀 KSCN溶液 溶液呈红色 Fe2+(浅绿色) NaOH溶液 加NaOH溶液生成白色沉淀,在空气中迅速变为灰绿色,最后变为红褐色 KSCN溶液,新制氯水 加KSCN溶液,无明显现象,加新制氯水后溶液呈红色 H+ 紫色石蕊溶液 变红色 甲基橙溶液 变红色 pH试纸 变红色 锌粒 生成无色气体 Cu2+(蓝色) NaOH溶液 加NaOH溶液,有蓝色沉淀生成,若加热则沉淀变黑 H2S(或Na2S溶液) 生成黑色沉淀 Ag+ 稀盐酸或氯化物溶液,稀硝酸 生成白色沉淀,不溶于稀硝酸 NaOH溶液 加NaOH溶液,加热并用湿润的红色石蕊试纸检验产生的气体,试纸变蓝 Na+ 焰色反应 火焰呈黄色 K+ 火焰呈紫色(透过蓝色钴玻璃片) 6.常见阴离子的检验 离子 检验试剂或方法 实验现象 OH‒ ①取少量试液于试管中,向其中滴加紫色石蕊溶液(或酚酞试液);②用玻璃棒蘸取少量试液滴于红色石蕊试纸上 ①紫色石蕊溶液变蓝(或酚酞试液变红);②红色石蕊试纸变蓝 Cl‒ 取少量试液于试管中,向其中滴加少量AgNO3溶液,再加入稀硝酸 生成白色沉淀,且不溶于稀硝酸 Br‒ 取少量试液于试管中,向其中滴加少量AgNO3溶液,再加入稀硝酸 生成浅黄色沉淀,且不溶于稀硝酸 I‒ ①取少量试液于试管中,向其中滴加少量AgNO3溶液,再加入稀硝酸;②滴入淀粉溶液后再滴入氯水 ①生成黄色沉淀,且不溶于稀硝酸;②溶液显蓝色 氯化钡溶液、稀硝酸 生成白色沉淀,加稀硝酸后白色沉淀溶解,产生无色无味气体 氯化钡溶液、稀盐酸 不生成沉淀,加稀盐酸,产生无色无味气体 氯化钡溶液、盐酸、品红溶液 先生成白色沉淀,加盐酸后白色沉淀溶解,将生成的气体通入品红溶液中,溶液褪色 取少量试液于试管中,向其中加入足量稀盐酸后,再加入BaCl2溶液 2溶液后生成白色沉淀 加热浓缩溶液,加入浓硫酸和铜片 有红棕色的气体产生,溶液变蓝色 S2‒ ①稀硫酸或盐酸;②Pb(NO3)2溶液、稀硝酸 ①生成无色有臭鸡蛋气味的气体;②生成黑色沉淀,且不溶于稀硝酸 7.常见气体的检验 待检物 检验方法 注意事项 O2 使带火星的木条复燃 H2 纯净的H2在空气中燃烧发出淡蓝色火焰,混入空气后点燃有爆鸣声 CH4、CO等在空气中燃烧也发出淡蓝色火焰,且产物能使澄清石灰水变浑浊 SO2 无色,有刺激性气味;能使品红溶液褪色,加热后恢复红色;能使酸性KMnO4溶液褪色;能使溴水褪色;能使澄清石灰水变浑浊 CO2也能使澄清石灰水变浑浊,应注意区别;SO2的漂白原理与新制氯水的漂白原理不同 CO2 能使澄清石灰水变浑浊,能使燃着的木条熄灭 SO2也能使澄清石灰水变浑浊,N2也能使燃着的木条熄灭,应注意区别 NO 无色气体,接触空气时立即变为红棕色 Cl2 黄绿色,有刺激性气味,能使湿润的淀粉-碘化钾试纸变蓝 Cl2有毒,注意闻气味的方法 NO2 红棕色,有刺激性气味,通入水中生成无色溶液并产生无色气体,水溶液显酸性 NO2的颜色与溴蒸气相近,NO2溶于AgNO3溶液无沉淀生成,而溴蒸气溶于AgNO3溶液有淡黄色沉淀生成 HCl 无色,有刺激性气味,在潮湿的空气中形成白雾;用蘸有浓氨水的玻璃棒靠近时冒白烟;通入AgNO3溶液时有白色沉淀生成 HCl极易溶于水,做相关实验时应防倒吸 NH3 无色,有刺激性气味,能使湿润的红色石蕊试纸变蓝;用蘸有浓盐酸的玻璃棒靠近时冒白烟 NH3极易溶于水,做相关实验时应防倒吸 考试规范答题 (1)气体验满和检验操作 ①氧气验满:将带火星的木条平放在集气瓶口,若木条复燃,则说明收集的氧气已满。 ②可燃性气体(如氢气)的验纯方法:用排水法收集一小试管的气体,将大拇指摁住管口移近火焰,放开手指,若听到尖锐的爆鸣声,则气体不纯;若听到轻微的“噗”的一声,则气体纯净。 ③二氧化碳验满:将燃着的木条平放在集气瓶口,若火焰熄灭,则气体已满。 ④氨气验满:用湿润的红色石蕊试纸放在集气瓶口,若试纸变蓝说明气体已满。 ⑤氯气验满:用湿润的淀粉碘化钾试纸放在集气瓶口,若试纸变蓝说明气体已满。 (2)萃取分液操作 关闭分液漏斗活塞,将混合液倒入分液漏斗中,塞上塞子,用右手心顶住塞子,左手握住活塞部分,将分液漏斗倒置,充分振荡、静置、分层,在漏斗下面放一个小烧杯,先打开上口塞子再打开分液漏斗活塞,使下层液体从下口沿烧杯壁流下,上层液体从上口倒出。 (3)从某物质稀溶液中结晶的实验操作 ①溶解度受温度影响较小的:蒸发→结晶→过滤。 ②溶解度受温度影响较大或带结晶水的:蒸发浓缩→冷却结晶→过滤。 (4)粗盐的提纯 ①实验室提纯粗盐的实验操作依次为取样、溶解、沉淀、过滤、蒸发结晶、过滤、烘干。 ②若过滤时发现滤液中有少量浑浊,从实验操作的角度分析,可能的原因是过滤时漏斗中液面高出滤纸边缘、玻璃棒靠在单层滤纸一边弄破滤纸。 ▍ 编辑:Wulibang(ID:2820092099) ▍ 来源:综合网络 ▍ 声明:如有侵权,请联系删除;若需转载,请注明出处。返回搜狐,查看更多 |
【本文地址】
今日新闻 |
推荐新闻 |