初三化学填空题试题 |
您所在的位置:网站首页 › 分式函数怎么求反函数 › 初三化学填空题试题 |
初三化学填空题试题
|
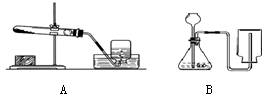
(16分)根据下图回答问题:
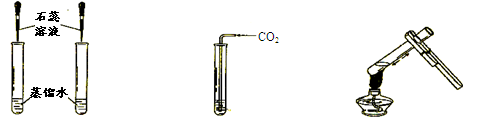
(1)若选用A装置用高锰酸钾制取氧气,还需补充的一种仪器是 (填名称),反应的化学方程式为: ; (2)实验室若选用B装置制取二氧化碳,则需要改正的一点是 , 请你写出用石灰石与稀盐酸反应制取二氧化碳的化学方程式 ; (3)用制取的二氧化碳进行如下实验:
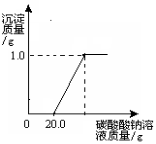
(I)向蒸馏水中滴入紫色石蕊溶液 (Ⅱ)向其中一支试管中通入二氧化碳 (Ⅲ)将通入二氧化碳的试管加热 ①实验(II)中溶液变为 色; ②实验(III)中加热之后,溶液又变为 色,解释出现此现象的原因 (用化学方程式表示)。 (4)同学们在做完“二氧化碳的制取和性质”实验后,废液缸中盛有大量的盐酸与氯化钙的混合溶液(不考虑其它杂质)。为了对废液进行处理,某同学做了如下实验:取废液缸上层清液20.0g于烧杯中,逐滴滴入溶质质量分数为5.3%的碳酸钠溶液直至过量,滴入碳酸钠溶液的质量与生成沉淀的质量的变化关系如图所示。
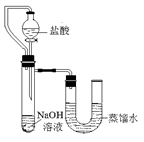
请计算: ①当废液中盐酸完全反应时,生成的二氧化碳的质量为多少? ②当废液中两种物质刚好消耗完毕时,所得溶液中溶质的质量分数为多少?(计算结果精确到0.1%) 九年级化学填空题极难题查看答案及解析 某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其证明与某盐酸发生了中和反应。 (1)配制100g质量分数为8%的氢氧化钠溶液。 ①计算:需要氢氧化钠固体的质量为________g,水的体积为mL(水的密度近似看作1g/cm3)。 ②称量:调节托盘天平平衡,将一个烧杯放在托盘天平的________盘,称量其质量。然后按需要添加砝码、移动游码,再将氢氧化钠固体加入烧杯中,直至天平平衡。该步骤中用烧杯而不用纸称量氢氧化钠的原因是________。 ③溶【解析】 用量筒量取所需的水,倒入盛有氢氧化钠固体的烧杯里,搅拌,使其溶解,并冷却至室温。 ④把配好的溶液装入试剂瓶,塞好橡皮塞并贴上标签。 (2)某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验。 【实验方案】 方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且最终小至小于7,则证明NaOH溶液与稀盐酸发生了化学反应。 ①用pH试纸测定NaOH溶液pH时,正确的操作是:________________。 ②简述强调“测得的pH小于7”的理由:。 方案二:化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生。如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应。该组同学在没使用温度计的情况下,通过下图所示装置完成了实验。则该组同学根据________
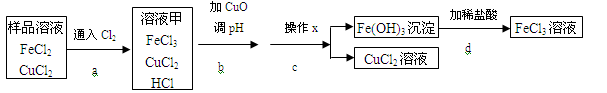
九年级化学填空题极难题查看答案及解析 在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液(主要含有FeCl2和CuCl2)处理和资源回收的过程简述如下: I:向废液中投入过量铁屑,充分反应后分离出固体和滤液; II:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。 试回答下列问题: ⑴过程I加入铁屑的主要作用是________;试写出其对应的化学方程式:________; ⑵从固体中分离出铜需采用的方法是________; ⑶滤液中溶质主要为________(写出化学式);已知过程II生成的最终产物为Fe(OH)3,则Fe(OH)2与氧气和水反应的化学方程式为:________。 九年级化学填空题极难题查看答案及解析 FeCl3可用作催化剂和外伤止血剂.某实验兴趣小组利用FeCl3腐蚀电路铜板后的溶液(主要成分为FeCl2、CuCl2)进行了氯化铁回收实验。 该实验小组同学通过查阅资料,进行了尝试。
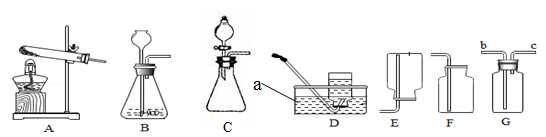
【阅读资料:】 不同金属氢氧化物可以在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液pH的方法,使金属氢氧化物依次沉淀,结合过滤等操作,进行物质分离。右表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH Fe(OH)3 Cu(OH)2 开始沉淀的pH 1.9 4.7 沉淀完全的pH 3.2 6.7 (1)进行操作x时,应用到的仪器有:铁架台、玻璃棒、烧杯和 。 (2)实验中,步骤b加入CuO消耗溶液甲中的HCl,使溶液pH增大到所需范围,请写出盐酸与氧化铜反应的化学方程式 ;你认为步骤b调节溶液的pH到 (填数值范围)比较合适。 (3)实验中,步骤d加稀盐酸前,因缺少 (填操作名称)而使获得的氯化铁溶液不纯。 (4)FeCl3溶液容易生成Fe(OH)3发生变质,在保存FeCl3溶液时,常向FeCl3溶液中加入某种酸,以防止FeCl3溶液变质,你认为选用 (用字母表示)最合理。 A.稀硝酸 B.稀硫酸 C.稀盐酸 D.稀醋酸. 九年级化学填空题极难题查看答案及解析 如图A~F是实验室制备某些常见气体的装置示意图.
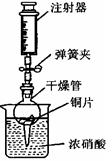
(1)装置图中仪器a的名称为 。 (2)用氯酸钾和二氧化锰混合共热制取氧气,写出反应的化学方程式: 。 (3)实验室利用B装置制取二氧化碳的化学方程式为 ,如果利用G装置收集二氧化碳,气体应从 端通入(填“b”或“c”),用C装置代替B装置作为发生装置,其主要优点是 。 (4)排水法收集与排空气法收集CO2的比较(分别用体积相同的2个集气瓶收集) 比较项目 排水法 向上排空气法 收集方法可行性分析 因为CO2气体生成和从水面逸出的速率远大于其溶解和与水反应的速率,所以可用排水法收集。 因为_________①_________,所以可用向上排空气法收集。 收集过程分析 用排水法收集CO2,集满现象是: ② “验满”分析:因气体无色,故集满与否较难确定.即便用燃着木条移近容器口火焰熄灭,也难以证明空气完全排尽 向收集到CO2的集气瓶内倒入等体积适量澄清石灰水,并振荡 先浑浊后变澄清所需时间较短 先浑浊后变澄清所需时间较长 由上述实验可得结论 与排空气法相比,排水法的优点是: ③ (5)查阅资料可知:在金属活动性顺序里,位于氢后面的金属Cu,在常温下虽然不能与稀盐酸、稀硫酸反应,但可以与无色硝酸溶液反应,其化学方程式为Cu + 4HNO3(浓)=Cu(NO3)2 + 2NO2↑+2H2O。 反应生成的NO2是红棕色、有刺激性气味的有毒气体。可用下图所示装置进行实验,请回答:
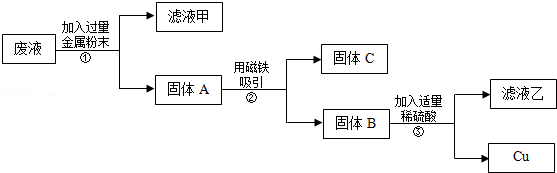
①检查装置的气密性:关闭弹簧夹,将干燥管放入带有水的烧杯中,若观察到_______________________,则表明该装置的气密性良好。 ②打开弹簧夹,用注射器慢慢抽取干燥管内的气体,浓硝酸沿着干燥管慢慢上升,直到硝酸与铜片接触,停止抽拉注射器,关闭弹簧夹,观察干燥管内的现象是:_____________________________________。 ③上述实验完成后,须用足量NaOH溶液将气体吸收,其目的是_____________________。 九年级化学填空题极难题查看答案及解析 在实验课中,各小组作了如下实验: 实验编号 1 2 3 4 实验操作 实验后,同学们按老师要求将废液都倒在指定的大烧杯中,小科猜想该烧杯中的废液可能有硫酸铜、硫酸锌、硫酸亚铁…,应该可以从中提炼出铁和铜.经思考后,他设计了如图所示的实验,并设法使滤液甲和乙所含的溶质相同.
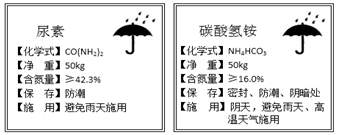
则固体C是________,操作③的名称是________,实验中所加的过量金属粉末是________. 九年级化学填空题极难题查看答案及解析 在世界范围内,据统计化肥对粮食增产的贡献率已超过40%,下图是两种氮肥标签的一部分。请根据图示中的信息回答下列问题:
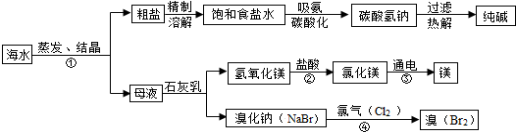
(1)从标签上看,碳酸氢铵不同于尿素的化学性质是____ _(填字母序号); A.易溶于水 B.受热易分解 C.有挥发性 (2)尿素的式量为____ _; (3)纯碳酸氢铵中氮元素的质量分数为_______________,这种碳酸氢铵肥料的纯度至少为___ __。(计算结果精确至0.1%) 九年级化学填空题极难题查看答案及解析 (11分)海水是巨大的资源宝库,利用海水为原料获得许多化工产品的流程如下图:
(1)实验室去除粗盐中难溶性杂质的一般步骤是:溶解、过滤、 、计算产率; (2)步骤①中选用蒸发结晶而不用降温结晶的理由是 。 (3)由上述流程图看出碳酸氢钠的热稳定性 (填“大于、小于或等于)纯碱的热稳定性。 (4)步骤②发生的反应属于 反应(填一种基本反应类型)。用镁制造的一种镁铝合金常用作生产飞机外壳的材料,该材料具有的优良性能有 (任答一点)。 (5)步骤④发生的反应为置换反应(类似于金属与盐溶液之间的反应), 反应后溴元素的化合价比反应前 (填“升高”或“降低”或“不变”)。 (6)通过海水为原料制取纯碱中会含有杂质氯化钠,为了测定纯碱中杂质氯化钠的质量分数,小阳同学进行了三次实验,实验数据如下表: 编 号 第 1 次 第 2次 第 3次 所取固体样品的质量/g 13 10 10 样品用98g水溶解后,加入CaCl2溶液的质量/g 100 100 125 反应后生成沉淀的质量/g 8 8 8 完成下列计算: ①固体样品中氯化钠的质量分数是 ; ②第 2 次反应结束后溶液中溶质质量分数是多少?(写出必要的计算题过程) 九年级化学填空题极难题查看答案及解析 (12分)以下是我们日常生活中常用各种清洗剂。 名称 洗涤灵 洁厕灵 炉具清洁剂 活氧彩漂 污渍爆炸盐 产品样式
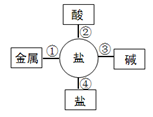
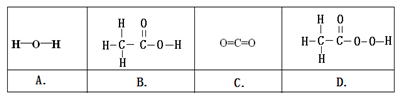
有效成分 或功能 清洗油污 盐酸 氢氧化钠 过氧化氢 过碳酸钠 (1)我们使用洗涤灵清洗餐具上的油污,这是因为它具有 的功能。 (2)清除以下物质,可以使用洁厕灵的是 填字母序号)。 A.铁锈 B.水垢(主要成分为碳酸钙和氢氧化镁) C.油渍 D.氢气还原氧化铜实验后,试管内壁残留的红色固体 (3)“污渍爆炸盐”溶于水后会生成Na2CO3和H2O2。将爆炸盐溶于水后,再加入足量的洁厕灵,产生能使澄清石灰水变浑浊的气体,这一反应了体现右图中 (选填①②③④)性质关系。
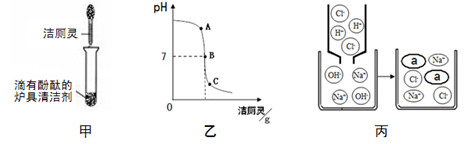
(4)将洁厕灵滴入炉具清洁剂中,如图甲所示。
①若反应后溶液呈红色,则反应后溶液中的溶质是(酚酞除外) ;此时溶液可用图乙中 点处(选填A、B、C)表示。 ②若反应后溶液pH为7,图丙中a微粒的化学式为 。 (5)①“活氧彩漂”可用于漂洗衣物、杀菌消毒等,原因是其有效成分过氧化氢分子中含有“过氧基”(—O—O—)。据此推测,下列物质中,可用作杀菌消毒剂的是 (填序号)。
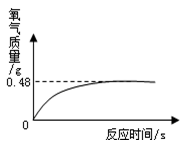
②氧化氢溶液常用于医用消毒,某兴趣小组为测定一瓶久置的医用过氧化氢溶液中溶质质量分数。他们取该溶液51g,加入适量二氧化锰,生成氧气的质量与反应时间的关系如图所示。试计算该过氧化氢溶液中溶质的质量分数。
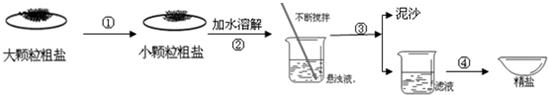
(写出计算过程) 九年级化学填空题极难题查看答案及解析 盐城濒临黄海,海盐文化全国知名.某兴趣小组同学去盐场参观,带回了部分粗盐样品,并对其进行了如下探究:
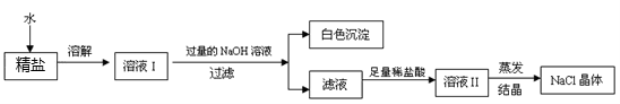
(1)操作①中必须用到的一种仪器是 (填序号) A.研钵 B.量筒 C.烧杯 D.试管 (2)操作③的名称是 ,操作④中用到玻璃棒,作用为 . (3)用提纯得到的“精盐”配制100g 7.5%的氯化钠溶液.经检测,溶质质量分数偏小,其原因可能有 (填序号) ①氯化钠固体不纯 ②称量时精盐与砝码放反了 ③量取水时俯视读数 ④装瓶时,有少量溶液洒出 (4)查阅资料得知:粗盐中除含少量泥沙等不溶性杂质外,还含有少量的可溶性杂质(假定可溶性杂质只有MgCl2一种),为了得到较纯净的氯化钠,小组同学将所得的“精盐”又作了如下处理:
①白色沉淀的化学式为 . ②在得到的滤液中加入足量的稀盐酸的目的是 . ③若实验过程中不考虑损耗,最终到的NaCl固体的质量将 (填“大于”、“小于”或“等于”)原精盐中NaCl的质量. 九年级化学填空题极难题查看答案及解析 |
【本文地址】