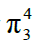大π键的计算方法 |
您所在的位置:网站首页 › 价电子对个数怎么算 › 大π键的计算方法 |
大π键的计算方法
|
1、概念: 由三个或三个以上的原子形成的π键。这种多个原子上相互平行的P轨道,它们连贯地“肩平肩”地重叠在一起而形成离域的化学键键,称其为大π键。 这种在化合物分子或离子中的π键电子不仅仅局限于两个原子的之间,而是在参加成键的多个原子形成的分子或离子骨架中运动。 2、形成条件: (1)所有参与形成离域π键的原子必须在同一直线或同一平面上。所以中心原子只能采取sp2或sp1杂化。 (2)参与离域π键的原子都必须提供一个或两个互相平行的P轨道。 (3) 形成离域π键的P电子的总数小于P轨道数的两倍。 3、表示方法
n为原子个数,m为共用电子个数,m ≦ 2n 4、m值的计算: ABn型分子或离子 m=价电子总数—σ键数×2—未参与的孤对电子个数 提醒:中心原子若有孤对电子,一定要把孤对电子从价电子总数中减去。 5、常见分子或离子的大π键 (1)ABn型分子 ①CO2:2个
m值计算:m=4+6×2-2×2-2×2=8 >2n,所以分为2个 等电子体:
②O3:
中心原子sp2杂化,所以中心原子中有1对孤对电子没有参与形成大π键 m值计算:m = 6×3-2×2-2-4×2 = 4 等电子体:
③ CO32-:
中心原子sp2杂化,中心原子的所有电子都参与成键 m值计算:m= 4+6×3+2-2×3-4×3 = 6
(2)环状分子 环上的原子都是sp2杂化
|
【本文地址】



 键
键