新药资讯:治疗肺动脉高压的潜在创新药物Sotatercept |
您所在的位置:网站首页 › 二期临床试验的一个重要目标 › 新药资讯:治疗肺动脉高压的潜在创新药物Sotatercept |
新药资讯:治疗肺动脉高压的潜在创新药物Sotatercept
|
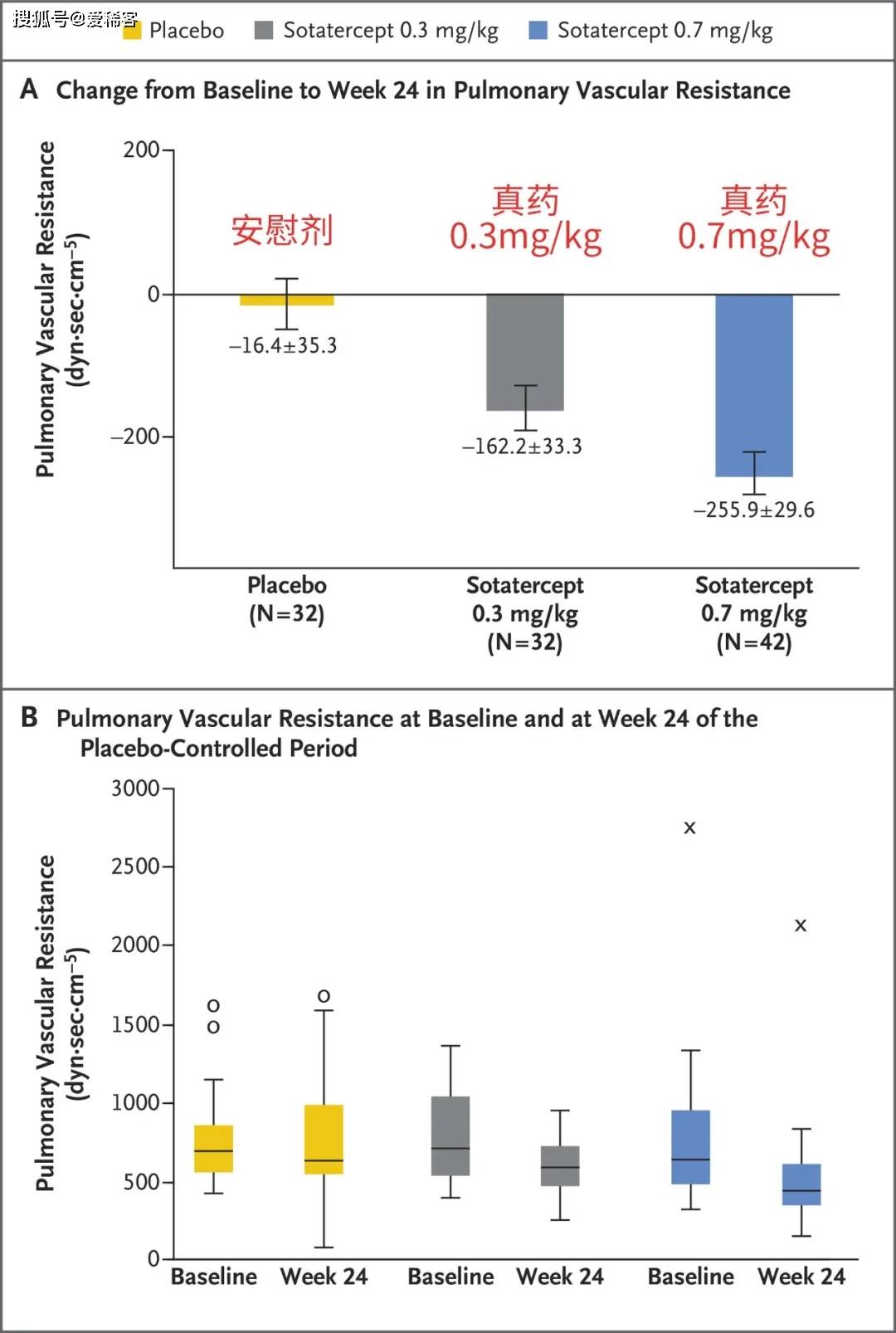
试验的主要终点是肺血管阻力从基线到第24周的变化,次要终点是6分钟步行距离。 划重点:临床试验终点指的是一些可衡量的指标,用于评估临床试验的结果。Sotatercept的这项临床试验主要终点是肺血管阻力从基线到第24周的变化,意思就是在试验第24周时,科学家主要根据每个参与试验的患者的肺血管阻力变化,来评估这项临床试验的结果;同时也会看次要终点,也就是6分钟步行距离。 入组患者的基线特征相似,经过24周的试验,结果显示:与安慰剂组相比,两个真药组的肺血管阻力有明显的下降;在真药组中,0.7mg/kg组比0.3mg/kg组肺血管阻力下降得更多(如下图所示)。
同时,试验还发现Sotatercept与NT-proBNP的降低有相关性。根据这些数据得出结论:在有接受背景治疗的肺动脉高压成人患者中,Sotatercept可以降低肺血管阻力;同时,6分钟步行距离和NT-proBNP水平也得到了一定的改善。 在这次临床试验中,最常见的不良事件是血小板减少和血红蛋白水平升高。0.7 mg/kg组中有1例患者死于心脏骤停。由于2期临床试验的样本相对少、持续时间短,尚未确定 Sotatercept 在此临床背景下的长期影响。目前,Sotatercept正处于多项治疗特定PAH患者的3期临床试验研究中。 划重点:2期临床试验一般只筛选少数患者入组,目的是初步评价药物对目标适应症患者的治疗作用和安全性。临床试验到了3期,才发展为大型临床试验,大量患者入组,评价新药的疗效和安全性,目的是获得足够的数据以向管理当局申请新药上市许可。现在,新药Sotatercept就处于3期临床试验中。 03 已获得FDA突破性疗法认定Sotatercept已经获得了美国食品药品监督管理局(FDA)授予的“罕见病药物”和“突破性疗法”认定,以及欧盟委员会和欧洲药品管理局(EMA)分别授予的治疗肺动脉高压(PAH)的罕见病药物和优先药物(PRIME)认定。 另外值得一提的是,近期出了个大新闻:这个新药的研发公司Acceleron有望被制药巨头默沙东以110亿美元收购,目前正在谈判中。观点认为,默沙东不惜斥巨资收购Acceleron的动力之一,就是看上了“被誉为Acceleron皇冠上的明珠的Sotatercept”。
这也可以从一个侧面说明,Sotatercept这个新药被认为有很大的潜在价值,有可能成为肺动脉高压治疗史上的一个里程碑。 大家一定要接受科学治疗,尽可能做到足量服药、定期随访,把病情稳住,耐心等待医学界放大招! 编辑:范小喵 排版:万怿玮
|
【本文地址】

 返回搜狐,查看更多
返回搜狐,查看更多