肿瘤靶点 |
您所在的位置:网站首页 › herceptin靶点 › 肿瘤靶点 |
肿瘤靶点
|
来源:雪球App,作者: 徐徐有米,(https://xueqiu.com/5943184518/226380992) 本文是肿瘤靶点系列之一,肿瘤靶点大概分为5大类: 1、肿瘤形成的靶点(形成/调控机制) 2、肿瘤生长的靶点(微环境) 3、发现肿瘤的靶点(特异性标志物) 4、消灭肿瘤的靶点(免疫调节) 5、找到肿瘤父亲的靶点(肿瘤干细胞)
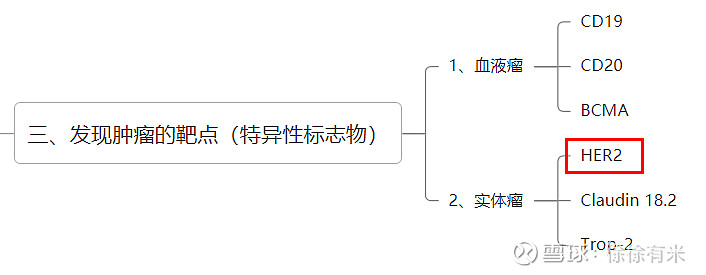
Her2是属于第3类肿瘤特异性标志物中的一个重要靶点,主要内容小结如下: 1、是迄今为止认识最为透彻的胃癌靶点、乳腺癌靶点; 2、HER2基因异常在膀胱癌,宫颈癌、胆管癌、结直肠癌、胃肠道癌症和肺癌等多种癌症中均有表现,在乳腺癌中是最常见的,在乳腺癌中已是公认的预测因子和治疗靶点。 3、在22%的胃癌以及28%的尿路上皮癌体现出高表达;在大约20%-30%的乳腺癌存在HER2基因的扩增或过表达; 4、1998年9月,赫赛汀(曲妥珠单抗)在美国上市;2012年,罗氏新一代的HER2抑制剂(帕妥珠单抗)在美国上市;2014年7月,赫赛汀的专利在欧盟到期(2019年6月,其美国专利也到期了)众多仿制药企纷纷涌进这条赛道。2019年12月,第一三共的ADC药物DS-8201在美国获批上市。 5、目前已上市的靶向HER2药物约15+,全球销售规模超过126亿美元;其中曲妥珠单抗和帕妥珠单抗近一年销量最高; 6、罗氏三大乳腺癌药物(全球第一款人源化 HER2 单抗、二代 HER2 单抗、全球首个单药治疗实体瘤的ADC),已建立起从最初的新辅助治疗、术后的辅助治疗、以及晚期一线治疗全程的抗 HER2 治疗体系,实现从早期到晚期的全程全覆盖。 7、在单抗、双抗、ADC、小分子几个方面均有药物上市: 单抗:1)曲妥珠单抗(赫赛汀),罗氏,1998年上市;2)帕妥珠单抗,罗氏,2012年上市;3)Incyte的Margetuximab,再鼎医药获大中华权益; 双抗:1)Zanidatamab,Zymeworks/百济,全球性3期临床试验,胃癌/胆癌;2)KN-026,康宁,乳腺癌/胃癌; ADC:1)曲妥珠单抗的ADC版本:恩美曲妥珠单抗;2)DS-8201,T-DXd,第一三共/阿斯利康,美国2019年上市,国内三期临床;3)维迪西妥单抗,代号RC48,荣昌生物 小分子:1)吡咯替尼,恒瑞,已上市; 下为细述。 一、历史: 1979年 Weinberg教授实验室的一名博士后研究员发现了一种特殊蛋白,后来它被命名为HER2。
1987年 这是乳腺癌治疗史上里程碑式的一年,加州大学洛杉矶分校的Dennis Slamon博士联手德克萨斯州立大学圣安东尼奥分校的Bill McGuire博士以及几名基因泰克的科学家共同发现,HER2过度表达和乳腺癌的发展有很大关系,导致了更低的生存率和更快的复发,HER2毫无疑问的成为了乳腺癌的一个潜在治疗靶点。
基因泰克人员开始了HER2单抗的研究,但一波三折,当时有其他制药公司的类似项目都失败了。
1990年 在Dennis Slamon的坚持研发下,第一支HER2抑制剂诞生,起名为Herceptin,取自HER2、阻断(intercept)和抑制剂(inhibitor)三个英文单词,这就是大名鼎鼎的“赫赛汀”,当年就在老鼠身上取得了不错的效果。但这样依然没有打动基因泰克,公司决定停止对该项目的赞助。
1992年 Dennis Slamon招募了37名罹患乳腺癌的妇女参加临床试验,不过试验效果很不理想,只有5人完成所有试验,其中一位取得了很好的治疗效果。
1993年 一名女医生尼尔森·纳尔逊罹患乳腺癌,她向基因泰克申请“特许使用”赫赛汀,被公司拒绝,不久后告别人世。此事在乳腺癌患者群体中引发轰动。
1994年 12月5日,她们闯入基因泰克公司的园区,并开进15辆车为女医生纳尔逊“送葬”,表达不满。这件事成为基因泰克1976年成立以来最大的一次公关危机事件。
1996年 基因泰克无奈重启HER2靶向药物的研究。
1998年 一项大型III期临床试验结果公布,单抗与化疗药物的联用确实减缓了患者的肿瘤进展,延长了患者的生存期; 9月,赫赛汀(曲妥珠单抗)在美国上市,成为全球第一个靶向生物药,斯拉蒙也被人称为“赫赛汀之父”。赫赛汀也是第二款获批上市的新型生物抗癌药物。
2002年 中国国家药监局批准赫赛汀在国内上市,当时每支价格高达2.2万元,高昂的价格一度让很多中国乳腺癌患者望而却步。
2007年 第一三共成立:日本的第一制药株式会社和三共株式会社谋求合并。第一制药在抗癌化药方面积累深厚,三共制药则在人源化抗体领域有所特长,合并后,ADC药物很快就被确定为新成立的“第一三共”的重点项目。
2010年 FDA批准靶向HER2的单克隆抗体曲妥珠单抗(赫赛汀)联合化疗一线治疗HER2阳性转移性胃癌,使HER2成为胃癌治疗的明星靶点,该疗法也成为HER2阳性晚期胃及胃食管结合部(GEJ)腺癌患者的标准一线治疗方法。
2012年 罗氏新一代的HER2抑制剂帕妥珠单抗在美国上市。
2014年 7月,赫赛汀的专利在欧盟到期(2019年6月,其美国专利也到期了)众多仿制药企纷纷涌进这条赛道。
2017年 赫赛汀通过医保谈判,价格降为每支7600元,降幅高达70%; 诺华与葛兰素史克联合开发的HER2小分子靶向药物拉帕替尼也通过2016年医保谈判,该药在中国被推荐用于接受过包括蒽环类、紫杉类、曲妥珠单抗治疗的晚期或转移性乳腺癌患者; 在中国,赫赛汀的“仿制药”一直未能取得突破,国家药监局药品审评中心下发“英雄帖”,号召国内企业加快开发曲妥珠单抗类似药。 8月末,第一三共研发的DS-8201得到了美国FDA颁发的突破性疗法认定。很快,阿斯利康注意到了这款产品。
2018年 恒瑞研发的HER2靶向小分子药物吡咯替尼上市; 12月,帕妥珠单抗获批在中国上市,并纳入医保。罗氏从此奠定在HER2大分子靶向药物上绝对的领导地位。到目前为止,罗氏两款名字带“妥”的单抗,依然是业内公认、一线治疗乳腺癌妥妥的选择。
2019年 3月,阿斯利康以69亿美元的价格获得了DS-8201在日本地区以外的商业化权益。 12月,DS-8201在美国获批上市。
2020年 恒瑞的吡咯替尼被纳入国家医保目录。临床数据显示,曲妥珠单抗治疗失败后,吡咯替尼+卡培他滨的方案在各项指标上有望挑战拉帕替尼的地位; 4月,罗氏在中国又有一款抗体偶联药物(ADC)恩美曲妥珠单抗上市,这款曲妥珠单抗和小分子细胞毒素药物DM1偶联的药物也是国内上市的首个ADC药物; 6月,三生国健的HER2抑制剂伊尼妥单抗获批,成为国内HER2靶点首个生物新药; 8月18日,复宏汉霖成功开发中国第一个赫赛汀的生物类似药获批上市(华兰生物、正大天晴等企业曾进行过研究,但均未取得最终成果。)
2021年 1月15日获FDA批准Enhertu上市,用于治疗先前接受过曲妥珠单抗治疗的HER2阳性局部晚期或转移性胃或食管胃结合部(GEJ)腺癌成人患者,它的出现标志着针对HER2靶点胃癌二、三线疗法宣告成功。 6月,恩美曲妥珠单抗(T-DM1,罗氏)单药用于接受了紫杉烷类和曲妥珠单抗治疗的HER2阳性、不可切除局部晚期或转移性乳腺癌患者的适应症在国内获批,标志着我国晚期乳腺癌正式迈入抗HER2治疗ADC新时代。 9月,欧洲肿瘤科学会全体大会上公布了DS8201疗效好于罗氏的ADC恩美曲妥珠单抗,后者疗效已经好于罗氏第一代单抗曲妥珠单抗,自此,DS-8201就像一团阴影,笼罩在罗氏的“曲妥珠城堡”之上。 11月,美国国家综合癌症网络NCCN更新了《乳腺癌临床实践指南(2022年第一版)》。在针对HER2阳性、复发性不可切除或IV期疾病的全身治疗的二线方案中,DS-8201取代恩美曲妥珠单抗,成为1类首选方案,罗氏的ADC被换到2a类或其他方案中。美国更新诊疗指南,对于全球乳腺癌的治疗均有借鉴意义。
2022年 3月,DS-8201在中国的上市申请获受理; 4月,DS-8201治疗既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性乳腺癌成人患者获中国国家药监局突破性疗法认证。 上半年,罗氏对恩美曲妥珠单抗的价格进行调整,规格100mg的价格由近2万元降至不足8500元;160mg的价格由2.7万余元降至1.3万余元,降幅超过55%。
二、靶点介绍: 1、靶点: 人表皮生长因子受体是一个小家族,有4位成员——HER1、HER2、HER3和HER4。作为跨膜蛋白,它们可以在细胞表面与生长因子结合,进行信号传导,调节细胞的生长、分裂和修复。在正常细胞中Her2的表达水平极低。 HER2 的过表达与许多上皮细胞癌症的恶性化程度关系密切,Her2高表达肿瘤表现出极强的迁移性和浸润性、化疗药物敏感性差、愈后差、易复发等特点。 HER2阳性,意味着该基因发挥作用,抑制细胞凋亡,促进增殖,大大增加癌细胞的侵染力。 类似于PD-1,HER2基因异常在膀胱癌,宫颈癌、胆管癌、结直肠癌、胃肠道癌症和肺癌等多种癌症中均有表现,在乳腺癌中是最常见的,在乳腺癌中已是公认的预测因子和治疗靶点。
2、机制: 只要阻断HER2与生长因子的结合,那么疯狂的癌细胞的末日也就不远了。 单抗可以“代替”生长因子与HER2结合,阻止调节细胞生长增殖的信号的传递。
3、各癌种表达量: 在22%的胃癌以及28%的尿路上皮癌体现出高表达; 在大约20%-30%的乳腺癌存在HER2基因的扩增或过表达,这意味着,这部分乳腺癌患者的每个癌细胞上有高达200万个HER2,是正常标准的100倍!过多HER2的存在导致了细胞增殖的失控和肿瘤的发展,这部分患者也因此具有更低的生存率和更快的复发。
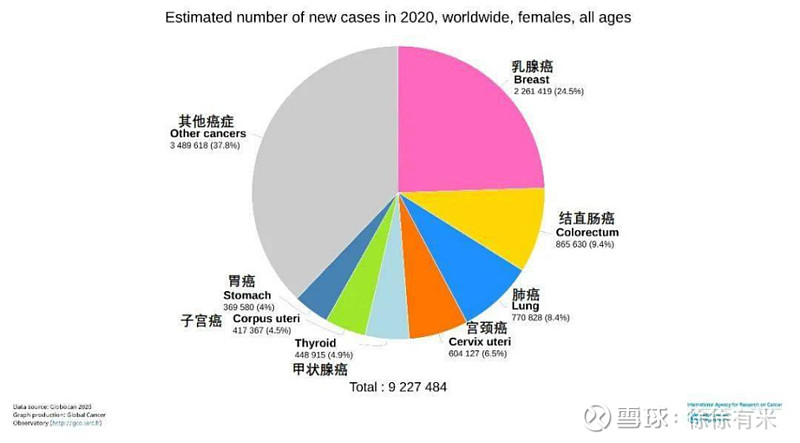
4、适应症规模和情况: 1)乳腺癌: 据估计,2020年全球新发癌症病例1929万例,死亡病例996万例:2020年乳腺癌新增人数为226万,肺癌为220万,乳腺癌超过肺癌,首次成为全球第一大癌症,约占新发癌症病例的 11.7%。 中国乳腺癌的情况更为严峻。国家肿瘤质控中心乳腺癌专委会副主委马飞曾表示:中国的乳腺癌发病率的增长速度超过全球平均水平。中国新发乳腺癌 41.6 万例,占女性新发癌症总数的 19.9%,排名第一。
2020年 全球女性癌症新发病例数和类型分布 2)胃癌: her2阳性胃癌患者占胃癌40%左右,每年有7-8万新增; 化疗在过去几十年里仍然是一线治疗的首要选择,然而化疗的治疗效果有限,晚期或转移性胃癌患者的5年生存率只有5%。 自2010年赫赛汀获批联合化疗作为一线疗法试验之后,各种针对HER2靶点的胃癌二线疗法都相继失败。
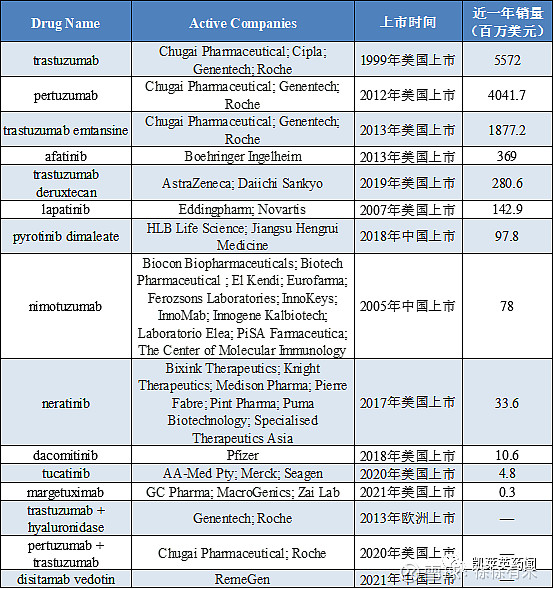
三、上市药/在研现状: HER2抗体药物以高特异性、有效性和安全性等优势, 在肿瘤、自身免疫病等重大疾病的治疗中取得突破, 已成为全球医药产业中发展速度最快、潜力最大的领域之一。 1、销售额和销售规模: 据不完全统计,目前已上市的靶向HER2药物全球销售规模超过126亿美元(根据已上市药物的销量进行预测:可知未来五年市场呈现上升趋势,随着相关药物的陆续获批,2025年预测销量至少在150亿美元以上,年均复合增长率8.09%。) 其中trastuzumab(曲妥珠单抗)和pertuzumab(帕妥珠单抗)近一年销量最高。 曲妥珠单抗上市至今已给罗氏带来超过1000亿美元回报。
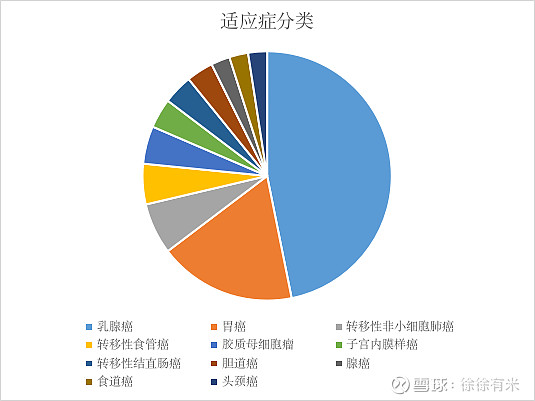
2、在研药物的适应症(21年9月底数据): 其中针对乳腺癌的药物134个,胃癌的药物51个,转移性非小细胞肺癌药物19个,转移性食管癌药物15个,卵巢癌药物15个,胶质母细胞瘤药物14个,子宫内膜样癌药物11个,转移性结直肠癌药物11个,胆道癌药物10个,腺癌药物7个,食道癌药物7个,头颈癌药物7个。
3、在研的企业(21年9月底数据): 海外:Roche拥有该靶点药物8个,Genentech拥有7个,NantKwest拥有6个,NantCell拥有5个,3SBio拥有4个,Biocad拥有4个,Chugai Pharmaceutical拥有4个,EirGenix拥有4个,Immunwork拥有4个,Marker Therapeutics拥有4个,Refuge Biotechnologies拥有4个; 国内企业:齐鲁(5)、苏州康宁杰瑞(4)、海正(4)、恒瑞(3)、复宏汉霖(3)、百济(2)、康缘(2)、正大天晴(2) 罗氏三大乳腺癌药物(全球第一款人源化 HER2 单抗、二代 HER2 单抗、全球首个单药治疗实体瘤的ADC),已建立起从最初的新辅助治疗、术后的辅助治疗、以及晚期一线治疗全程的抗 HER2 治疗体系,实现从早期到晚期的全程全覆盖。
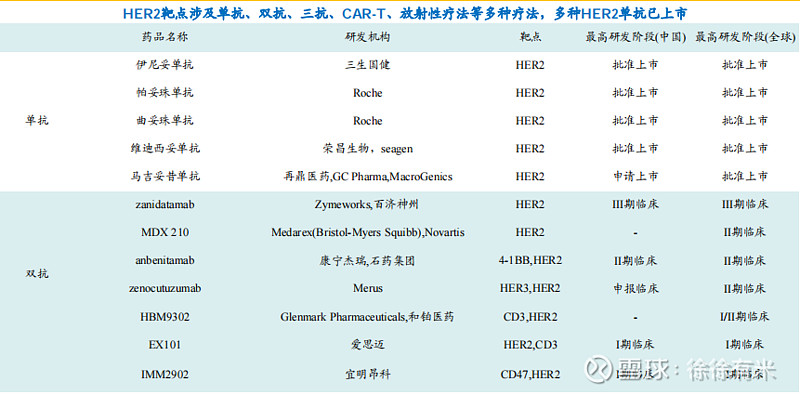
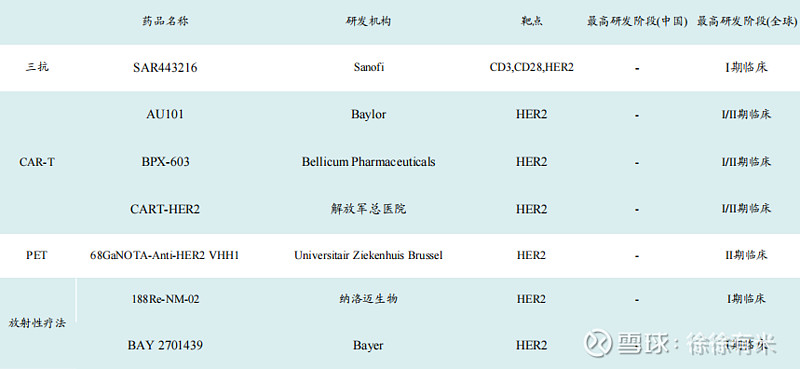
4、除ADC外,在研汇总:
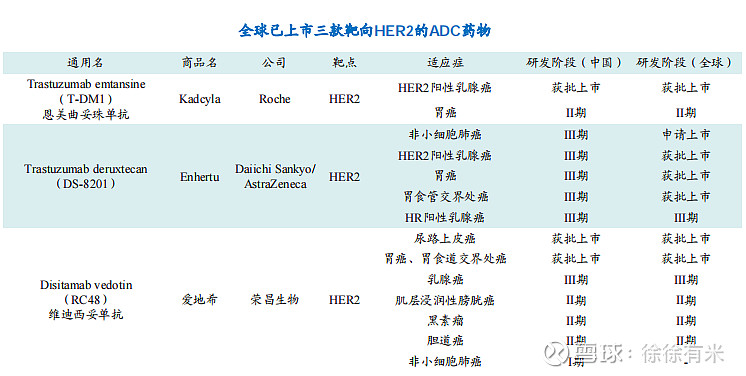
5、ADC在研情况: 全球已有9款ADC药物获批上市,3款为HER2;
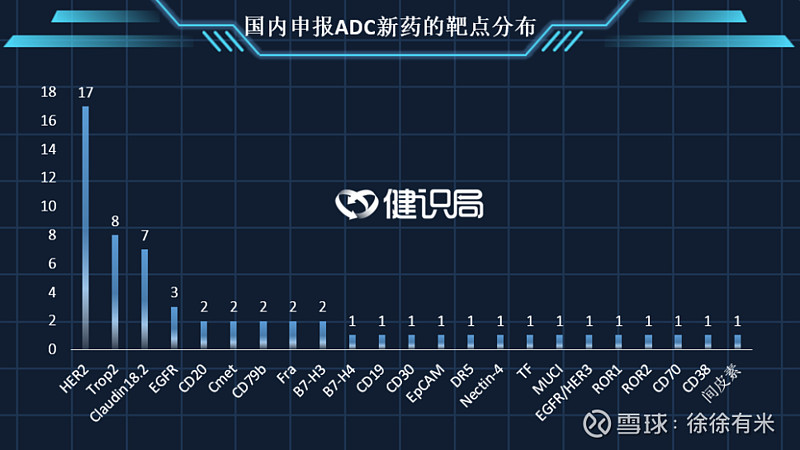
中国市场有三款ADC ,分别是罗氏的恩美曲妥珠单抗(HER2)、荣昌生物的维迪西妥单抗(HER2)、云顶新耀的戈沙妥珠单抗(TROP2),荣昌生物和罗氏的产品适应症有所错开; ADC崛起的时候,国内企业快速跟上了这一潮流:截至6月初,全球共有200多个进入临床阶段的ADC项目,其中国内占近60个。 国内在研ADC中,靶向HER2的占比最多,这些品种多借鉴了恩美曲妥珠单抗(随时获批上市的DS-8201可能会对这些产品构成降维打击。)
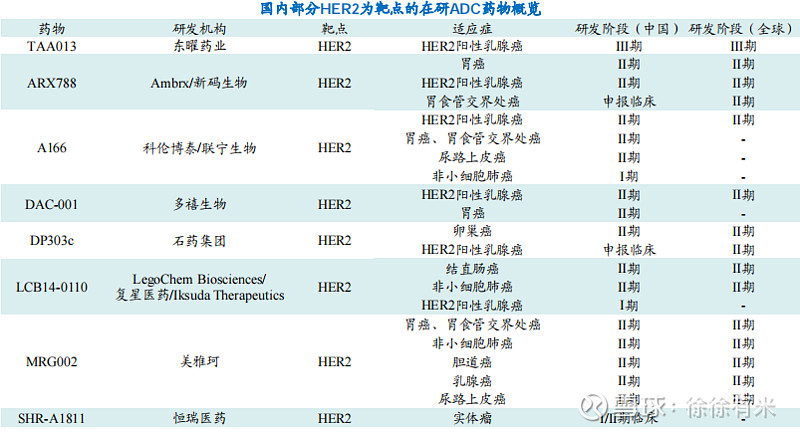
国内部分HER2的ADC在研:
四、重点药:
罗氏、第一三共称王,其他各家各有千秋 再鼎有一款单抗,百济、康宁各有一款双抗,恒瑞有一款小分子
1、单抗: 1)曲妥珠单抗(赫赛汀),罗氏,1998年上市 20多年来,曲妥珠单抗成为乳腺癌治疗的最优选对象,是目前临床上针对HER2阳性乳腺癌最常用的药物,一上市便取得巨大的成功,长期占据全球药物销售TOP10榜单,为罗氏贡献了超1000亿美元的营收。 原理:通过直接与癌细胞表面的HER2相结合,激活淋巴细胞释放细胞毒性物质,促使癌细胞凋亡。 疗效:2021年7月,英国《柳叶刀》在线发表7项随机对照试验13864例早期HER2阳性乳腺癌女性研究结果表明,对于早期HER2阳性乳腺癌,曲妥珠单抗+化疗与单用化疗相比,无论记录在案的患者特征和肿瘤特征如何,乳腺癌复发率和乳腺癌死亡率可减少三分之一。 胃癌方面:曲妥珠单抗联合化疗中位总生存期(mOS)更长(13.8月 VS 11.1月),中位无进展生存期(mPFS)也更长(6.7月 VS 5.5月),客观缓解率(ORR)更大, 疾病控制率(DCR)也更大(78.9% VS 69.3%),试验具有里程碑式的意义,它是全球第一个证明靶向治疗能延长晚期胃癌生存时间的大型III期临床试验,曲妥珠单抗也成为了第一个在胃癌上探索成功的分子靶向药物,宣告了胃癌靶向治疗时代的到来。
2)帕妥珠单抗,罗氏,2012年上市 靶向Her2的单抗药物,和曲妥珠单抗与Her2蛋白的结合位点不同,帕妥珠单抗+曲妥珠单抗联合使用则可以充分阻断Her2信号通路,起到协同增效的作用。 帕妥珠单抗在HER2阳性晚期乳腺癌一线治疗中的获批。 疗效: 持续长达8年随访的CLEOPATRA研究和来自中国人群的PUFFIN研究的两项研究结果: CLEOPATRA研究显示帕妥珠单抗+曲妥珠单抗联合多西他赛可以使HER2阳性晚期乳腺癌患者的PFS延长51%,达到18.7个月,患者OS延长40%,生存期可延长至近5年; PUFFIN研究是CLEOPATRA的桥接研究,显示帕妥珠单抗联合曲妥珠单抗双靶组较对照组患者的复发和死亡风险降低了31%,中位PFS为14.5个月,对照组为12.4个月。
3)Margetuximab,再鼎医药 由Incyte和MacroGenics开发,再鼎医药获得在大中华区的独家开发与推广许可。 Margetuximab与曲妥珠单抗具有相似的HER2结合和抗增殖作用,通过对抗体进行改造,增强了它的细胞毒性。 适应症和疗效: 在2021 ESMO大会上,MacroGenics公司公布了其与抗PD-1抗体联用,一线治疗HER2阳性,PD-L1阳性的胃食管腺癌(GEA)患者的临床结果:截至2021年7月19日,在40名可以评估疗效的患者中,21名获得缓解(53%,95% CI,36%-69%)。在接受过至少一次病灶扫描的41名患者中,32名患者的肿瘤缩小(78%);患者的疾病控制率为73%,中位缓解持续时间为10.3个月,中位无进展生存期为6.4个月;在12和18个月时,总生存率为85%;使得它具有成为一线治疗HER2阳性胃癌患者的潜力。
2、双抗: 1)Zanidatamab,Zymeworks/百济,全球性3期临床试验,胃癌/胆癌 百济神州在2018年11月以4000万美元的首付款,至多3.9亿美元的潜在里程碑付款获得在亚洲(日本除外)、澳大利亚和新西兰的开发和推广的独家授权。 原理: 通过与HER的两个非重叠表位结合,产生多种作用机制,包括双重HER2信号阻断、增加HER2蛋白从细胞表面的清除,以及提高抗体介导的细胞毒性作用,从而提高抗癌活性。 成就: 2020年12月,美国FDA已授予zanidatamab突破性疗法认定,用于治疗HER2基因扩增的经治胆道癌(BTC)患者。 疗效: 在2021 ESMO上报告的最新结果显示:zanidatamab与化疗联用,在28名可以评估疗效的HER2阳性转移性胃食管腺癌患者中,达到75%的客观缓解率(ORR)和89%的疾病控制率。在28名患者中,只有1名患者的肿瘤没有缩小;中位缓解持续时间为16.4个月,中位无进展生存期为12.0个月。
2)KN-026,康宁,乳腺癌/胃癌 一款抗HER2双特异性抗体,可以同时结合HER2的两个非重叠表位,阻断HER2信号。 适应症: 临床前研究数据显示,在HER2阳性肿瘤细胞株中,KN-026具备优效的肿瘤抑制作用;同时,KN-026对HER2中低表达肿瘤和曲妥珠单抗抗性细胞株也有抑制作用。 1期临床试验结果表明,KN-026具有良好的耐受性和安全性,在多线抗HER2治疗后进展的HER2阳性乳腺癌患者中仍然表现出显著的抗肿瘤活性。 同时,KN026 对 HER2 中低表达肿瘤和曲妥珠单抗抗性细胞株也有抑制作用。 进度方面: 目前,正在开展多项关键2期临床试验,包括针对HER2低表达或阳性乳腺癌、晚期HER2阳性胃和胃食管结合部癌及其他HER2阳性实体瘤等适应症。
3、ADC:
1)曲妥珠单抗的ADC版本:恩美曲妥珠单抗
由罗氏开发的、全球首个单药治疗实体瘤获批的ADC ADC版本的曲妥珠单抗,效果比单用曲妥珠单抗高出一个等级,具有靶向性和细胞毒杀伤的双重抗肿瘤作用,能有效突破抗HER2治疗耐药和患者生存期延长的瓶颈,将使新辅助治疗后仍残存病灶的 HER2 阳性早期乳腺癌患者复发或死亡风险降低 50%。 疗效: 与拉帕替尼+卡培他滨相比,T-DM1显著延长了患者的中位PFS(9.6 vs. 6.4个月, HR=0.650,P |
【本文地址】
今日新闻 |
推荐新闻 |