【重磅综述】皮肤衰老的机制和对全身衰老的影响 |
您所在的位置:网站首页 › fmvp2021皮肤 › 【重磅综述】皮肤衰老的机制和对全身衰老的影响 |
【重磅综述】皮肤衰老的机制和对全身衰老的影响
|
以下文章来源于老顽童说 ,作者老顽童说  老顽童说. 公众号致力于传播衰老相关的前沿科研进展和趣味科普,帮助大家更深入地了解衰老背后的科学故事~ 关注我们,获取更多相关资讯 皮肤是人体最大的器官,其重要性不言而喻。随着年龄的增长,衰老的皮肤细胞逐渐积累,并可通过旁分泌方式将衰老表型传递到邻近细胞,导致皮肤厚度、再生能力和屏障效应降低,进而会对全身多种功能产生影响。科英布拉大学的Cláudia Cavadas团队于2022年2月在Trends in Molecular Medicine上发表题为“Skin senescence: mechanisms and impact on whole-body aging”的综述,详细阐述了皮肤老化的机理,并为通过靶向皮肤衰老来延缓全身衰老的临床研究策略提供了新思路。 摘 要 皮肤是机体最大的器官,起着重要的保护作用。与其他组织一样,皮肤衰老不仅会受到内源性变化带来的影响,还会受到由环境引发的外在因素的影响。衰老的皮肤在结构、细胞和分子水平都会发生变化,还会出现衰老细胞的积累。这些衰老细胞可以诱导或加速皮肤或其它组织细胞的衰老相关功能障碍。然而,其程度和潜在的机制仍然未知。在本文中,作者讨论了皮肤衰老在诱导其他器官或组织产生衰老表型、加剧全身衰老方面的相关影响。此外,文章认为局部施用延缓衰老或治疗类药物可以改善全身衰老表型。 亮 点 随着年龄的增长,衰老细胞在皮肤中积聚并影响邻近细胞衰老,导致皮肤厚度、再生能力和屏障效应能力降低。 皮肤老化和细胞衰老表型与免疫衰老、寿命以及心血管疾病患病风险相关。 由紫外线辐射诱导的皮肤老化通过减少海马神经发生、激活下丘脑中部—垂体—肾上腺轴,从而对大脑产生影响。 抗衰老类药物,如达沙替尼和非瑟酮,能够选择性清除衰老细胞,并已有临床试验对其进行皮肤的局部施用,显示出潜在的延缓衰老的效应。 术语表 细胞外囊泡(EVs):脂质双层结构,由细胞分泌到细胞外空间,可以包裹核酸、蛋白质或脂质。EVs可以被受体细胞吸收,对靶细胞发挥各种作用。 内在衰老(Intrinsic aging):由时间变化引起的遗传程序性衰老类型,也称为按时间顺序的衰老。 外在衰老(Extrinsic aging):由于暴露于有害环境或因生活方式引起的皮肤衰老类型。 免疫衰老:进行性功能障碍和免疫功能下降,通常与衰老或衰老相关疾病有关。 炎症老化:与年龄相关的慢性低度炎症状态。 光老化:由紫外线辐射引起的外在皮肤衰老类型。 分泌蛋白质组:由特定细胞分泌的整套蛋白质。 旁分泌衰老:由初代衰老细胞分泌蛋白组引起的细胞衰老。 衰老相关分泌表型(SASP):衰老细胞分泌的一组促炎、促血管生成和生长刺激因子,可对细胞微环境和周围细胞产生影响。 下丘脑—垂体—肾上腺(HPA)轴:由下丘脑、垂体和肾上腺组成的神经内分泌单元,通过整合生理和内分泌信号,在身体稳态和对压力反应中发挥核心作用。 神经发生:通过干细胞分化在大脑中产生新神经元的过程。 抗衰老类药物:选择性清除衰老细胞的一类药物,可以靶向组织内衰老细胞。 皮肤衰老是系统性衰老的触发因素 衰老被定义为生理衰退的渐进过程,可引发衰弱以及增龄相关疾病,并最终导致死亡。细胞衰老是一种应对破坏性刺激的防御机制,导致组织功能随着年龄的增长而衰退,被认为是衰老的标志之一。 衰老细胞停止增殖,但仍可保持代谢活性,并分泌相关因子(被统称为衰老相关分泌表型SASP,见术语表)。SASP会进而诱导其它正常细胞的衰老。皮肤衰老细胞随着年龄增长而逐渐积累,由于其不同的衰老机制,将直接影响皮肤结构和功能。 皮肤含有多个系统来源的细胞类型,如神经、免疫、循环和内分泌系统。皮肤中的神经内分泌系统维持皮肤和大脑之间的交流。一些证据表明皮肤衰老与机体衰老和年龄相关功能障碍有关。 认识皮肤衰老对全身衰老的影响可能有助于全身衰老延缓和年龄相关疾病治疗的新方法研究,例如使用有效抗衰老类药物靶向皮肤衰老细胞来延缓机体衰老。因此,文章深入讨论了皮肤衰老是否具有导致其他器官或组织衰老,加速全身衰老的关键调控功能。 皮肤老化和衰老 皮肤是人体最大的器官,是抵抗外界环境的物理屏障,因此长期暴露于外界环境中(框1)。在人的一生中,幼年与老年时期会表现出明显的皮肤差异(图1)。皮肤衰老,由时间变化引起的称为内在衰老,而由环境因素引起的,例如空气污染、吸烟、营养不良和紫外线(UV)等,称为外在衰老。 内在衰老是由时间变化引起的,导致细胞损伤的积累,其特征是皮肤变薄、产生细纹。厚度降低可能是由于细胞增殖减少以及随着年龄增长引起的真皮成分发生显著变化导致的。细胞外基质(ECM)成分(胶原蛋白、弹性蛋白、糖胺聚糖等)随着皮肤内在衰老而显著减少。此外,伴随增龄,多种因素如线粒体损伤、炎症反应等产生的活性氧增加,同时,与年龄相关的细胞修复能力下降,使得氧化应激增加,从而导致了皮肤的内在衰老。 皮肤中存在几种具有强有丝分裂能力的细胞类型,随着年龄增长,这些分裂能力强的细胞逐渐达到了细胞分裂极限,表现为复制性衰老,并逐渐在皮肤中累积,导致皮肤中的衰老细胞增多。细胞衰老对皮肤而言是有益的,因为它可以促进伤口愈合并防止肿瘤病变。事实上,激活细胞周期停滞相关通路(框2)对于预防皮肤癌至关重要。诱发肿瘤的刺激与诱导皮肤细胞衰老的刺激(如紫外线)是相似的。 框1. 皮肤结构和作为环境传感器的功能 皮肤分为三个结构层:表皮、真皮和皮下脂肪层。表皮是具有永久增殖和更新能力的复层上皮,包括不同形态和功能的分层。底层通常是单层细胞,由增殖细胞组成,当它们向表皮最外层(由角质细胞组成)移动时会发生终末分化。该层最常见的细胞类型是角质形成细胞,同时也发现了其他细胞类型,例如朗格汉斯细胞(抗原呈递细胞),默克尔细胞(应激敏感细胞)和黑色素细胞。表皮黑色素在黑色素细胞的黑素体中产生,具有重要的光保护作用。简而言之,黑色素生物合成通常始于氨基酸L-酪氨酸,被该过程中的关键调节酶酪氨酸酶羟基化为L-二羟基苯丙氨酸(L-DOPA)。L-DOPA被进一步氧化成前体多巴醌,多巴醌可转化为真黑素(黑色或棕色)或褐黑素(黄红色)。黑色素细胞将成熟的黑素体转移到表皮角质形成细胞上,表皮角质形成细胞在细胞核上形成保护帽。 黑色素生成主要由促黑激素(MSH-α)和促肾上腺皮质激素(ACTH)调节,它们起源于阿黑皮素原(POMC)分裂,激活黑皮质素受体MC1-R,并刺激褪黑素活性。紫外线辐射(UVR)是黑色素发生中最相关的调节因子,可增加表皮黑色素合成,从而赋予光保护能力。UVR促进黑素细胞增殖和积累、树突数量增加以及黑素体转移到角质形成细胞中。 真皮主要由ECM组成,具有两种主要蛋白质纤维类型(胶原蛋白和弹性蛋白)和糖胺聚糖。真皮的细胞成分包括成纤维细胞、真皮树突胶质细胞和肥大细胞。皮下脂肪组织不被认为是皮肤的一部分,然而,它在体温调节和能量储存方面具有重要作用,能够提供缓冲和保持皮肤稳定性。 皮肤是内部和外部环境之间的接口。鉴于其位置,皮肤识别并整合环境相关因素,并在处于某种刺激的临界阈值时协调生物反应。皮肤对应激的反应由皮肤神经内分泌系统介导。具体而言,皮肤具有系统性HPA的所有分子成分,皮肤驻留细胞能够合成并表现出几种神经内分泌激素的受体,包括POMC、ACTH、β-内啡肽(β-endorphins)、促肾上腺皮质激素释放激素(CRH)、尿皮质激素(urocortin)等。此外,皮肤参与类固醇生成和性激素转化。糖皮质激素,包括皮质醇或皮质酮,在皮肤中合成,此过程受环境因素调控。 根据刺激的类型和强度,皮肤可以通过神经传递或皮肤衍生因子(例如细胞因子或激素)激活中枢HPA系统到中枢神经系统。 这些系统存在于人类和啮齿动物的皮肤中,并且具有差异性,特别是在CRH方面。与人类皮肤相反,CRH mRNA在小鼠中的表达水平极低,这表明蛋白质CRH通过神经递送到皮肤。人类和小鼠皮肤也表现出CRH受体(CRH-R1和CRH-R2)的相反表达。CRH-R2在人体皮肤中很少表达,而优先在小鼠皮肤中表达;这些差异可能可以解释小鼠毛皮和夜间行为,这极大减少了皮肤暴露于UVR时对应激系统(如CRH系统)的需求。因此,皮肤不仅仅是一个屏障,还是一个动态器官,在维持有机体体内平衡方面起着至关重要的作用。 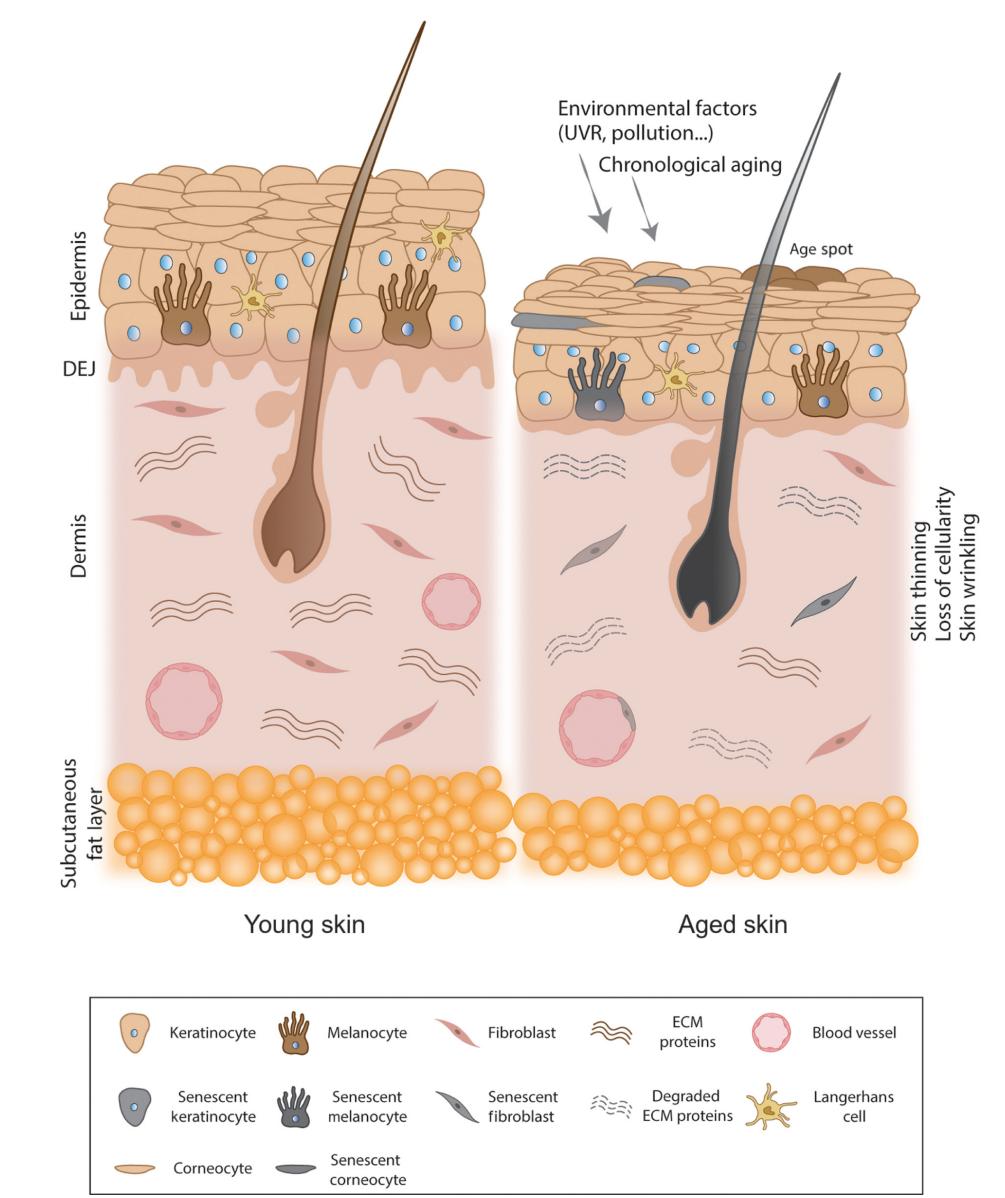 图1. 年轻和年老皮肤。年轻(左)和年老皮肤(右)示意图。皮肤随着时间变化(按时间顺序老化)和暴露于环境因素(外在衰老)而衰老。衰老的皮肤通常表现为皮肤皱缩,这是由于皮肤细胞的增殖能力降低和细胞外基质蛋白(如胶原蛋白或弹性蛋白)的减少或降解。同时,真皮表皮连接(DEJ)发生扁平化,是导致皮肤完整性丧失和皮肤皱纹发展的原因,是皮肤衰老的主要标志。皮肤色素沉着变化,不仅发生在皮肤,也发生在头发,并且由于黑色素细胞的活动功能障碍,该变化在衰老过程中很常见。时间变化和环境刺激会导致皮肤中衰老细胞积累,随着年龄的增长,皮肤功能下降。缩写:ECM,细胞外基质;UVR,紫外线辐射。 框2. 细胞衰老的一般特征 细胞衰老最早由Hayflick和Moorhead在20世纪60年代提出,他们观察到体外培养的细胞在经过一定次数的复制后会停止增殖。作者描述了一种当前被认为与端粒损耗有关的复制性衰老现象。 细胞衰老的特征是细胞具有稳定的周期阻滞。肿瘤抑制途径p53/21或p16/pRB中任意一种被激活均会导致细胞周期阻滞。有丝分裂信号和基因组或表观基因组应激均可激活这些通路。p16是细胞周期蛋白依赖性激酶CDK4和CDK6的抑制剂(CDKIs),而肿瘤抑制蛋白p53通过直接诱导p21的反式激活来介导细胞周期阻滞。细胞周期抑制剂p21反过来又抑制CDK2。CDKIs能够磷酸化视网膜母细胞瘤(RB)家族,该家族抑制E2F家族转录因子的活性。而E2F是细胞周期进展所必需的,抑制E2F导致了衰老细胞的永久细胞周期阻滞特征。E2F抑制与典型的衰老细胞染色质重组有关,称为“衰老相关异染色质病灶”(SAHFs)。 衰老细胞表现出多种标志,即:端粒和线粒体功能障碍;永久性DNA损伤反应;SAHFs的形成,负责沉默促增殖基因;形态变大;凋亡抵抗(BCL-2上调);代谢改变等。 衰老细胞保持代谢活性,并通过分泌SASPs影响其环境,包括免疫调节剂(炎症因子和趋化因子)、细胞外囊泡EVs、降解细胞外基质的酶(基质金属蛋白,MMPs)和生长因子。SASP基因在衰老过程中上调,其主要调控因子为NF-κB和C/EBP β。然而,其他如miRNAs或雷帕霉素受体(mTOR)通路也在SASP的调控中发挥作用。 SASP具有激活免疫应答或伤口愈合等相关功能。它主要以旁分泌的方式诱导周围细胞衰老,并导致持续的慢性炎症(称为炎性衰老),导致组织功能障碍以及出现衰老表型。 此外,还有其他几种药物可以促进细胞衰老,如下表所示。 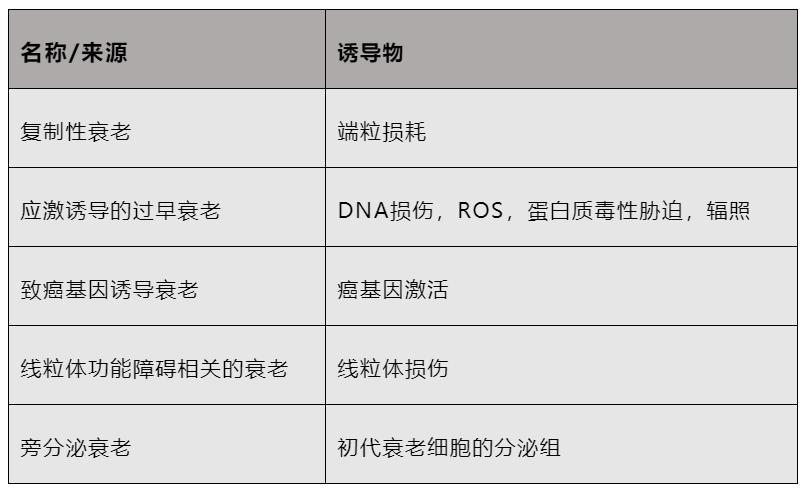 衰老最初是为了保护皮肤免受损伤,然而皮肤衰老细胞随着衰老而积累,所伴随的SASP通过一个称为旁分泌衰老的过程诱导相邻细胞衰老,进一步引发了组织功能障碍。有证据表明,皮肤老化反映并预测了其他器官与年龄相关的功能障碍(在下文中讨论),这表明皮肤老化能够加速其他组织的老化。研究发现,本质上老化的真皮成纤维细胞分泌组含有一种独特的蛋白质,称为“皮肤老化相关分泌蛋白”,即SAASP,与经典的SASP不同。SAASP与染色质改变增强衰老(DNA-SCARS)的DNA片段的存在有关,后者对应于p53结合蛋白1和早幼粒细胞白血病蛋白1阳性病灶。与传统SASP类似,SAASP富含基质金属蛋白酶(MMPs)和促炎介质。然而,SAASP蛋白表现了不同于SASP的独特分泌蛋白质模式,并突出了皮肤衰老过程的独特性。 外源性皮肤老化与生活方式和暴露于促进衰老的环境因素相关,如紫外线辐射、污染、压力、烟草烟雾等。 光老化是指紫外线诱导的皮肤老化,这是研究最多的外在皮肤老化形式。除了因诱发皮肤功能障碍(如晒伤或其致癌特性)而闻名外,紫外线提供的能量一直是地球生命和进化的基础。紫外线辐射的有益作用之一是在皮肤中产生维生素D3(框3)。 UVR光谱由UVA(320-400纳米)、UVB(280-320纳米)和UVC(100-280纳米)组成,是一种强环境氧化剂,也是导致大多数皮肤损伤和衰老的诱变剂。事实上,80%的可见皮肤老化迹象与紫外线照射相关。大多数UVC被臭氧层吸收,而UVB和UVA射线分别穿透皮肤的表皮层或表皮层和真皮层。 UVB是太阳能的一小部分,与UVA相比,其穿透能力更弱,但可引发更多的生物效应。生物体的发色团包括吸收紫外线的分子,如芳香族氨基酸、DNA、不饱和脂质等。事实上,与UVA相比,UVB优先被发色团吸收,并引起发色团结构改变,进而引发UVA或其他分子之间的化学相互作用,发挥生物功能。例如,DNA对UVB的吸收形成了嘧啶二聚体。这些紫外线诱导的光产物会引起突变并引发皮肤癌。 相比之下,通过促进氧化损伤,UVA辐射通过增加ROS水平间接引起DNA损伤。从结构上看,光老化的皮肤较厚,有很深的皱纹和异常的色素沉着斑点。紫外线照射增加了基质金属蛋白酶的表达,因此,光损伤的皮肤通常与真皮结缔组织的改变有关,包括异常弹性纤维的积累(称为“日光弹性症”)以及胶原纤维的组织紊乱和断裂。基质金属蛋白酶降解ECM会导致皮肤起皱,这是皮肤老化的主要标志。此外,长期暴露在紫外线照射下会引发皮肤细胞的衰老。 皮肤衰老的标志物 皮肤衰老细胞表现出典型的细胞衰老标志(框2)。SA-β-半乳糖苷酶在皮肤细胞中的表达早在体外和体内都被发现。该标记物是使用最广泛的衰老细胞标记物之一。然而,它不仅在固定的组织样本中失去了活性,由于它在非衰老细胞中的活性已有报道,因此该技术也缺乏特异性。此外,细胞周期抑制因子上调、染色质重组、DNA损伤和端粒损伤灶也是衰老皮肤细胞中的生物标志物。 皮肤老化的另一个标志是线粒体DNA(mtDNA)中4977个碱基对的缺失,这被称为“常见缺失”。该突变被认为是由UVA诱导的氧化应激损伤引起的。因此,尽管存在于防晒组织中,但这种突变在皮肤中的存在与紫外线照射有关。此外,mtDNA缺失数量与个体年龄相关。 皮肤衰老也可以通过核纤层蛋白Lamin B1表达的减少来检测,该蛋白属于核纤层蛋白家族,与Lamin A和C一起构成核纤层。这种缺失发生在体外和体内以及两种类型的衰老中。 细胞衰老对皮肤衰老的影响 越来越多的证据表明,衰老细胞的积累会导致皮肤老化。老年供体皮肤黑素细胞p16表达增加,这些细胞的衰老表型主要是通过长度无关的端粒损伤获得的。此外,黑素细胞端粒损伤病灶与年龄相关的皮肤特征呈正相关,如表皮-真皮交界处(EDJ)变平。此外,作者还发现SASP以旁分泌的方式诱导衰老黑色素细胞端粒功能障碍,并通过线粒体ROS损害角质形成细胞的增殖能力;使用抗衰老药物(ABT737)清除这些衰老的黑素细胞可以抑制这种效应。之前的一项研究强调,使用相同的延缓衰老药物清除表皮上的衰老细胞会增加毛囊干细胞的增殖。衰老生物标志物p16不仅在体内表皮和真皮室中随年龄增长而增加,而且与弹性纤维形态缺陷、皮肤皱纹增加和感知年龄相关。总之,这些数据表明,皮肤中的衰老细胞会进一步对表皮细胞增殖能力、毛发生长等产生不良影响,并可能加剧其他皮肤衰老特征的发生。 衰老细胞在皮肤中的过度积累导致通过SASP抑制巨噬细胞依赖的清除功能,从而导致衰老细胞在皮肤中的积累增加,导致皮肤老化。 SASP的细胞间通讯形式不仅包括可溶性因子,还包括EVs。研究表明,与早代成纤维细胞相比,衰老的真皮成纤维细胞分泌更多EVs,这反过来减弱了真皮对角质形成细胞分化和屏障功能的影响,并增加了促炎细胞因子IL-6的分泌。这说明在老化和相关病理中SASP的细胞间通讯作用,不仅通过可溶性因子,而且通过EVs进行。 另一项研究表明,在胶原基质中增加应激诱导的早衰成纤维细胞构建的人类器官型皮肤培养模型呈现出皮肤老化的特征,包括表皮厚度减少、增殖受损、屏障效应缺陷和表面性质改变。所有这些数据都表明衰老的皮肤细胞会促进皮肤衰老。 框3. 褪黑素和维生素D作为皮肤光保护剂和抗衰老分子 褪黑素,也称为“黑暗激素”,是松果体唯一已知的激素产物。这种激素在夜幕降临时释放,通过与下丘脑视交叉上核相互作用,发挥其众所周知的促进睡眠功能,并同步昼夜节律。此外,褪黑素还具有多种功能,包括对皮肤产生影响。皮肤含有这一途径中酶促成分的元素,可以直接合成褪黑素。褪黑素还具有对皮肤光的保护作用。在紫外线照射前,用褪黑素孵育HaCaT细胞,可以减少细胞凋亡,特别是通过维持线粒体膜电位和抑制caspases 9、3和7的激活,来促进细胞活力。褪黑素的抗氧化和自由基清除特性支持了这种保护作用。据报道,褪黑素可保护DNA免受损伤,并防止紫外线介导的抗氧化酶(过氧化氢酶、超氧化物歧化酶和谷胱甘肽过氧化物酶)防御的减少。此外,一些研究表明褪黑素在皮肤进程中还有其他重要作用,包括通过增加角质形成细胞增殖和表皮大分子(如总苞素、角蛋白-10和14)的表达来调节屏障功能,减少皮肤黑素生成,体温调节等。这种保护作用是由抗氧化和清除自由基的褪黑素支持的。据报道,褪黑激素可以保护DNA免受损伤,并防止紫外线介导的抗氧化酶防御(过氧化氢酶、超氧化物歧化酶和谷胱甘肽过氧化物酶)的减少。此外,一些研究表明褪黑素在皮肤其他生理过程中具有其他重要作用,包括通过增加角质形成细胞增殖和表皮大分子(如内披蛋白involucrin、角蛋白-10和14)的表达来调节屏障功能,减少皮肤黑色素生成,体温调节等。 维生素D是在皮肤暴露于UVB时产生的。UVB直接光解7-脱氢胆固醇导致维生素前体D3的产生。这进一步转化为三种光异构体:维生素D3、速甾醇和光甾醇(L3)。 维生素D3转化为其活性形式25-羟基维生素D3 [25(OH)D3],然后转化为1,25(OH)2D3/骨化三醇。维生素D活性代谢物1,25(OH)2D3和维生素D受体(VDR)在皮肤中的激活改善了终端分化和表皮屏障效应(增加了蛋白分子如involucrin,兜甲蛋白loricrin和聚丝蛋白的表达),并降低了角化细胞增殖,具有肿瘤抑制活性。此外,CYP11A1 L3催化的产物L3-羟基化物也可以与VDRs和肝X受体(LXRs)相互作用。LXRs具有重要的功能,如调节脂质/甾醇稳态,表明L3化合物具有更广泛的作用机制和生物学功能。羟基甾醇也被报道通过诱导自由基清除,防止DNA损伤,发挥抗炎活性(抑制NF-κB,从而抑制炎症细胞因子的表达)和促进UVB照射下角质形成细胞的表皮分化来介导光保护作用。 这些数据表明,褪黑素和维生素D衍生物都是强力的光保护剂,可能是有希望促进皮肤内环境稳定和防止环境应激源(如UVR)损害、延缓皮肤衰老的策略。 皮肤衰老对全身衰老的影响 有证据表明,皮肤衰老会将衰老表型传递到其他组织或器官(图2)。而且不同的研究表明,皮肤反映了机体的健康状况、死亡风险和寿命。事实上,对防晒区域的皮肤皱纹和面部外观是否与家族寿命、疾病风险和死亡率相关的研究表明,防晒区域皮肤皱纹的减少与寿命显著相关,而且女性的认知年龄、生存率和心血管疾病风险之间存在显著的关联。此外,皮肤衰老还与机体衰老有关。皮肤中p16阳性细胞的出现频率与CD4+ T细胞免疫衰老标志物和生物年龄呈正相关。研究人员发现,皮肤微生物群能够准确预测时序年龄。不过这些研究是基于相关性的,而这些相关性背后的机制尚未得到准确回答(见悬而未决的问题)。 悬而未决的问题 衰老的皮肤细胞是否会引发其他组织或器官的衰老相关功能障碍? 皮肤衰老会通过下丘脑促进全身衰老吗? 皮肤衰老是否会损害HPA轴? 局部应用抗衰老药物是预防或延缓衰老的有效策略吗? 皮肤对环境刺激很敏感,会引起一定程度上的局部反应,分泌激素、神经肽、神经递质及其相应的受体。这是由皮肤神经内分泌系统介导的:皮肤局部表达下丘脑-垂体-肾上腺(HPA)轴的元素,特别是促肾上腺皮质激素释放激素(CRH)系统、原皮质黑素皮质激素(POMC),以及参与类固醇生成酶机制(框1)。下丘脑是一个在系统衰老中起关键作用的大脑区域(框 4),而中央HPA轴的激活会增加下丘脑中CRH的产生和释放。有趣的是,UVR根据波长/剂量激活HPA系统,这些效应对UVC和UVB的反应比对UVA更明显。因此,UVB照射小鼠皮肤后,不仅提高了脑和血浆中几种神经肽(CRH、尿皮质激素、ACTH和β-内啡肽)以及皮质酮(CORT)的水平,而且还促进了免疫抑制。UVR也能刺激皮肤产生类固醇。此外,UVB和UVC比UVA增加了11β-羟甾体脱氢酶(一种调节皮质醇可用性的酶)和皮质醇的产生,同时降低了体外人皮肤中表皮糖皮质激素受体的表达。 另一项研究表明,小鼠皮肤中的UVR会导致影响海马体的应激反应,损害神经发生,降低突触蛋白表达,这表明皮肤通过CORT与海马体进行交流。皮肤HPA增加了UVR暴露后的皮质酮水平,触发海马体的应激改变。此外,皮肤中的慢性UVR促进了小鼠的抑郁行为,这表明皮肤影响了大脑功能。根据这些数据,作者得到一个假设,由于皮肤和大脑之间的密切联系,皮肤衰老(主要通过其相关的分泌体)会导致海马和下丘脑功能障碍,并导致机体功能下降,从而导致衰老。然而,皮肤衰老对下丘脑功能的影响尚未得到完全阐明。 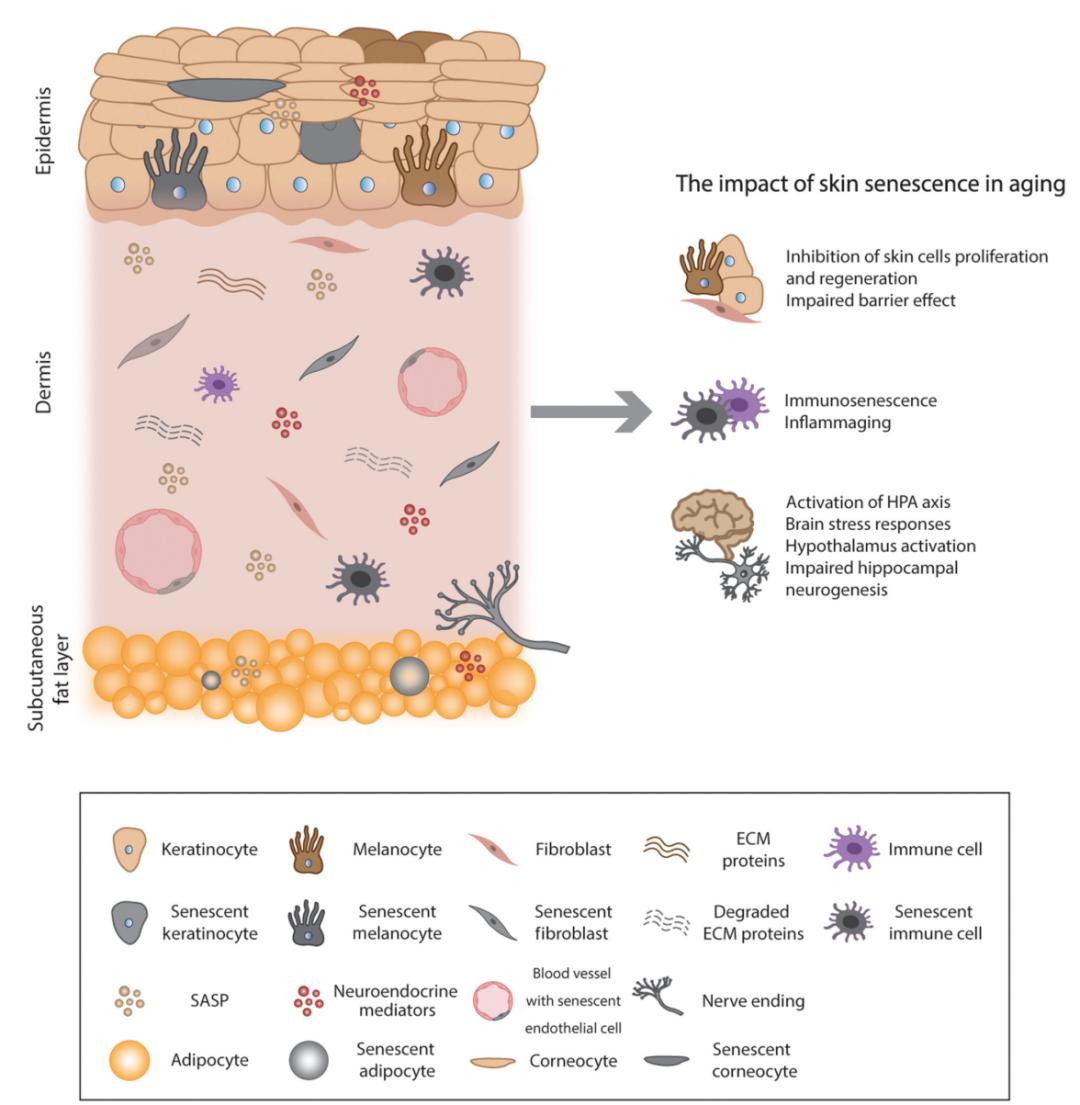 图2. 皮肤衰老在全身衰老中的作用。由于暴露于环境因素中,随着衰老的发生,皮肤中会出现衰老细胞。这些细胞(灰色部分)表现出稳定的细胞周期阻滞和衰老相关分泌表型(SASP)的分泌,其中包括细胞因子和基质金属蛋白酶。SASP诱导功能障碍,并将衰老传递到附近的细胞,这些细胞可以是皮肤细胞或其他类型的细胞,如免疫细胞、内皮细胞或神经细胞。此外,皮肤具有皮肤神经内分泌系统,可被环境或内源性应激源激活并产生神经内分泌介质。这种皮肤内不同细胞和分子之间的相互作用会导致衰老:皮肤衰老细胞会导致皮肤功能下降,包括再生和增殖能力;衰老表型可能导致免疫衰老和慢性低度炎症状态;此外,由于通过下丘脑-垂体-肾上腺轴维持沟通,皮肤应激可促进大脑应激反应和功能障碍。缩写:DEJ,真皮-表皮交界处;ECM,细胞外基质。 框4. 下丘脑是机体衰老的调节器 下丘脑是一个大脑区域,负责调节最基本的维持生命的功能,如新陈代谢、发育、睡眠、食物摄入、生长和生殖。此外,它通过整合来自外周环境、激素、代谢和神经信号来维持机体内稳态。 下丘脑还通过促生长轴 [生长激素释放激素(GHRH)、生长激素(GH)和胰岛素样生长因子-1(IGF-1)] 参与寿命调节,它们随着年龄的增长而下降,这个过程被称为“生长激素分泌停滞”。许多哺乳动物的生长激素水平下降都与年龄有关,这主要是由于下丘脑GHRH水平的降低导致的。 事实上,近年来,下丘脑已成为系统衰老的关键研究区域,但其机制仍未完全阐明。一项关于下丘脑在小鼠系统性衰老中的作用的关键研究表明,下丘脑免疫由IκB激酶-β(IKK-β)、NF-κB和相关小胶质-神经元免疫交流抑制促性腺激素释放激素(GnRH),触发与衰老相关的下丘脑GnRH下降。此外,使用脑特异性IKK-β敲除模型,作者观察到老年小鼠皮肤萎缩的改善,支持了皮肤和下丘脑之间的交流。作者提出免疫抑制或GnRH治疗是延缓衰老的潜在策略。 最近,也有研究表明,下丘脑干细胞丢失是小鼠模型衰老的一个原因之一。在表达衰老样下丘脑干细胞的小鼠模型中(通过SOX2和BMI1沉默),加速了与年龄相关的改变,寿命被缩短。这些下丘脑干细胞向脑脊液释放外泌体miRNAs,其水平随着年龄的增长而下降。这些数据表明,下丘脑干细胞中的一种衰老样表型通过释放外泌体miRNAs促进衰老。 新出现的证据支持了远距离器官之间存在通信轴的观点,如肠-脑轴或皮肤-脑轴。脑-皮肤回路由神经免疫内分泌因子介导,是许多过敏和炎症性皮肤病理的基础。例如,有报道称心理应激通过抑制皮肤屏障功能、毛发生长和表皮朗格汉斯细胞频率来促进皮肤功能障碍的发生。因此,这种脑-皮肤交流可能支持皮肤损伤导致衰老过程中下丘脑功能障碍的假说。 临床医生角 皮肤老化是一项健康挑战,不仅因为它的美学意义,如皱纹的出现、老年斑、弹性丧失等,而且还因为它的功能丧失和皮肤癌风险增加。 目前对抗皮肤衰老的方法是基于局部化妆品的使用,包括防晒霜和类维甲酸或白藜芦醇等成分。然而,这些产品及其对皮肤衰老的功效之间的关系尚未完全了解。 局部应用抗衰老药物可能是一种潜在的抗衰老方法,因为这些化合物具有抗炎和促黑素生成的特性,有助于保护皮肤、防止癌变、延缓衰老和减少年龄相关疾病。 在将这些药物应用于皮肤科临床实践之前,局部外用延缓衰老药物的安全性和有效性需要由临床试验来验证。 通过使用局部抗衰老药物来去除皮肤衰老细胞是否可以延缓全身衰老? 应对衰老的紧急策略包括使用抗衰老药物来消除衰老细胞。抗衰老药物达沙替尼( Dasatinib,D)和槲皮素(Quercetin,Q)可有效诱导衰老细胞的凋亡。D是多种酪氨酸激酶的抑制剂,用于治疗癌症,而Q是一种靶向BCL-2/ BCL-XL,PI3K/ AKT,p53/ p21/ 血清SCAPs的黄酮类化合物。最近的一项研究表明,移植少量的衰老细胞就足以在正常宿主细胞中诱导衰老标记物的表达,并引起幼鼠持续的生理功能障碍。而使用D+Q能减轻小鼠的生理功能障碍,增加存活率。 联合药物D+Q正在进行一项II期临床随机临床试验(NCT02848131),针对糖尿病肾病患者,通过邀请招募。该研究的主要结果是衰老细胞负荷的改变。在I期结束时,脂肪组织、皮肤活检和SASP血浆中的衰老标志物水平显著下降。统计分析包括数据计数、百分比、平均值和定量数据的标准差。无严重不良事件的报道。此外,作者声称,由于其特异性最高,这种药物组合在针对慢性疾病的细胞衰老方面是最有益的。事实上,其他靶向BCL-2途径的抗衰老药物,如Bcl-2抑制剂(navitoclax,ABT-263)或非瑟酮(Fisetin,一种低毒的天然黄酮类化合物),也被发现在部分衰老细胞中具有抗衰老作用。非瑟酮和D已被局部应用于小鼠皮肤,发现可以减少紫外线诱导的炎症并增加皮肤中的黑色素生成。 同类药物,如二甲双胍和雷帕霉素,通过抑制SASP靶向衰老细胞。二甲双胍(Metformin)是一种降糖药物,它被证明可以缓解几种与年龄相关的疾病,并增加人类的生存率。雷帕霉素(Rapamycin)及其类似物(抑制雷帕霉素受体),是美国食品药品监督管理局(FDA)已批准的多种治疗方法之一,并被发现也可改善人体免疫衰老。此外,有报道称它们可以延缓小鼠衰老并延长寿命。二甲双胍和雷帕霉素都已被局部应用于人体皮肤。雷帕霉素显著降低了p16水平,增加了胶原蛋白VII的水平,对可见的皮肤结构有整体改善。这些研究大多是使用暴露在人工光源下的细胞或啮齿类动物模型进行的。因此,目前还需要更多的人体研究来更好地阐明这些化合物对皮肤衰老的功效。另外,将这些疗法转化为针对皮肤衰老及其对机体衰老的潜在影响,可能有助于开发新的有效的抗衰老疗法(见临床医生角和悬而未决的问题)。 结束语 鉴于皮肤所处的位置,它会永久地被暴露在环境因素下。通过神经内分泌系统,皮肤感知来自环境的信号和协调适当的反应在维持机体内稳态中起着关键作用。 皮肤衰老是随着年龄增长或暴露于环境攻击物(如紫外线辐射)而发生的,并可以通过SASP将衰老表型从皮肤传递到其他组织和器官,从而影响全身衰老。因此,作者假设,由于皮肤永久地受到促衰老因子的影响,并在这个过程中一直与包括大脑在内的其他几个器官保持密切交流,因此皮肤的衰老可能会促进其他组织或器官中与年龄相关的功能障碍。作者认为,通过抗衰老药物或衰老治疗药物的局部给药,可能有助于开发新的抗衰老策略,并延缓全身衰老和年龄相关疾病的发生。不过目前人们还需要更广泛的研究来更好地阐明皮肤衰老在全身衰老中的作用。  原标题:《【重磅综述】皮肤衰老的机制和对全身衰老的影响》 阅读原文 |
【本文地址】