探索高压下过渡金属的氟化极限 |
您所在的位置:网站首页 › c的电负性和h的电负性 › 探索高压下过渡金属的氟化极限 |
探索高压下过渡金属的氟化极限
|
探索高压下过渡金属的氟化极限
氧化态反映元素在化合物中的成键方式及其在化学反应过程中的电子得失情况,因而与材料的物理和化学性质密切相关。因此,探索新氧化态的形成机制及由此构造具有特殊性质的新材料是化学和凝聚态物理的重要研究课题之一。由于氟极强的得电子能力,有利于元素在氟化物中呈现出高的氧化态。因此,探索富氟组分化合物成为认识元素化学属性极限的有效方法。 富氟组分过渡金属氟化物具有强氧化性,在新材料制备方面有重要应用价值。压力作为一种基本热力参量,在诱导结构相变获取新材料和稳定非常规组分化合物方面有独特优势。东北师范大学杨国春教授(点击查看介绍)课题组在高压富氟组分过渡金属氟化物探索方面进行了努力与尝试,基于第一性原理结构预测方法,发现了热力学稳定的 AuF4和AuF6分子晶体,既弥补了Au空缺的+4氧化态,并将Au的正氧化态延伸至+6 (J. Am. Chem. Soc., 2018, 140, 9545);压力诱导稳定的IrF8分子晶体,成为首例中性过渡金属八氟化物,Ir首次在体相中呈现+8氧化态,计算表明IrF8具有极强的氧化能力 (J. Am. Chem. Soc., 2019, 141, 5409)。 鉴于过渡金属元素多样的d 电子构型和前期工作所发现的压力诱导的富氟组分化合物,非常有必要探索高压下过渡金属的氟化极限及其稳定机理。过渡金属能够提供更多价电子是获得富氟组分化合物必要前提。杨国春教授课题组以14种具有6个以上价电子的第五、六周期过渡金属元素 (第四周期元素由于原子半径较小被排除) 为对象,探索高压下过渡金属的氟化极限。
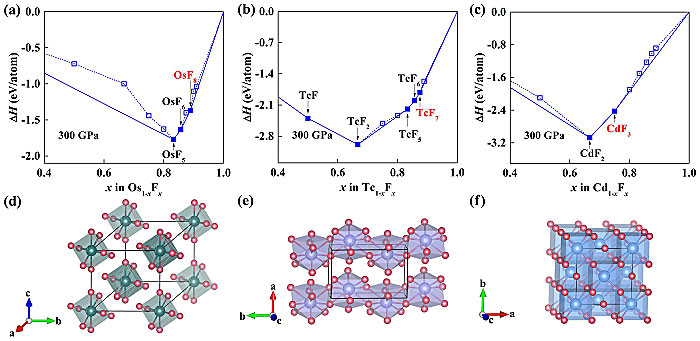
图1. (a) Os-F、(b) Tc-F和(c) Cd-F体系在300 GPa下的热力学稳定性及发现的富氟组分(d) OsF8、(e) TcF7、(f) CdF3的结构。绿、紫、蓝、红球分别代表Os、Tc、Cd和F原子。图片来源:Angew. Chem. Int. Ed. 基于CALYPSO结构预测方法,作者研究了14种过渡金属元素 (Mo、Tc、Ru、Rh、Pd、Ag、Cd、W、Re、Os、Ir、Pt、Au和Hg) 和F2在300 GPa下的化学反应,确定了不同组分间的相对热力学稳定性 (图1)。除前期工作所得富氟化合物,在其他过渡金属中也发现了更富氟组分化合物:OsF8、TcF7和CdF3。首次实现Os和Tc在氟化物中价电子完全用于成键。其中,300 GPa下的TcF7和CdF3分别与同族的ReF7和HgF3的高压相同构。OsF8为典型的分子相,与IrF8的高压相都展现出罕见的立方配位构型。
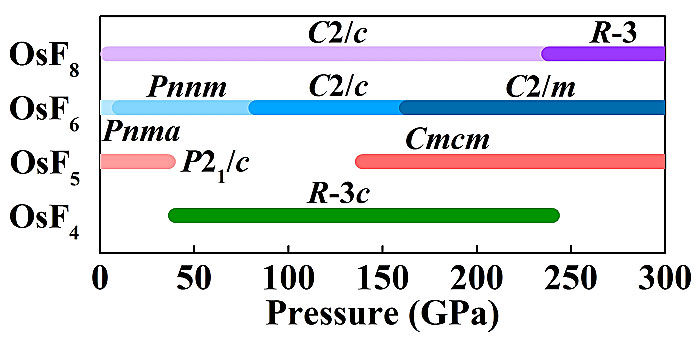
图2. Os-F化合物在0 ~ 300 GPa压力范围内的压力-组分关系相图。图片来源:Angew. Chem. Int. Ed. 作者研究了Os-F体系在0 ~ 300 GPa范围内的压力-组分相图 (图2)。OsF5在环境条件下以P21/c相存在 (图3a)。随着压力的增加,OsF5将在36 GPa时分解,并在139 GPa时以Cmcm相再次稳定 (图3b)。常压不稳定的OsF4在~40 GPa稳定于空间群为R-3c的三角结构 (图3c),并在240 GPa时分解为单质Os和OsF5。在常压下,OsF6以Pnma分子相存在 (图3d),在10 GPa时相变为另一空间群为Pnnm的分子相 (图3e)。进一步压缩 (~80 GPa),其相变为C2/c (图3f),完全失去其分子晶体特性,随后在~160 GPa左右再次相变为C2/m结构 (图3g)。相比于IrF8的稳定压力39 GPa,OsF8在~4 GPa压力下即可稳定于单斜结构C2/c相 (图3h),具有明显的分子相特征。在240 GPa时相变为前文所述的R-3相 (图1d)。值得注意的是,配位数为8的过渡金属配合物在常压下通常呈现四方反棱柱配位构型。而这4种Os-F化合物的高压相 (即R-3c OsF4、Cmcm OsF5、C2/m OsF6和R-3 OsF8) 都以准立方八配位构型作为基本结构单元。随着F含量的增加,立方单元的连接方式从顶点共享 (OsF4) 到边共享 (OsF5和OsF6),最后变为准分子相 (OsF8)。
图3. 晶体结构图:(a) 1 atm下P21/c OsF5,(b) 200 GPa下Cmcm OsF5,(c) 200 GPa下R-3c OsF4,(d) 1 atm下Pnma OsF6,(e) 50 GPa下Pnnm OsF6,(f) 100 GPa下C2/c OsF6,(g) 200 GPa下C2/m OsF6和(h) 50 GPa下C2/c OsF8。绿球代表Os原子,红球代表F原子。图片来源:Angew. Chem. Int. Ed. 为什么常压下难以得到1:8化学计量比的过渡金属氟化物?它们又为什么能在高压下稳定存在?压力不仅可以调控元素电负性,而且能诱导原子轨道能级发生变化,但压力对不同原子的调控程度有所不同。元素的电负性越低则越容易失去电子。如图4所示,所研究过渡金属的电负性随着压力的增加都有较大幅度的降低,而氟的电负性只是略有降低。另外,在化学反应中,电子容易从高能级轨道转移到低能级轨道。随着压力升高,相对于F 2p轨道能级,Ir和Os的5d 能级显著提升,导致元素间能级差逐渐增大。因此,从原子角度讲,Ir和Os在高压下更容易被氟夺取电子而形成高价化合物。但在实际化学反应中,电荷转移程度与物质结构密切相关。
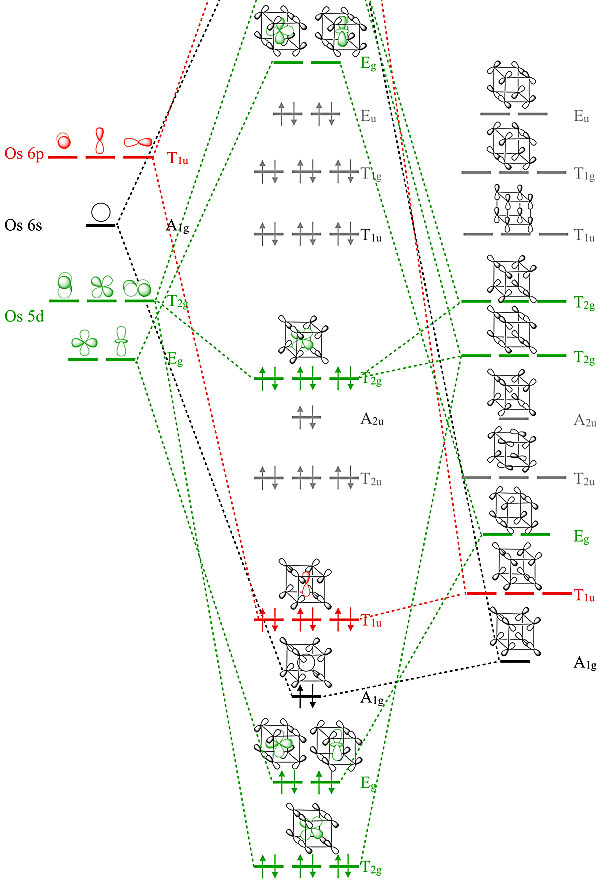
图4. 14种过渡金属和氟的电负性随压力的变化情况(单位eV e-1,6 eV e-1约等于1鲍林电负性标度)。图片来源:Angew. Chem. Int. Ed. 根据配位场理论,在八配位立方体配位场中,过渡金属的d电子能级将分裂为3条能量较高的T2g轨道和2条能量较低的Eg轨道。为了探究过渡金属电子与配体之间相互作用及电荷转移,作者计算了OsF8立方构型的中Os的价轨道与周围立方配体场的相互作用 (图5)。除了Os 5d电子与立方F8配体相互作用形成化学键外 (Os 5d → F 2p电荷转移),原本未占据的Os 6p轨道能级在压力和配体场共同作用下发生下移,与F8中次低的T1u配体轨道相互作用,发生配体到金属的电荷转移 (F 2p → Os 6p)。因此,立方构型中Os-F键共价性得到增强,使Os-F化合物在高压下倾向于立方配位构型。在OsF8中,Os和F的价电子已将成键轨道完全填满,最高占据轨道是Eu。如果再添加一个价电子,它将占据Os-F反键轨道Eg。Ir 比Os多一个价电子,其八氟化物的稳定性会弱于OsF8,需要在更高的压力 (~39 GPa)才能稳定存在,而OsF8的稳定压力为~4 GPa。Pt和Au有更多价电子,将占据能量更高的反键轨道,提升体系焓,从而不可能稳定存在。
图5. 分子轨道图:Os 5d、6s、6p与F 2p之间的相互作用。图片来源:Angew. Chem. Int. Ed. 氟化是公认挑战化学极限的方法。杨国春教授课题组探索高压下过渡金属的氟化极限,表明压力能够将常规条件下的氟化极限进一步延展:不仅发现了更富氟组分化合物,而且稳定化合物展现出独特的几何结构;诱发了不同寻常的电荷转移,中心金属原子既是超价的也是超配位的。希望这些研究激发实验工作者合成富氟组分过渡金属氟化物。相关研究成果发表在Angew. Chem. Int. Ed.,并被遴选为“热点论文”。课题组博士研究生蔺健妍为第一作者,瑞典查尔姆斯理工大学Martin Rahm教授和东北师范大学杨国春教授为共同通讯作者。 原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):
Exploring the Limits of Transition-Metal Fluorination at High Pressures Jianyan Lin, Xin Du, Martin Rahm, Hong Yu, Haiyang Xu, Guochun Yang Angew. Chem. Int. Ed., 2020, DOI: 10.1002/anie.202002339 杨国春教授课题组简介
杨国春教授课题组依托东北师范大学紫外光发射材料与技术教育部重点实验室。近五年,课题组基于第一性原理结构预测方法开展研究,取得系列创新性研究成果,发表SCI论文40余篇,包括Phys. Rev. Lett. (2篇),J. Am. Chem. Soc. (5篇),Angew. Chem. Int. Ed. (1篇)。1篇入选ESI高被引论文,应邀撰写综述论文3篇。研究成果获得同行和媒体的一致好评和广泛关注,如被《物理评论快报》遴选为 “Editors’ Suggestion”,美国《超导周报》专题报道,美国物理门户网站新闻报道,被《Angewandte Chemie》遴选为“Hot Paper”,《Nature Review Chemistry》专题报道,《Advanced Science News》新闻报道和《Chemistry World》亮点报道等。 欢迎对课题组研究方向感兴趣的有志青年学生加入!联系方式:[email protected] https://www.x-mol.com/university/faculty/77535 科研思路分析 Q:这项研究最初是什么目的?或者说想法是怎么产生的? A:如上所述,在富氟组分过渡金属化合物中,中心金属通常可表现出极高的氧化态。前期工作中,我们发现了几种过渡金属元素(Au、Ag、Cu、Ir)可以在压力的调控下进一步氟化,形成环境条件下无法形成的化学计量比。本工作试图从全局角度探究过渡金属富氟组分化合物所能达到的极限,并进一步分析了富氟组分化合物在高压下的稳定机制,为今后实验的最终合成提供理论依据。 Q:该研究成果有哪些重要意义? A:富氟组分的探索是挑战化学极限的一种有效方法,无论是在晶体结构方面还是电子性质方面。本研究探索了高压条件下过渡金属氟化物所能达到的最高氟化学计量,并对能够形成八氟化物的Os-F体系相图及化合物结构进行了深入研究。从配位场理论和压力诱导原子轨道能级及电负性变化角度探究了富氟化合物的稳定机理,研究结果表明,OsF8及IrF8两种过渡金属八氟化物不仅是超配位的,而且是超价态化合物。此研究工作拓宽了人们对经典化学的理解,为发展高压化学理论提供原型和知识储备。 如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载! 点击分享 收藏 取消收藏 评论: 0 |
【本文地址】