快讯 |
您所在的位置:网站首页 › bimekizumab单抗中文名 › 快讯 |
快讯
|
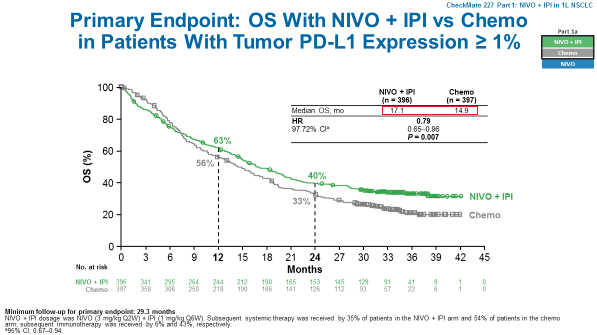
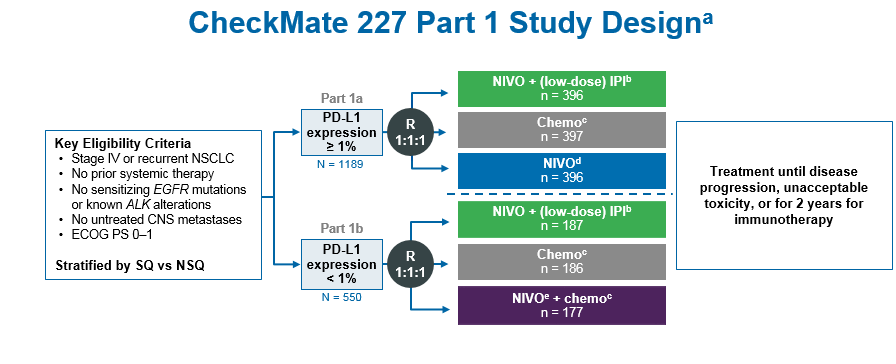
FDA同时批准了PD-L1 IHC 28-8pharmDx伴随诊断适合接受双重免疫治疗的患者。 “患有转移性肺癌的患者仍然需要新治疗方案,以产生持久缓解,”纪念斯隆-凯特琳癌症中心癌症中心的医学肿瘤学家兼CheckMate-227试验研究员Matthew D. Hellmann博士在新闻稿中表示。“ CheckMate-227试验的结果表明,双重免疫疗法为合适的转移性NSCLC患者提供了更长的生存期。” 在一项多重,开放标签的3期CheckMate-227试验中,研究人员评估了非鳞状和鳞状晚期NSCLC患者接受一线nivolumab/ipilimumab方案与含铂化疗方案的疗效对比。 第1a部分:肿瘤PD-L1表达的患者使用nivolumab/低剂量ipilimumab或单药nivolumab与化疗比较 第1b部分: 肿瘤PD-L1不表达的患者使用nivolumab/低剂量ipilimumab联合化疗或nivolumab联合化疗与化疗比较 第2部分:nivolumab联合化疗与化疗相比,无论PD-L1表达或肿瘤突变负荷状态(TMB)在1a部分,将1189例患者按1:1:1的比例随机分配接受化疗(n = 397),单药nivolumab(n = 396)和nivolumab/低剂量的ipilimumab(n = 396)。在1b部分,将550名患者随机分配接受nivolumab/低剂量ipilimumab(n = 187),化疗(n = 186)和nivolumab/化疗(n = 177)。
每2周以3mg/kg的剂量给予nivolumab,在联合治疗组中,每6周给予1mg/kg的ipilimumab。 直至疾病进展,出现不耐受的毒性或接受免疫治疗持续2年。 符合入组条件的患者必须患有IV期或复发性NSCLC,未接受过预先系统治疗,没有敏感EGFR突变或ALK变异,无未经治的中枢神经系统转移,ECOG表现状态为0或1。患者按鳞状和非鳞状组织分类。 Nivolumab/Ipilimumab与化疗对照共同的主要研究终点为PD-L1阳性(≥1%)人群的OS与高TMB人群的无进展生存期(PFS)。次要终点包括PD-L1 |
【本文地址】
今日新闻 |
推荐新闻 |