MPO |
您所在的位置:网站首页 › anti-mpo阳性 › MPO |
MPO
|
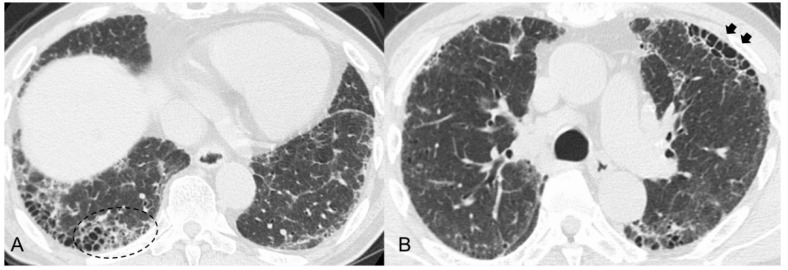
图1 HRCT扫描结果 A,HRCT显示蜂窝样和牵拉性支气管扩张周围的衰减增加(虚线圆圈);B, HRCT显示上叶前部蜂窝样病变,表现为上叶前部集中大量囊性空腔(黑色箭头)
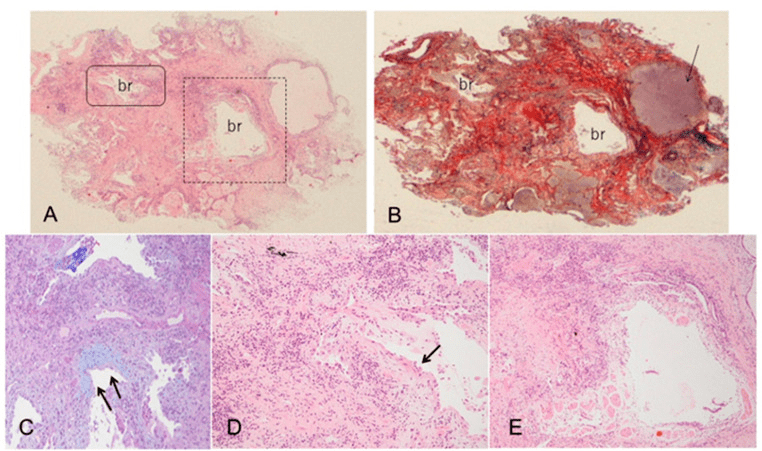
图2 MPO-ANCA阳性ILD病例的经支气管肺冷冻活检 A, 苏木精和伊红染色显示病变特征为支气管周围致密的肺泡纤维化并伴有结构破坏;B, Elastica van Gieson染色显示细支气管部分弹性层缺失,表现为毛细支气管炎和充满黏液的囊性气腔;C和D,放大A中实线长方形区域显示扩张的细支气管伴上皮下成纤维细胞灶(箭头),纤维化中有中度淋巴细胞和浆细胞浸润;E, 放大A中虚线正方形区域显示扩张的细支气管上皮细胞脱落、上皮下纤维化、淋巴细胞和浆细胞浸润 表1 MPO-ANCA阳性ILD和IPF的特征和HRCT/病理表现
预后和死亡原因 先前的队列研究报告MPA-ILD患者的中位生存时间为4.1~11年,5年生存率为46%~60%,但长期预后报道较少。MPO-ANCA阳性但无系统性血管炎表现的ILD是特发性ILD的一种形式,MPA-ILD与特发性ILD在生存时间和预后上是否存在差异,目前仍存争议。MPO-ANCA阳性ILD患者即使表现出UIP模式,其生存时间也很可能比UIP/IPF患者更长。报告的不良预后因素包括年龄较大、ANCA滴度较高、炎症标志物(如ESR、CRP)水平较高、用力肺活量降低和前上叶蜂窝状病变。 导致MPO-ANCA阳性ILD患者死亡的主要原因包括ILD急性加重(AE)(10%~25.5%)、慢性进行性纤维化(PF-ILD)(7.8%~19%)、感染性疾病(19.2%~20%)和弥漫性肺泡出血(DAH)(4.3%~30%)。需要注意的是,对于MPO-ANCA阳性特发性ILD患者,MPA进展最初可能表现为DAH,这是一种可危及生命的疾病。这些发现提示存在这四种主要死亡原因的情况下,临床医生应制定针对MPO-ANCA阳性ILD患者的治疗策略。 MPO-ANCA阳性ILD的治疗 (1)合并MPA的ILD患者 当诊断ILD合并MPA时,应根据血管炎的器官受累情况进行治疗,包括使用高效抗炎药物进行诱导治疗,如糖皮质激素、环磷酰胺、利妥昔单抗、霉酚酸酯和硫唑嘌呤。然而,没有研究表明治疗MPA本身对ILD是否也有效。 (2) 无系统性血管炎表现的MPO-ANCA阳性ILD患者 首先,当考虑为无系统性血管炎表现的MPO-ANCA阳性ILD时,临床医生应在HRCT上确定患者是否有UIP模式。对于NSIP或有组织肺炎的患者,应将其视为特发性ILD进而开始使用抗炎药物(主要是糖皮质激素)治疗。 其次,由于缺乏证据,对于存在UIP模式的MPO-ANCA阳性ILD的治疗评估是最困难且具有争议的。在考虑是否开始或切换治疗时,两个主要因素很重要,即ILD的炎性变化或纤维化变化。 支持炎症改变的一个因素是MPA样疾病的存在,如反复不明原因的发热和(或)较高的CRP/ESR和MPO-ANCA滴度的上升趋势。第二个因素是在HRCT上看到的纤维化改变周围的衰减增加和病理性肺病变中显著的炎性细胞浸润。对于前者,如果MPO-ANCA阳性特发性ILD患者发生MPA,则应进行抗炎治疗,因为未经治疗的MPA(尤其是伴有DAH的MPA)通常是进行性的、致命的。后者作为一种放射病理发现而言,即使存在UIP模式,抗炎是一种有效的治疗方案。 相反,促进纤维化改变的因素是CRP或ESR水平不升高,MPO-ANCA滴度降低或趋于稳定,纤维化改变在HRCT上呈网状扩张伴牵拉性支气管扩张和蜂窝状而不增加衰减,在没有明显炎性细胞的肺标本中,病理斑片状纤维化表现为UIP模式和/或成纤维细胞灶。需要注意的是,毛玻璃样阴影(GGO)通常与炎症或浸润相关,但并不总是代表可逆的肺部疾病,在某些情况下,它可能代表显微镜下的纤维化。因此,肺活检可能有助于评估炎症还是纤维化为主要病变。最近的报告显示,所有与ILD相关的病因都可能导致不良预后,尤其是在一些存在一定程度的UIP病例中。也就是说,部分病例代表了ILD由炎症性改变向纤维化性改变的自然演变。 Adegunsoye等人指出,蜂窝状表现为一种进行性纤维化性ILD表型,与结缔组织疾病、特发性ILD等基础疾病无关。此外,ILD的AE可以影响所有ILD患者,但在具有潜在UIP模式的患者中发生率更高,这是导致患者死亡的主要原因。纤维化改变的存在和(或)扩大,尤其是在UIP模式中,在随访期间发现网状伴牵拉性支气管扩张及蜂窝状,对所有与ILD相关的病因都有重要的预后意义。 如果确定纤维化占主导,则考虑开始抗纤维化治疗,目前尼达尼布或吡非尼酮已被批准用于治疗IPF。INBUILD研究显示尼达尼布对PF-ILD的疗效优于IPF,且有抑制ILD AE的潜力,事后分析表明,尼达尼布对所有PF-ILD亚组患者(包括自身免疫性ILD)都有治疗益处。在RELIEF研究中,虽然证据质量低,但显示吡非尼酮可显著抑制由结缔组织病相关ILD、纤维化NSIP、纤维化过敏性肺炎、进行性纤维化ILD患者用力肺活量的恶化。综上所述,UIP模式患者的纤维化改变扩大可导致PF-ILD和ILD AE的风险较高,这意味着MPO-ANCA阳性ILD的患者预后也较差。因此,在这种情况下应考虑开始抗纤维化治疗,例如尼达尼布。 此外,从不同的角度考虑治疗评估,抗炎治疗在某些情况下可能是有害的。已经强调了将IPF与特定全身性疾病(例如与结缔组织疾病相关的疾病)相关的ILD 区分开来的重要性。建议IPF患者不要进行抗炎治疗。最近的一份报告也显示,使用糖皮质激素的抗炎治疗在CTD-ILD中发生PF-ILD的风险更高。在RA-ILD中,泼尼松龙剂量高于10 mg与感染合并症风险较高相关。与老年MPA-ILD患者一样,大剂量糖皮质激素治疗是严重感染的重要危险因素,而严重感染是死亡的主要原因。一般来说,糖皮质激素会增加慢性肺部感染风险,如非结核分枝杆菌和肺曲霉病。由于肺气肿的存在也可能是ILD患者发生慢性肺部感染的危险因素,临床医生在考虑是否启动或加强抗炎治疗时,应在一定程度上关注合并肺气肿的ILD患者。 Kawamura等人报道,糖皮质激素的使用与ILD AE风险增加有关,即使在低剂量时也呈剂量依赖性。虽然不能肯定,但不完全的抗炎治疗可能会引起感染性疾病、ILD AE等不良事件,导致预后不良。综上,当难以在抗炎和抗纤维化治疗之间进行选择时,感染风险高、有ILD AE的患者,如启动或长期使用中、高剂量糖皮质激素并伴有一定程度的肺气肿者,应优先考虑抗纤维化治疗(图3)。前瞻性研究应明确MPA-ILD的自然史以及ANCA阳性在特发性ILD患者中的作用,为不同类型的特发性ILD患者提供更好的治疗方法。
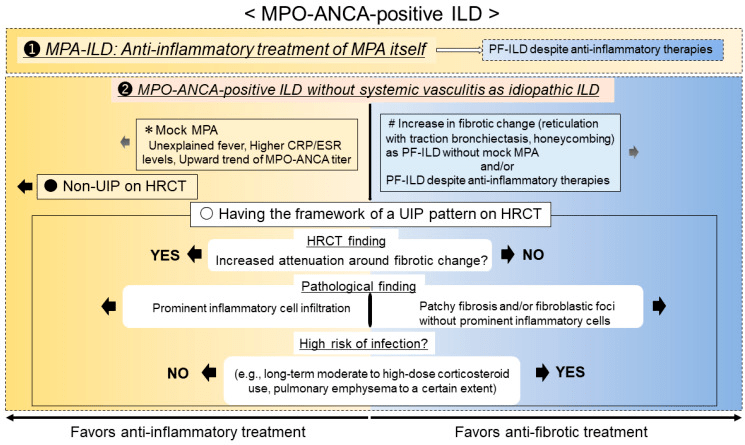
图3 MPO-ANCA阳性ILD的治疗方案 总结 在任何MPA-ILD或特发性ILD病例中,MPO-ANCA阳性ILD并不少见。一些在诊断时存在MPO-ANCA阳性的特发性ILD患者或在随访期间转为MPO-ANCA阳性的患者可发展为MPA,临床医生应特别注意DAH的存在,因为这种并发症可能是致命的。对于MPA-ILD患者,首先应通过抗炎治疗控制MPA。当存在MPO-ANCA阳性ILD伴UIP模式(包括PF-ILD伴MPA)时,尽管进行了抗炎治疗,临床医生仍需要仔细判断纤维化引起的炎症是否占主导。当抗炎治疗和抗纤维化治疗难以取舍时,合并感染和AE的ILD高危患者应优先选择抗纤维化治疗。由于MPO-ANCA阳性ILD可导致全身血管炎和(或)预后不良,因此,对患者进行长期监测很重要。肺科医生、风湿病医生、放射科医生和病理学家之间的多学科协作有助于MPO-ANCA阳性患者的治疗。 文章摘译自:Yamakawa H, Toyoda Y, Baba T, et al. Anti-Inflammatory and/or Anti-Fibrotic Treatment of MPO-ANCA-Positive Interstitial Lung Disease: A Short Review. J Clin Med. 2022 Jul 1;11(13):3835. 聚群英,促交流 “风湿界读者之家” 欢迎您的加入!返回搜狐,查看更多 |
【本文地址】
今日新闻 |
推荐新闻 |