【前沿】质谱技术在多组学中的前景及挑战 |
您所在的位置:网站首页 › MALDITOFMS进行细菌鉴定的主要标志是 › 【前沿】质谱技术在多组学中的前景及挑战 |
【前沿】质谱技术在多组学中的前景及挑战
|
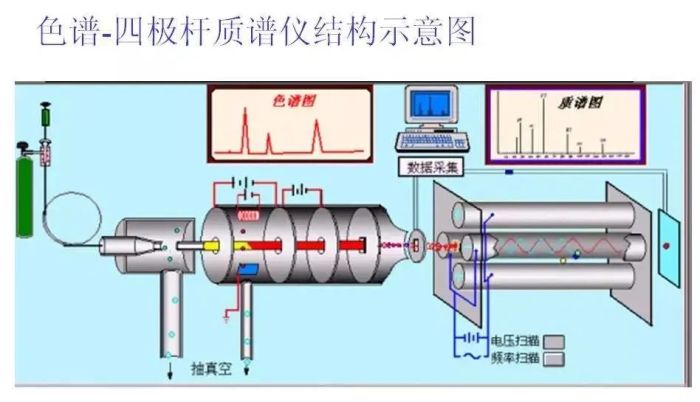
传统医学模式正进入到基因组学、蛋白质组学、代谢组学等多组学整合分析的精准诊断时代。以高性能质谱为核心的多组学研究已成为各类疾病筛查、早期诊断、治疗监测和预后评估的生物标志物创新发现的关键技术平台。 质谱仪是一种通过测量相对分子质量或质荷比鉴定物质的分析工具,质谱仪通常由3个基本部分组成:即离子源、质量分析器和检测器。通过将双重/多重质量分析仪串联起来或与气相色谱、液相色谱、毛细管电泳等技术平台联用,可以提高质谱仪的分析性能。
发现检验生物标志物 以高性能质谱为核心的组学研究已成为发现检验生物标志物的主要来源,生物标志物是指用于疾病诊断、风险评估及预后判断的生物分子,组学领域的扩展和检测技术手段的进步不断拓展了生物标志物的范畴。 目前生物标志物不仅涵盖了传统的核酸、蛋白质、糖类及代谢物等标志物类型,还囊括细胞遗传学和细胞动力学参数,以及体液中的外泌体、细胞等。在过去的几十年里,研究者用各种组学技术致力于生物标志物的发现和疾病的早期诊断,质谱技术作为组学研究的核心技术,其在生物标志研发策略方面的科学价值和优势越来越受到检验医学的重视。 1、质谱技术正成为蛋白质组学研究和临床应用的关键技术 蛋白质作为直接参与细胞生物学过程的大分子,是生理功能的执行者和生命现象的直接体现者,蛋白质水平的变化直接反映了生命在生理或病理条件下的变化,可以精准地预测疾病的状况和进展。 临床蛋白质组学中有2种策略可以识别生物标志物, 一是经典策略,使用电泳技术分离蛋白质和多肽混合物然后进行质谱鉴定;二是利用质谱技术分析样品的完整质谱图,以获得可以用作疾病“指纹”的完整蛋白质/肽谱。 组织、器官、体液和细胞培养物等生物样品均可被用作为蛋白质类生物标志物的研究,但从临床诊断的角度来看,体液无疑是寻找生物标志物的最佳材料。蛋白质组学研究的一个重大挑战是蛋白质数据库的多样性分析及蛋白质、多肽鉴定,质谱技术较好地解决了这些难题,满足了蛋白质组学对技术平台的需求。 ESI和MALDI 2种“软”电离方法使基于质谱的蛋白质组学蓬勃发展,MALDI通过激光辐射将与基质共结晶的蛋白质电离,而ESI将蛋白质样品电离出溶液,可以很好地保存目标分子的完整性,从而实现高灵敏度和高准确度的质量分析。 MALDI通常与飞行时间联合用于蛋白质鉴定,而ESI的优势在于可以直接与液相色谱对接,用于从高度复杂的混合物中分析蛋白质。不同类型的质谱仪根据需要可以用于蛋白质的鉴定和定量分析、蛋白质翻译后的修饰研究、蛋白质相互作用分析等。 病变细胞或微环境产生的蛋白质或蛋白质片段可以在疾病发生和发展过程中扩散到循环系统中,通过质谱法测定其浓度,利用生物信息学工具进行数据分析后用于诊断。在过去的二十多年中,以质谱为核心的蛋白质组学成为分子临床医学研究的重要平台,并发现了一批涉及各种疾病的生物标志物。通过对不同类型癌症患者的血浆、血清及尿液蛋白质组学分析,发现了一系列与癌细胞形成和发展相关的蛋白质标志物,用于许多类型的癌症诊断,包括卵巢癌、前列腺癌、乳腺癌、膀胱癌、肾癌、肺癌、胰腺癌、星形胶质瘤等,这些标志物不仅可以对癌症进行筛查、诊断和预后监测,同时还可以对癌症的亚型进行分类。 外泌体蛋白质组学成为发现癌症标志物的一个新研究方向,外泌体蛋白标志物不仅可以区分组织中肿瘤与非肿瘤细胞,而且还可以确定肿瘤的原发灶。通过对胰腺癌患者血浆及血浆中外泌体的蛋白质组学分析,发现了外泌体携带的与胰腺癌相关的蛋白会引起体内的免疫反应并由此产生自身抗体,其中M2-型丙酮酸激酶和人可溶性半乳糖凝集素3结合蛋白产生的自身抗体可以比较好地区分早期胰腺导管腺癌与健康人群、早期胰腺导管腺癌与胰腺炎。 对于一些特殊类型疾病,如阿尔茨海默病(AD)、帕金森病(PD)、系统性硬化症(SSc)等,由于不完全清楚发病机制,其诊断和治疗面临巨大挑战,蛋白质组学的发展和质谱技术的进步促进了这些疾病新标志物的发现。 SSc是一种临床表现为纤维化引起的皮肤增厚,内脏纤维化和血管纤维性增生的系统性疾病,目前认为其与免疫系统异常(细胞、体液免疫反应与自身抗体的合成)相关。多个研究组采用质谱技术对患者的血清、唾液、支气管肺泡灌洗液的蛋白质组成进行研究,发现钙离子通道家族成员、钙调蛋白、网状局部蛋白1和网状局部蛋白3等可作为其诊断的候选生物标志物。 对蛋白类生物标志物的临床诊断强烈依赖以抗原-抗体反应为核心的各种免疫分析方法,放射免疫分析因放射性污染而被淘汰,电化学发光目前仍是主流的分析平台。 免疫分析法有不可避免的局限性: 一次分析只能检测到一种蛋白或有不同转录后修饰形式的蛋白;检测结果受所使用的抗体特异性和稳定性的限制,抗体对目标蛋白不能完全地识别而导致测定结果的偏差。 与之相比,质谱可以在蛋白质组层面对某种疾病进行整体而全面地分析,包括蛋白翻译后修饰和源自基因组畸变的变体,一次质谱分析可以同时准确测定数十种蛋白,实现多项指标联合检测的目的;质谱通过测定目标蛋白的特异性肽段(即一段氨基酸序列)的水平来准确地表征目标蛋白的水平,其特异度更好。这些优势不仅巩固了基于质谱的临床蛋白质组学在标志物开发方面的优势,而且还加速了其向常规分析和临床实践的转变。利用质谱检测这些标志物并推广到临床还面临诸多挑战: (1)样品一般需要酶解消化、同位素标记等复杂的前处理过程,耗时较长,且亟须建立严格的标准操作程序; (2)多种仪器平台、电离技术并存,各有优势和局限性,难以形成如基因组研究比较一致的方法; (3)目前的技术瓶颈导致特征肽段分析并不能完全代表蛋白质的水平,且单次质谱分析仅能分析1个标本,限制了临床检测通量; (4)质谱分析产生的大型数据库需要更完备的数据分析策略,不同研究组间的结果的可比性及重复性较差,需要大量的样本验证。 2、质谱技术是代谢物类标志物检测的最佳平台 代谢组学研究生物体中相对分子质量 |
【本文地址】
今日新闻 |
推荐新闻 |