铁红(主要成分为Fe2O3)是一种用途广泛的颜料,用废铁屑制备铁红的流程如下:(1)操作Ⅰ... |
您所在的位置:网站首页 › FeOOH制备铁红的化学方程式 › 铁红(主要成分为Fe2O3)是一种用途广泛的颜料,用废铁屑制备铁红的流程如下:(1)操作Ⅰ... |
铁红(主要成分为Fe2O3)是一种用途广泛的颜料,用废铁屑制备铁红的流程如下:(1)操作Ⅰ...
|
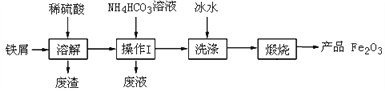
铁红(主要成分为Fe2O3)是一种用途广泛的颜料,用废铁屑制备铁红的流程如下:
(1)操作Ⅰ的名称是_________。 (2)检验FeCO3沉淀是否洗净的实验方法是________。 (3)加入NH4HCO3溶液的反应除了生成FeCO3沉淀,还会生成一种气体,生成气体的离子方程式为________。 (4)在空气中煅烧FeCO3的化学方程式是________,若煅烧不充分,产品Fe2O3中会有FeO,为了避免产品中有FeO,可以采取的措施是________。 (5)称取3.0 g 产品,用稀硫酸溶解,逐滴加入0.10 mol·L-1 KMnO4溶液20.00 mL,二者恰好反应完全。若此产品中只含有FeO、Fe2O3,求算产品中Fe2O3的质量分数,写出计算过程___。 (已知:10FeSO4+2KMnO4+8H2SO4===5Fe2(SO4)3+2MnSO4+K2SO4+8H2O) 高一化学综合题困难题查看答案及解析 铁红(主要成分为Fe2O3)是一种用途广泛的颜料,用废铁屑制备铁红的流程如下:
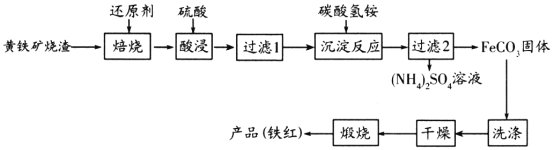
(1)操作Ⅰ的名称是_________。 (2)检验FeCO3沉淀是否洗净的实验方法是________。 (3)加入NH4HCO3溶液的反应除了生成FeCO3沉淀,还会生成一种气体,生成气体的离子方程式为________。 (4)在空气中煅烧FeCO3的化学方程式是________,若煅烧不充分,产品Fe2O3中会有FeO,为了避免产品中有FeO,可以采取的措施是________。 (5)称取3.0 g 产品,用稀硫酸溶解,逐滴加入0.10 mol·L-1 KMnO4溶液20.00 mL,二者恰好反应完全。若此产品中只含有FeO、Fe2O3,求算产品中Fe2O3的质量分数,写出计算过程___。 (已知:10FeSO4+2KMnO4+8H2SO4===5Fe2(SO4)3+2MnSO4+K2SO4+8H2O) 高一化学综合题困难题查看答案及解析 黄铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用黄铁矿烧渣为原料制备高档颜料—铁红(Fe2O3)的流程如下:
回答下列问题: (1)“焙烧”时所添加的最佳还原剂是________(填序号)。 a.焦炭 b.硫黄 c.镁粉 d.锌粉 (2)“过滤1”后的滤液中溶质的主要成分是________________(填化学式)。 (3)“沉淀反应”时反应温度不宜过高,其原因为________(用化学方程式表示)。 (4)为检验FeCO3是否洗涤干净,可以向最后一次洗涤液中滴加________溶液。 (5)在空气中煅烧FeCO3生成铁红和另一种氧化物,反应的化学方程式为________。 (6)现有黄铁矿烧渣500t,铁元素的质量分数为16.8%,经过一系列转化后,得到90t铁红,该产品的产率为________。(提示: 高一化学工业流程中等难度题查看答案及解析 黄铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用黄铁矿烧渣为原料制备高档颜料—铁红(Fe2O3)的流程如下:
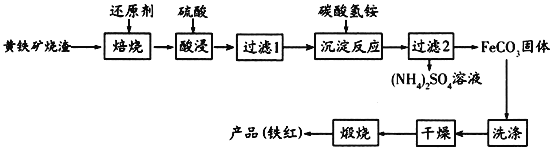
回答下列问题: (1)“焙烧”时所添加的最佳还原剂是________(填序号)。 a.焦炭 b.硫黄 c.镁粉 d.锌粉 (2)“过滤1”后的滤液中溶质的主要成分是________________(填化学式)。 (3)“沉淀反应”时不宜混入过多空气,其原因为______________________(用离子方程式表示)。 (4)为检验FeCO3是否洗涤干净,可以向最后一次洗涤液中滴加________溶液。 (5)在空气中煅烧FeCO3生成铁红和另一种氧化物,反应的化学方程式为________。 (6)现有黄铁矿烧渣500t,铁元素的质量分数为16.8%,经过一系列转化后,得到90t铁红,该产品的产率为________。(提示: 高一化学工业流程中等难度题查看答案及解析 氧化铁的用途较为广泛。工业上用废铁屑制备氧化铁的流程如图:
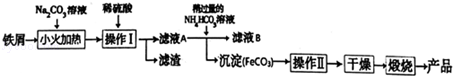
(1)“溶解”时主要反应的离子方程式为___。 (2)操作Ⅰ的名称是___。 (3)加入 NH4HCO3溶液生成FeCO3沉淀和CO2,则“废液”中含有的主要离子有___。 (4)在空气中煅烧FeCO3可得产品Fe2O3,写出该反应的化学方程式:___。实际生产时,产品Fe2O3中常混有FeO。为了减少FeO,“煅烧”时可以采取的措施有___(写一条)。 (5)产品Fe2O3与A粉的混合物称为铝热剂,可用于焊接铁轨。该反应的化学方程式为___。 高一化学工业流程简单题查看答案及解析 氧化铁是重要的工艺颜料,用废铁屑制备它的流程如下:回答下列问题:
(1)①加碳酸钠溶液并小火加热的操作目的是 ; ②操作Ⅰ的名称是 ,操作Ⅱ的名称是 ; (2)①流程所发生的反应为FeSO4+2NH4HCO3=FeCO3↓+(NH4)2SO4+CO2↑+H2O过程中,加入稍过量的NH4HCO3溶液后,且要控制溶液的为6.8~7.2之间.加入稍过量的目的是 ,溶液的pH不能过低的原因是 ②检验滤液B中含有NH4+的方法是 . (3)有些同学认为KMnO4溶液滴定能进行铁元素含量的测定. a、称取2.85g绿矾(FeSO4•7H2O)产品,配成250mL溶液; b、量取25.00mL待测溶液于锥形瓶中; c、用硫酸化的0.0100mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL. ①写出酸性KMnO4溶液与FeSO4溶液反应的离子方程式 . ②用KMnO4标准溶液滴定时应选用 滴定管(填“酸式”或“碱式”). ③计算上述样品中FeSO4•7H2O的质量分数为 . 高一化学实验题困难题查看答案及解析 硫铁矿烧渣的主要成分为 Fe2O3、Fe3O4,以及少量 SiO2、Al2O3 等。由硫铁矿烧渣制备铁红(Fe2O3) 的一种工艺流程如下:
已知:还原焙烧时,大部分 Fe2O3、Fe3O4 转化为 FeO。 几种离子开始沉淀和完全沉淀时的 pH 如下表所示:
(1) “酸浸、过滤”步骤中所得滤液中的金属阳离子有(填离子符号)______________。 (2)Fe 粉除调 pH 外,另一作用是___________;Fe 粉调节溶液的 pH 范围为__________。 (3) 已知“沉铁、过滤”中生成沉淀为碳酸铁沉淀,则高温条件下,“氧化”步骤中发生反应的化学方程式为______________。 (4) Fe2O3 也是赤铁矿的主要成分,工业上若要得到 120t 纯度为 93%生铁需要含杂质 20%的(杂质不含铁 元素)赤铁矿的质量为________。 高一化学填空题中等难度题查看答案及解析 铁黄是一种重要的颜料,化学式为Fe2O3•xH2O,广泛用于涂料、橡胶、塑料、文教用品等工业。实验室模拟工业利用硫酸渣(含Fe2O3及少量的CaO、MgO等)和黄铁矿粉(主要成分为FeS2)制备铁黄的流程如图:
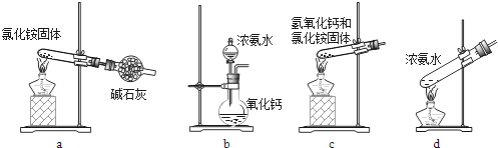
(1)操作Ⅰ与操作Ⅱ中都用到玻璃棒,玻璃棒在两种操作中的作用分别是________、________。 (2)试剂a最好选用______(供选择使用的有:铝粉、空气、浓HNO3);其作用是________。 (3)上述步骤中需用到氨气.下列装置可用于实验室制氨气的是______(填序号)。
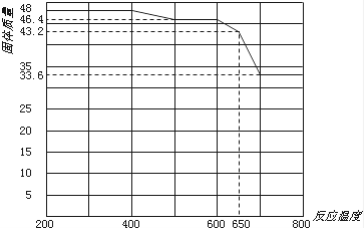
(4)检验溶液Z中含有NH4+的方法是________。 (5)查阅资料知,在不同温度下Fe2O3被CO还原,产物可能为Fe3O4、FeO或Fe,固体质量与反应温度的关系如下图所示。
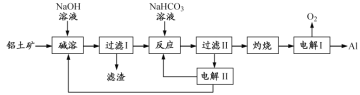
根据图像推断650℃时Fe2O3还原产物的化学式为________,并设计一个简单的实验,证明该还原产物的成分(简述实验操作、现象和结论)________。仪器自选。可供选择的试剂:稀H2SO4、稀盐酸、H2O2溶液、NaOH溶液、KSCN溶液。 高一化学综合题困难题查看答案及解析 铝是应用广泛的金属。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:
注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。 (1)“碱溶”时生成偏铝酸钠的离子方程式为___________________________________________。 (2)“过滤Ⅰ”中所用到的玻璃仪器有___________________________________________。 (3)“过滤Ⅱ”中得到的固体中混有杂质,需要对沉淀进行洗涤,请你叙述如何洗涤?_______。 高一化学实验题中等难度题查看答案及解析 某校研究性学习小组用一些大部分已经锈蚀(成分为 Fe2O3)的废铁屑制备绿矾(FeSO4·7H2O),实验操作过程如下:
已知:杂质不溶于稀硫酸。 请回答下列问题: (1)步骤①中,稀硫酸与 Fe2O3反应的离子方程式为 ______,废铁屑用硫酸处理后,还含有不溶性杂质,为获取澄清的A溶液,需进行的操作名称是 _________。 (2)步骤②中溶液A与铁粉反应的离子方程式为________________。 (3)检验溶液 B 中是否还存在杂质金属阳离子的方法是_______。 高一化学综合题中等难度题查看答案及解析 |
【本文地址】
今日新闻 |
推荐新闻 |